Vervaardiging, karakterisering en cytotoxiciteit van sferisch gevormde geconjugeerde van goudkokkelschil afgeleide calciumcarbonaat nanodeeltjes voor biomedische toepassingen
Abstract
De evolutie van nanomateriaal in de wetenschap heeft geleid tot een groeiende toename van nanotechnologie, biogeneeskunde en technische velden. Deze studie was gericht op fabricage en karakterisering van geconjugeerde van goudkokkelschelp afgeleide calciumcarbonaat nanodeeltjes (Au-CSCaCO3 NP's) voor biomedische toepassing. De gebruikte synthetische techniek gebruikte gouden nanodeeltjes citraatreductiemethode en een eenvoudige precipitatiemethode in combinatie met mechanisch gebruik van een programmeerbare roller-ball mill. Het gesynthetiseerde geconjugeerde nanomateriaal werd gekarakteriseerd voor zijn fysisch-chemische eigenschappen met behulp van transmissie-elektronenmicroscoop (TEM), veldemissie scanning-elektronenmicroscoop (FESEM) uitgerust met energiedispersieve röntgenstraling (EDX) en Fourier-transformatie-infraroodspectroscopie (FTIR). De complexiteit van cellulaire mechanismen kan echter een uitdaging zijn voor nanomateriaal zoals Au-CSCaCO3 NP's en dus de behoefte aan beoordeling van cytotoxiciteit. De verkregen bolvormige nanodeeltjes (lichtgroen paarsachtig) hebben een gemiddelde diameter van 35 ± 16 nm, een hoge koolstof- en zuurstofsamenstelling. Het geconjugeerde nanomateriaal bezit ook unieke spectra voor aragonietpolymorf en carboxylbindingen die interacties tussen geconjugeerde nanodeeltjes aanzienlijk ondersteunen. De negatieve oppervlaktelading en spectra-absorptie benadrukten hun stabiliteit. De resulterende bolvormige geconjugeerde Au-CSCaCO3 NP's kunnen een geweldig nanomateriaal zijn voor biomedische toepassingen.
Achtergrond
De productie van monodisperse nanodeeltjes is belangrijk gebleken in elektronische, optische, biomedische en magnetische toepassingen [1,2,3,4]. Hun evolutie en die van biomaterialen heeft de farmaceutische industrie [5], biomedische systemen [6], medicijnafgiftesystemen [7], cosmetica en waterbehandeling [7,8,9] gunstig verbeterd. In hetzelfde opzicht zou de ontwikkeling van geconjugeerde materialen die biocompatibel, biogeen en niet-toxisch zijn, waardevolle bijdragen kunnen leveren op het gebied van biowetenschap en biogeneeskunde [10]. Bovendien zou biocompatibel metallisch geconjugeerd bio- en nanomateriaal kunnen bijdragen aan meer wetenschappelijke vooruitgang voor biomedische toepassingen zoals weefselmanipulatie [5], therapieën [11] en medicijnafgifte [12]. Dit is uitvoerig aangetoond in recente werken, zoals het gebruik van injecteerbare zelfassemblerende collageen-goud hybride hydrogel [13], colloïdale goud-collageen core-shell nanoconjugaten [14] en co-geassembleerde dragervrije nanomedicijnen voor antitumortherapie [15]. Een aantal studies hebben ook gedocumenteerd dat metalen nanodeeltjes enzymelektroden kunnen produceren in elektrochemische biosensoren met anorganische niet-silica poreuze materialen [16]. Bovendien hebben de gesynthetiseerde grafeenoxide-albumine nanohybriden ook hun potentiële voordeel getoond voor verbeterde fotodynamische therapie [17]. Al met al heeft dit alleen maar meer interesse gewekt bij andere mogelijke toepassingen zoals biomedische beeldvorming en biosensorische systemen [16, 18].
Calciumcarbonaat als een ruw, natuurlijk mineraal is gebruikt in een breed scala aan toepassingen, waaronder biomedische, industriële en nanotechnologie [10, 19,20,21]. Aragoniet als een polymorf van calciumcarbonaat komt rijkelijk voor in kokkelschelp (Anadara granosa ), een in de volksmond ook in Maleisië aangetroffen weekdier [22]. Aragoniet is biogeen in tegenstelling tot de andere calciumcarbonaatpolymorfen van calciet en vateriet, en vormt tot 95-98% van de kokkelschaal. Calciumcarbonaat, een anorganisch materiaal van aragonietpolymorf, komt van nature en algemeen voor in de kokkelschelpen [23]. Aragonietpolymorf heeft steeds meer de aandacht getrokken in het onderzoeksveld vanwege de biocompatibiliteitseigenschappen en het veelbelovende potentieel bij de ontwikkeling van antikankergeneesmiddelafgiftesystemen [24] en biomedische beeldvorming [25, 26]. Momenteel hebben de meeste eerdere onderzoeksstudies hoofdzakelijk twee methoden voor de productie van calciumcarbonaat onthuld [26]. Ze omvatten de co-precipitatie of dubbele ontleding en carbonatatie van CO2 gas door calciumhydroxide onder gecontroleerde instellingen, die helaas geen biogeen calciumcarbonaat produceert [26,27,28]. Daarom bevatten de producten een mengsel van calciet en vateriet in grote hoeveelheden die ongeschikt zijn voor biomedisch gebruik vanwege hun niet-biocompatibiliteit en hoge toxiciteitsrapporten [26].
Met het toenemende gebruik van nanotechnologie in biomedische toepassingen, is de huidige studie echter gericht op de synthese van gecontroleerde kokkelschil-afgeleide calciumcarbonaat nanodeeltjes (CSCaCO3 NP's) met unieke grootte en vorm met behulp van dodecyldimethylbetaïne (BS-12) [29]. Dit is geïnspireerd op eerdere werken die BS-12 gebruiken als katalysator voor biomineralisatie bij de synthese van CSCaCO3 NP's die gemakkelijk kunnen worden gemanipuleerd voor bio-toepassingen, kostenefficiënt zijn en relatief zuivere nanodeeltjes [30]. De morfologie en grootte van gesynthetiseerde nanodeeltjes zijn cruciaal bij het bepalen van hun fysisch-chemische eigenschappen, met de nadruk op metalen nanodeeltjes gezien hun enorme potentiële biomedische toepassingen [31]. Gouden nanodeeltjes (AuNP's) zijn continu gebruikt vanwege hun optische eigenschappen, verschillende groottebereik en kleur die afhankelijk zijn van absorptiemaxima-variaties of de gebruikte synthesemethode [32]. De grootte en vorm van AuNP's beïnvloeden hun absorptie- en emissiekenmerken in het zichtbare lichtspectrum, waardoor ze variëren van zichtbare tot nabij-infraroodgebieden. Daarom kunnen ze vanwege hun synthese [33], fysisch-chemische eigenschappen [34], biocompatibiliteit [35] en oppervlaktefunctionalisering [36] worden gemanipuleerd voor verschillende en specifieke toepassingen [37]. Daarnaast is ook gesteld dat ze in de medische diagnostiek niet volledig worden gebruikt en dat hun waarde mogelijk onduidelijk is [37].
Dus misschien kunnen ze na de juiste functionalisering opnieuw worden ontworpen voor kankerbeeldvorming [38], kankerbehandeling [39], medicijnafgifte [40] en sensorische gadgets [41]. Een coating is essentieel om nanohybride biomateriaal te fabriceren met gefunctionaliseerde eigenschappen zoals gouden nanodeeltjes (AuNP's) geconjugeerd met poreuze calciumcarbonaat nanobolletjes [16, 42]. Het resulterende geconjugeerde goud-calciumcarbonaat nanomateriaal of nano-composiet hybride, die de voordelige ouderlijke eigenschappen zoals biocompatibiliteit, goede oplosbaarheid en dispergeerbaarheid in oplossing zou kunnen behouden [16]. Geconjugeerde gouden nanodeeltjes die een sterke kleurverandering en gelokaliseerde oppervlakteplasmonresonantie (LSPR) vertonen, zouden uitstekende kandidaten kunnen zijn voor potentiële meerdere receptorsystemen zoals aptameren, peptiden en antilichamen [35, 43,44,45]. De fabricage van in water oplosbare geconjugeerde polymeren en de toepassingen ervan in biosensoren, fluorescentiebeeldvorming en medicijnafgifte zijn met succes gerealiseerd [46,47,48]. De geconjugeerde nanodeeltjes of het nanomateriaal hebben echter in de loop der jaren steeds betere voordelen zoals fotostabiliteit [48, 49] en lage cytotoxiciteit [50], behalve een vriendelijkere voorbereiding [51] en scheidingskenmerken [48].
Hierbij de AuNP's en CSCaCO3 NP's worden controleerbaar gesynthetiseerd en gebruikt voor het fabriceren en karakteriseren van biogene geconjugeerde van goudkokkelschelp afgeleide calciumcarbonaat nanodeeltjes (Au-CSCaCO3 NP's) waarvan de diameter varieert van 19-51 nm. Aanvankelijk is de AuNPs-bereiding geïnspireerd op de klassieke Turkevich-methode [52] en de van de kokkelschil afgeleide nanodeeltjes met behulp van de dodecyl-dimethylbetaïne-synthetische benadering [26]. De modificaties in de synthetische parameters zoals concentratie zouden hun omvang vakkundig kunnen verkleinen of vergroten. Bijgevolg werd het gesynthetiseerde nanomateriaal gekarakteriseerd en onderzocht op cytotoxiciteit. De Au-CSCaCO3 NP's voorbereiding extra voordelen zijn; gemakkelijke synthese en kostenefficiëntie.
Methoden/experimenteel
Materialen en chemische reagens
Het goudzout (tetrachloorgoudzuur dat 49% goudoplossing bevat) en het trinatriumcitraat werden gekocht bij prima nexus Sdn Bhd (Maleisië). Verse kokkelschelp werd verkregen van de lokale markt (Pasar borong, Seri Kembangan, Selangor, Maleisië). Dodecyldimethylbetaïne (BS-12) en indocyaninegroene kleurstof (ICG) werden gekocht bij Sigma-Aldrich (Steinheim, Duitsland). Dulbecco's gemodificeerd Eagle's medium (DMEM), foetaal runderserum (FBS), combinatie van antibiotica (glutamine 100 mmol/L, penicilline 100 E/ml en streptomycine 100 μg/ml), fosfaatgebufferde zoutoplossing (PBS), dimethylsulfoxide (DMSO ) en MTT (3-dimethylthiazo-2,5-diphynyltetrazoliumbromide-kleurstof) werden gekocht bij Naclai tesque, Inc., Kyoto, Japan. Alle andere gebruikte reagentia waren van analytische kwaliteit.
Synthese van gouden nanodeeltjes
De synthese werd bereikt met behulp van een methode die eerder is beschreven door Verma et al. [53] met lichte wijzigingen in concentraties, 1% tetrachloorgoudzuur met 49% goudoplossing. Ongeveer 0,1% van de goudoplossing werd bereid en verdund in een reeks concentraties van respectievelijk 15, 25 en 20 mM in verschillende erlenmeyers. De oplossingen werden vervolgens verwarmd tot 100°C op een hete plaat gekoppeld aan magnetisch roeren (6 gepositioneerd, WiseStir® Korea). Vervolgens werd ongeveer 1% trinatriumcitraat aan de kokende oplossing toegevoegd onder continu magnetisch roeren totdat een kleurovergang werd waargenomen (geelachtige goudoplossing werd kleurloos en vervolgens naar zwart en werd uiteindelijk briljant rood). De verwarming werd na 15 min uitgeschakeld en men liet ze afkoelen tot kamertemperatuur. De gesynthetiseerde gouden nanodeeltjes werden vervolgens bewaard bij -4 ° C voor verder gebruik. De reactie werd weergegeven in de onderstaande vergelijking:
$$ 2{\mathrm{H}\mathrm{AuCl}}_4+3{\mathrm{C}}_6{\mathrm{H}}_8{\mathrm{O}}_7\left(\mathrm{citric} \ \mathrm{acid}\right)\to 2\mathrm{Au}+3{\mathrm{C}}_3{\mathrm{H}}_6{\mathrm{O}}_5\left(3-\mathrm {ketoglutaric}\ \mathrm{acid}\right)+8\mathrm{HCl}+3{\mathrm{C}\mathrm{O}}_2 $$Voorbereiding en synthese van van kokkelschelp afgeleide calciumcarbonaat nanodeeltjes (CSCaCO3 NP's)
Drie kilo vers verkregen kokkelschelpen werden grondig schoongemaakt, geschrobd en gewassen. Het kokkelschelppoeder is geproduceerd volgens de methode beschreven door Islam et al. [54]. De schoongemaakte kokkelschaal werd 7 dagen in een oven (Memmert UM500, GmbH Co, Duitsland) bij 50°C gedroogd. De kokkelschelpen werden tot poeder gemalen met behulp van een blender (Blender HCB, 550, VS) en gezeefd met een roestvrijstalen laboratoriumtestzeef (Endecott Ltd., gemaakt in Londen, Engeland) met een opening van 90 m om poeder van microngrootte te verkrijgen. Het poeder werd 7 dagen bij 74°C in de oven gedroogd. Het poeder werd verder verpakt in een luchtdichte plastic zak van polyethyleen voor later gebruik. De van kokkelschelpen afgeleide calciumcarbonaat nanodeeltjes werden gesynthetiseerd volgens de benadering beschreven door Islam et al. [55], met kleine wijzigingen in de methode- en syntheseparameters. Twee gram kokkelschelppoeder werd in een erlenmeyer van 250 ml gebracht, gevolgd door 50 ml dubbel gedeïoniseerd water, en een concentratie van 0,5 ml BS-12 werd in de erlenmeyer toegevoegd. Het mengsel in de erlenmeyer werd krachtig geroerd bij 1000 tpm, bij een temperatuur van 50 ° C gedurende 135 minuten met behulp van een systematische multi-hete plaat en magnetische roerder met kleine magnetische staaf. Het bereide monster werd gescheiden van de moedervloeistof met behulp van filterpapier met dubbele ring van 125 mm (Filtres Fioroni, China). Het residu werd vervolgens grondig gewassen om de overmaat BS-12 te verwijderen. De eindproducten, CSCaCO3 NP-poeder, werden verpakt in een droge schone container en 3 dagen gedroogd (Oven Memmert UM500, GmbH Co, Duitsland) bij 74 ° C. De container was goed ingepakt en verzegeld met Para-film na toevoeging van meerdere kleine marmeren balletjes erin. De container werd gedurende 5 dagen op een programmeerbare walsmolen (BML-6, Wisemix® Korea) geplaatst met een snelheid van 200 tpm. Het monster werd voor verder gebruik in luchtdicht polyethyleen in de oven bewaard.
Synthese van geconjugeerde van goudkokkels afgeleide calciumcarbonaat-nanodeeltjes (Au-CSCaCO3 NP's) en samenwerking van Near Infrared (NIR) Dye
In deze procedure wordt 0,2 g CSCaCO3 NP's en 5 mg nabij-infrarood (NIR) Indocyanine-groene kleurstof (ICG) werden gedispergeerd in 20 ml gouden colloïde-oplossing (pH 7) (AuNPs-oplossing), zoals op dezelfde manier beschreven door Cai et al. [16], in een schone lege erlenmeyer. Verdere synthesemodificaties werden aangebracht, waarbij het monster 20 minuten werd gesoniceerd en gedurende 3 dagen op een magnetische roerder met een kleine magnetische staaf bij 200 tpm werd geïncubeerd. Het monster werd gedurende 10 minuten ultragecentrifugeerd met een snelheid van 10.000 tpm om lichtgroen-paars, Au-CSCaCO3 te verkrijgen. NP composiet. Het supernatant werd afgeschonken en de pellet werd gewassen met een reeks gedeïoniseerd water. Het bereide composietmateriaal werd 4 dagen in de oven gedroogd en voor verdere analyse in luchtdicht polyethyleen in de oven bewaard.
Karakterisatie van geconjugeerde van goudkokkelschil afgeleide calciumcarbonaatnanodeeltjes (Au-CSCaCO3 NP's)
De deeltjesgrootte en morfologie van het nanomateriaal werd geanalyseerd met behulp van transmissie-elektronenmicroscoop (TEM). Het nanomateriaal werd gedispergeerd in absolute alcohol en gedurende 40 minuten gesoniceerd. Ongeveer 5 l van de gesuspendeerde monsteroplossing werd gepipetteerd op een monsterbevestiging met koperen grip. Het monster werd bekeken onder TEM (Hitachi H-7100). De veldemissie scanning elektronenmicroscoop (FESEM) (Model JOEL 7600F) werkte bij een spanning van 5 KV en was uitgerust met een energiedispersieve röntgenspectroscopie-eenheid (EDX). Dit werd gebruikt om de oppervlaktekenmerken van de Au-CSCaCO3 . te karakteriseren NP's. Het materiaal werd gedispergeerd in absolute alcohol en 1 uur gesoniceerd. Ongeveer 50 μl van de gesuspendeerde monsteroplossing werd gepipetteerd op een monsterhouder met koperen grip, een nacht gedroogd en gescand met behulp van de elektronenstralen. Bovendien werd de Fourier-transformatie-infraroodspectrometer (FTIR) ook gebruikt voor functionele analyse van het gesynthetiseerde geconjugeerde nanomateriaal; het nanomateriaal is gekalibreerd in 1 gew.% in Ker (FTIR Model 100, Perkin Elmer) in het bereik van 400-4000 cm −1 . Verder werd analyse voor de gesynthetiseerde nanoconjugaatgrootte en zeta-potentiaal gedaan met behulp van zetasizer (Nano ZS, Malvern Instruments). Het materiaal werd gesuspendeerd in gedeïoniseerd water en 50 minuten gesoniceerd; de homogene suspensie werd in de zetasizer-cuvet afgezet en onderzocht op deeltjesgrootte en zeta-potentiaal. De aanwezigheid van verschillende analyten van de geconjugeerde nanocomposiet werd gevolgd met behulp van een Uv-Vis-spectrofotometer (UV - 2600) bij verschillende golflengten variërend van 300 tot 800 nm.
Celkweek- en cytotoxiciteitsonderzoeken
Menselijke borstadenocarcinoomcellijn (JCRB:MCF-7) en de muisfibroblastcellijn (JCRB:NIH3T3) werden gekweekt in DMEM (hoge glucose) aangevuld met 10% FBS en een combinatie van antibiotica (glutamine 100 mmol/L, penicilline 100 E/ ml en streptomycine 100 g/ml). De kweekkolven (Eppendorf-cultuur T-25 en T-75) werden geïncubeerd in 5% kooldioxide bij 37 ° C en cellen bij 80-90% confluentie werden gebruikt voor het zaaien en het behandelingsproces.
Het zaaien en behandelen van cellen
De cellen werden uitgezaaid in steriele platen met 96 putjes met een dichtheid van 5 × 10 3 cellen per putje en gedurende 24 uur 's nachts geïncubeerd. De media in elk putje werden verwijderd en de cellen werden behandeld en samen gekweekt in replica's met geconjugeerde nanocomposietsuspensie (Au-CSCaCO3 NP) voor een periode van 24, 48 en 72 uur. Nadat de blootstelling aan de behandeling was voltooid, werden de media in de putjes afgezogen en gewassen met PBS voordat ze werden vervangen door een ander vers medium voorafgaand aan experimentele behandelingen.
Voorbereiding van Au-CSCaCO3 NP's voor behandeling
Voorraadoplossing van Au-CSCaCO3 NP's met een concentratie van 1 mg / ml in 10% serumvrije DMEM-media werden bereid. Na celzaaien van MCF-7-cellen en NIH3T3-cellen in platen met 96 putjes, werden de platen behandeld en geïncubeerd met verschillende concentraties in microgram (100-1,56) van de Au-CSCaCO3 NP's oplossingen.
(MTT) 3-dimethylthiazo-2, 5-diphynyltetrazoliumbromide-reagensbereiding en protocol
Typisch werd 5 mg MTT-reagenspoeder opgelost in 1 ml PBS, vergemakkelijkt door ultrasoonapparaatvortex voor een uniform mengsel. Na het zaaien en behandelen van de cellen werden de putjes geklaard en werd 20 μl MTT-reagens aan elk putje toegevoegd. Onmiddellijk daarna mochten de platen 3-4 uur incuberen om binding van de MTT aan de mitochondriën van de cellen mogelijk te maken. Na incubatie werd 1 ml DMSO aan elk van de putjes toegevoegd, waardoor het kleurproduct in de oplossing vrijkwam. De platen werden 30 minuten in een donkere kamer bewaard en de optische dichtheid (OD) van de oplossing werd gemeten met een microplaatlezer bij een golflengte van 570 nm [56]. De experimenten werden voor elke cellijn in drievoud uitgevoerd en de gemiddelde waarden werden geregistreerd. Het percentage levensvatbaarheid van de cellen werd bepaald met behulp van de onderstaande formule.
$$ \mathrm{Percentage}\ \mathrm{of}\ \mathrm{cell}\ \mathrm{viability}=\left(\ A\ Sample/A\ Control\right)\times 100 $$waar A Voorbeeld was de gemiddelde OD-waarde van verschillende geïncubeerde behandelde cellen van beide cellijnen en A Besturing was de gemiddelde OD-aflezing van de verschillende geïncubeerde cellen in alleen complete kweekmedia. De cytotoxiciteit van de cellen werd vervolgens beoordeeld aan de hand van de gemiddelde drievoudige waarden en vertoonde als gemiddelde ± standaarddeviatie (SD).
Statistische analyse
Statistische gegevensanalyse werd uitgevoerd met behulp van SPSS-software (versie 10, Chicago, VS). De experimenten werden in drievoud uitgevoerd en uitgedrukt als gemiddelde ± standaarddeviatie (M ± SD). De significantiedrempel was p < 0.01.
Resultaten en discussie
Fysisch-chemische eigenschappen van het geconjugeerde Au-CSCaCO3 NP's
Transmissie-elektronenmicroscoop
Het doel van de TEM-microfoto's was om de grootte van het gesynthetiseerde geconjugeerde Au-CSCaCO3 NP's die goed verspreide nanodeeltjes vertonen met een gemiddelde diameter van 35 ± 16 nm binnen het bereik van (19-51 nm). De verschillen in grootte die werden toegeschreven aan de syntheseomstandigheden waren zoals weergegeven in Fig. 1.
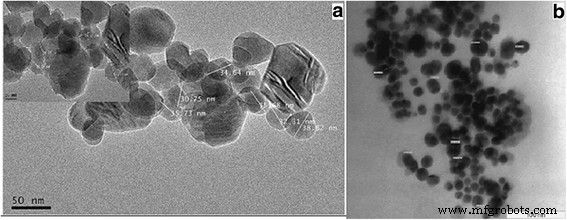
TEM (a , b ) afbeeldingen van de Au-CSCaCO3 NP's die hun verschillende grootte van de nanodeeltjes karakteriseren
TEM-microfoto's van het nano-conjugaat vertoonden een diameter van 19-51 nm en gedispergeerde nanodeeltjes. De uniek verkregen nanogrootte kan worden toegeschreven aan de gecontroleerde synthetische omstandigheden die worden gebruikt. Een andere mogelijke verklaring voor de dispersiteit van nanodeeltjes zou te wijten kunnen zijn aan de negatief geladen laag van citraationen die hielp bij de afstoting van nanodeeltjes van elkaar en ook, als gevolg van elektrostatische afstoting en de geconjugeerde hydratatie-oppervlaktelaag die aggregatie voorkomt en de stabiliteit van het conjugaat verhoogt, zoals op dezelfde manier wordt gerapporteerd door Jazayeri et al. [56]. Bovendien speelt het citraat-capping-reagens een rol bij de synthese, wat meer dispersiteit en stabiliteit van het nanodeeltjesconjugaat mogelijk maakte, zoals gerapporteerd door Rawat et al. [57]. De unieke deeltjesgrootte toonde de verschillende geabsorbeerde gouden nanodeeltjes in de nanobolmatrix van calciumcarbonaat, vergelijkbaar met het werk van Cai et al. [16], wat bijdraagt aan de waargenomen resulterende deeltjesgrootte. Dit resultaat bevestigt echter ook berichten dat calciet een slecht vermogen heeft om gouden nanodeeltjes te herbergen [16].
Field Emission Scanning Electron Microscopy (FESEM) en Energy Dispersive X-ray Spectroscopy (EDX)
De FESEM-microfoto beoordeelde de morfologie en vorm van de gesynthetiseerde nanodeeltjes die bolvormig en kettingachtig Au-CSCaCO3 vertoont NP's nanodeeltjes met een kleine mate van aggregatie zoals weergegeven in figuur 2. De elementaire spectra (figuur 2b) analyseerden de elementaire samenstelling van de geconjugeerde nanodeeltjes die 64,98% koolstof, 13,53% zuurstof, 0,02% calcium, 17,63% koper en 3,85% goud zoals weergegeven in tabel 1.

FESEM a FESEM-microfoto van de Au-CSCaCO3 NP's die de morfologie beschrijven. b EDX-spectra van de Au-CSCaCO3 NP's
FESEM-microfoto's beschreven de unieke morfologie als bolvorm, gladgemaakt oppervlak en kettingachtige gestructureerde geconjugeerde nanodeeltjes waarvan de fysische of chemische eigenschappen konden worden verklaard als gevolg van de bereidingsomstandigheden en synthetische methoden [58]. Evenzo was de sferische structurele aard die werd weergegeven door de geconjugeerde nanodeeltjes vergelijkbaar met die gerapporteerd door Verma et al. [53], maar in tegenstelling tot de geringe mate van aggregatie die wordt gepresenteerd. Een mogelijke verklaring voor deze uitkomst zou te wijten kunnen zijn aan de hydrofobe en elektrostatische interacties tussen de gouden nanodeeltjes en van de kokkelschil afgeleide calciumcarbonaat nanodeeltjes die leiden tot een sterke binding [48]. Bovendien werd de rol van BS-12 die bij de synthese werd gebruikt, weerspiegeld in de afbraak van de nanodeeltjes tot een bolvorm, analoog aan het werk dat is gedocumenteerd door Islam et al. [55]. Het elementaire profiel (Tabel 1) bracht geen significante veranderingen aan het licht in tegenstelling tot het verwachte resultaat. Evenzo zijn waargenomen bevindingen met de chemische samenstelling van de geconjugeerde nanodeeltjes gedocumenteerd zoals eerder getoond in eerdere werken [26, 54].
Oppervlaktelading en grootteverdeling naar intensiteit
Het zeta-potentieel van de geconjugeerde nanodeeltjes werd gedaan om hun oppervlaktelading, stabiliteit en grootteverdeling te beoordelen op basis van intensiteit die een negatieve lading van -16,4 ± -3,81 mV en een gemiddelde grootte van geconjugeerde nanodeeltjes van 57,97 nm onthult, zoals onthuld in Fig. 3 en Tabel 2.
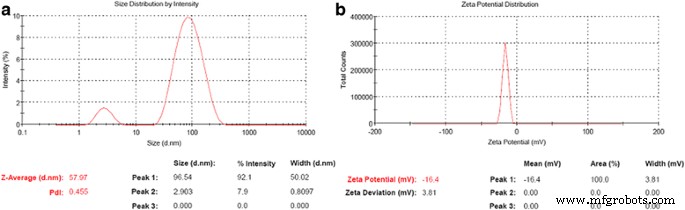
een Deeltjesgrootteverdeling naar intensiteit van de Au-CSCaCO3 NP's. b Zeta-potentiaal van de Au-CSCaCO3 NP's die de oppervlaktelading tonen
Zeta-potentiaal is een belangrijke test bij het beoordelen van de elektrostatische lading van nanodeeltjes die werd bepaald met behulp van zeta-sizer. Dit verklaarde verder de dispersiteit van het nanomateriaal in oplossing, waardoor we de algehele stabiliteit, houdbaarheid van nanodeeltjes, deeltjesinteracties tussen de geladen deeltjes en hun implicaties konden begrijpen [59]. De zeta-potentiaalbeoordeling van het geconjugeerde nanomateriaal gaf stabiliteit van de nanodeeltjes aan bij -16,4 mV en een polydispersiteitsindex (PdI) van minder dan 0,5. Een mogelijke verklaring zou kunnen liggen in de aanwezigheid van meer elektro-afstoting tussen de zwevende deeltjes tijdens de meting. Bovendien kunnen de agglomeratietendensen ook de grootteverdeling hebben beïnvloed, wat heeft geleid tot grotere afmetingen als gevolg van de synthetische methoden. Voorafgaand onderzoek door Hoque et al. heeft op vergelijkbare wijze gedocumenteerd [60] dat zeer positieve of negatieve zeta-potentiaal de aggregatie vermindert en de stabiliteit verhoogt. Bovendien kunnen de fysisch-chemische verschillen van de gesynthetiseerde nanodeeltjes worden toegeschreven aan de gebruikte synthesemethoden. De werken van Kanaujia en collega's [61] hebben ook benadrukt dat hogere negatieve of positieve waarden van zeta-potentiaal wijzen op stabiliteit en aggregatie van deeltjes voorkomen, vanwege elektrische afstoting die de dispersie van nanodeeltjes elektrisch stabiliseert, ook gerapporteerd door Isa et al. [62].
Fourier–Transform Infrarood spectrometer (FTIR)
Het FTIR-spectrum van Au-CSCaCO3 NP's laten zien dat de meest opvallende piek verscheen bij 1455,09 cm −1 gevolgd door pieken waargenomen bij 1059,12 cm −1 , 854,80 cm −1 , en 464,16 cm −1 , respectievelijk. Er werden ook zwakke pieken waargenomen bij 706,40 cm −1 en 1785,68 cm −1 zoals weergegeven in Afb. 4.
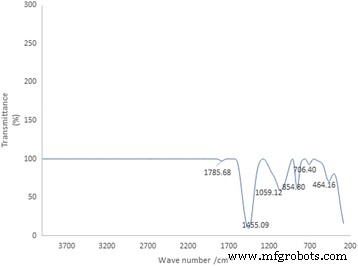
Fourier transformatie infrarood spectrometer spectrum van de belangrijkste karakteristieke pieken van Au-CSCaCO3 NP's. Alle markeringen komen overeen met de frequenties die in de tekst worden besproken
Het FTIR-spectrum van Au-CSCaCO3 NP's zoals gepresenteerd toonden aan dat de meest opvallende piek verscheen bij 1455,09 cm −1 , wat wijst op de zuurstof-waterstof (O–H) bindingen die aanwezig zijn in carboxylgroepen van gouden nanodeeltjes [14] en kokkelschaal nanodeeltjes, gevolgd door pieken die het best de aanwezigheid van aragoniet polymorf marker vertoonden waargenomen op 1059,12 cm −1 , 854,80 cm −1 , en 706,40 cm −1 , waarvan bekend is dat ze een alkylgroep rapporteren die voorkomt in de van kokkels afgeleide nanodeeltjes die consistent waren met de spectrumpieken [55]. Evenzo werd de zwakke piek waargenomen bij 1785,68 cm −1 vanwege de aanwezigheid van een carboxylgroep [54], en een extra piek werd waargenomen bij 464,16 cm −1 . Alle pieken vertoonden significante kenmerken van de aanwezigheid van covalente bindingen, koolstof-koolstof (C-C), koolstof-zuurstof (C-O) en koolstof-stikstof (C-N) bindingen waarvan de juiste functionele groepen aanwezig waren in onze geconjugeerde nanodeeltjes. De FTIR identificeerde in wezen de aanwezige functionele groepen door de infraroodspectrumpieken van het geconjugeerde nanomateriaal te verkrijgen en tegelijkertijd gegevens met een hoge spectrale resolutie te verzamelen over een breed spectraal bereik (400–4000 cm −1 ) [63]. Er wordt echter gemeld dat calcietpolymorf van calciumcarbonaat pieken heeft van 2000 tot 2900 cm −1 met de nanodeeltjes vervaardigd door de carbonatatiemethode [64].
Uv-Vis-spectrofotometer
De gesynthetiseerde geconjugeerde nanodeeltjes vertonen een zware absorptiepiek bij 530 nm, zoals weergegeven in figuur 5.
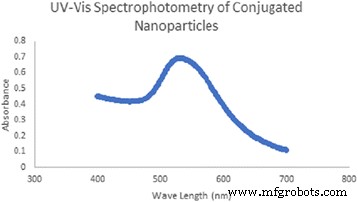
Uv-Vis spectrofotometer absorptiespectrum van de Au-CSCaCO3 NP's zoals besproken in de tekst
Gouden nanostructuren hebben een brede lichtabsorptie vanwege het gelokaliseerde oppervlakte-plasmonresonantie-effect van AuNP's [65, 66]. Een aantal rapporten heeft aangetoond dat gouddeeltjes vaak een scherpe absorptiepiek hebben die wordt waargenomen tussen 500-520 nm [66,67,68,69]. Deze techniek maakte verdere beoordeling van het geconjugeerde Au-CSCaCO3 . mogelijk NP's grootte, concentratie en aggregatieniveau [65]. Het is ook bekend dat de absorptieband verschuift naar de kleinere golflengten, wat wijst op de vermindering van de deeltjesgrootte, en de symmetrische vorm van de absorptiespectra geeft een smalle deeltjesgrootteverdeling aan [70], waarmee onze geconjugeerde Au-CSCaCO3 wordt bevestigd. sub> NP's die een bredere absorptiepiek vertoonden tussen 500-550 nm en het hoogste punt bij een golflengte van 530 nm. Aanvaardbaar in het nabij-infrarood zichtbare spectragebied, waar licht gemakkelijk wordt verzwakt door het weefsel en de absorptiepiek aanzienlijk verschuift naar een langere golflengte [71]. Een mogelijke verklaring hiervoor zou kunnen liggen in de synthese en conjugatie van het nanomateriaal. Ook consistent met Srinath et al., die onthulden dat de positie van de absorptieband voornamelijk afhangt van de kleurvariatie, aggregatie en oppervlakte-geadsorbeerde soorten [72]. Bovendien zou het absorptiespectrum van nanodeeltjes kunnen verschuiven afhankelijk van kleur, morfologie en grootte vanwege de gouden plasmonresonantie-eigenschap [73]. Nanostructuren met NIR-fotothermische eigenschappen hebben het vermogen om licht sterk te verstrooien, wat belangrijke toepassingen heeft in biomedische beeldvorming [74, 75].
Cytotoxiciteitsonderzoeken
MTT (3-dimethylthiazo-2, 5-diphynyltetrazoliumbromide)
Cytotoxiciteitsonderzoeken op menselijke borstcarcinoomcellen (MCF-7) en embryonale fibroblastcellen van muizen (NIH3T3) laten zien dat de Au-CSCaCO3 NP's remden meer dan 70% celproliferatie waardoor kankerceldood werd veroorzaakt en bijna 40% remming van de fibroblastcellen bij een dosering van 100 μg. De IC50 en lagere concentratiedoses zoals 25 μg bleken ook toxisch voor de kankercellen, wat een lage levensvatbaarheid van de cellen aan het licht bracht en ook de celproliferatie van de kankercellen voor de nanodeeltjes voor meer dan 50% remde. Aan de andere kant toonden identieke concentratiedoseringen aan de fibroblastcellen een verhoogde en consistente levensvatbaarheid van de fibroblastcellen. De IC50 vertoonde tot 80% cellevensvatbaarheid van de fibroblastcellen, zoals weergegeven in Fig. 6.
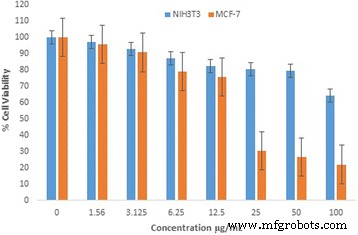
Cytotoxiciteitsbeoordeling van de met MCF-7 en NIH3T3 behandelde Au-CSCaCO3 NPs-cellen met behulp van MTT-assay geven percentage levensvatbaarheid van de cellen
3-Dimethylthiazo-2,5-diphynyltetrazolium Bromide (MTT) is een colorimetrische test die acceptabel wordt gebruikt om de levensvatbaarheid van cellen te bepalen [76]. Utilizing mitochondrial enzymes in the electron transport chain [77], viable cells with active metabolism converted MTT into purple-colored formazon crystals in the cellular cytosol [78]. The crystals were dissolved after cell lysis on adding an organic solvent dimethyl sulfoxide (DMSO) which is proportional to live cell number, unlike dead cells, due to cytotoxicity that are unable to carry out the reaction [79]. The conjugated nanoparticles displayed consistent cell death against the cancer cells and reliable cell viability of the fibroblast cells with concentration doses ranging from 25–100 μg. Furthermore, attesting low cytotoxicity and highlighting the biocompatibility of Au-CSCaCO3 NPs and potential usefulness for biomedical applications, the cytotoxicity could be due to the internalization of the nanoparticles which possibly triggered intracellular responses and thus induced cellular damage because of interaction with cell organelles. Despite contrary cytotoxicity findings with works done on HeLa cells (human cervical cancer cell line) due to nanoparticles inducing oxidative damage [35, 80], Zhang et al. demonstrated the biocompatibility of the nanoparticles and its likely use for drug delivery systems [80]. Similarly, reports of gold nanoparticles confirmed nontoxic dependent on their size [81] and concentration [39]. Studies strongly confirmed that biogenic gold conjugates are stable and nontoxic nanocarrier used in biomedical application [35, 39] suggesting use for biomedical applications such as drug delivery and cancer therapy [82].
Conclusies
Spherical-shaped conjugated gold-cockle shell-derived calcium carbonate nanoparticles (Au-CSCaCO3 NPs) were obtained. The conjugated nanoparticles were synthesized using a simpler, environmental friendly, and cost-efficient synthetic approach. Furthermore, based on the results, the obtained conjugated nanoparticles were relatively pure and stable. The source of material used for the cockle shell-derived nanoparticles is biogenic, readily available, and naturally occurring as seawater mollusca cockle shell. Based on the presented evidences, the conjugated Au-CSCaCO3 NPs could be a good biomaterial for biomedical applications.
Afkortingen
- Au-CSCaCO3 NPs :
-
Synthesized Conjugated Gold-Cockle Shell Derived Calcium Carbonate Nanoparticles
- AuNPs:
-
Gold nanoparticles
- BS-12:
-
Dodecyl dimethyl betaine
- C–C:
-
Carbon-carbon bond
- C–N:
-
Carbon-nitrogen bond
- C–O :
-
Carbon-oxygen bond
- DMEM:
-
Dulbecco’s modified Eagle’s medium
- DMSO:
-
Dimethyl sulfoxide
- EDX:
-
Energy dispersive X-ray
- FBS:
-
Fetal bovine serum
- FESEM:
-
Field emission scanning electron microscope
- FRGS:
-
Fundamental Research Grant Scheme
- FTIR:
-
Fourier transform infrared spectroscopy
- HeLa cells:
-
Human cervical cancer cell line
- IC50 :
-
50% inhibition concentration
- ICG:
-
Indocyanine green dye
- JCRB:
-
Japanese Collection Research Bioresource
- LSPR:
-
Localized surface plasmon resonance
- MCF-7:
-
Human breast adenocarcinoma cell line
- MTT:
-
3-Dimethylthiazo-2, 5-diphynyltetrazolium Bromide Dye
- NIH-3T3:
-
Mouse embryonic fibroblast cell line
- NIR:
-
Nabij infrarood
- O–H:
-
Oxygen-hydrogen bond
- OD:
-
Optical density
- PBS:
-
Phosphate-buffered saline
- TEM:
-
Transmissie-elektronenmicroscoop
Nanomaterialen
- Wat biedt de toekomst voor 3D-printen – biomedische toepassingen
- ALGEMENE TOEPASSINGEN VAN CALCIUMCARBONAAT
- Toepassingen van calciumcarbonaat masterbatch. Calciumcarbonaat voor het maken van filler masterbatch
- Multifunctionele gouden nanodeeltjes voor verbeterde diagnostische en therapeutische toepassingen:een overzicht
- Nanodeeltjes voor kankertherapie:huidige vooruitgang en uitdagingen
- Vooruitgang en uitdagingen van fluorescerende nanomaterialen voor synthese en biomedische toepassingen
- Grafeen- en polymeercomposieten voor toepassingen met supercondensatoren:een recensie
- Nieuwe biocompatibele Au Nanostars@PEG-nanodeeltjes voor in vivo CT-beeldvorming en eigenschappen voor nierklaring
- De voorbereiding van Au@TiO2 Yolk–Shell Nanostructure en zijn toepassingen voor afbraak en detectie van methyleenblauw
- Recente ontwikkelingen in synthetische methoden en toepassingen van zilveren nanostructuren
- Vervaardiging en karakterisering van ZnO-nanoclips door het door polyol gemedieerde proces



