Nanotechnologie:van in vivo beeldvormingssysteem tot gecontroleerde medicijnafgifte
Abstract
Wetenschap en technologie zijn altijd de vitale elementen geweest van de strijd van de mens, uitsluitend gebruikt voor de ontwikkeling van nieuwe instrumenten en producten, variërend van micro- tot nanoformaat. Nanotechnologie heeft veel aandacht gekregen vanwege de uitgebreide toepassingen in de biogeneeskunde, met name met betrekking tot biobeeldvorming en medicijnafgifte. Er zijn verschillende nanodevices en nanomaterialen ontwikkeld voor de diagnose en behandeling van verschillende ziekten. Hierin hebben we twee primaire aspecten van de nanogeneeskunde beschreven, d.w.z. in vivo beeldvorming en medicijnafgifte, met de nadruk op de recente vorderingen en toekomstige verkenningen. Enorme vooruitgang in de nanotechnologie-instrumenten voor de beeldvorming, met name van de kankercellen, zijn onlangs waargenomen. Nanodeeltjes bieden een geschikt medium om modificaties op moleculair niveau uit te voeren, inclusief de plaatsspecifieke beeldvorming en targeting. De uitvinding van radionucliden, kwantumdots, magnetische nanodeeltjes en koolstofnanobuizen en het gebruik van gouden nanodeeltjes in biosensoren hebben een revolutie teweeggebracht op het gebied van beeldvorming, wat heeft geleid tot een gemakkelijk begrip van de pathofysiologie van ziekten, een verbeterd vermogen om te diagnosticeren en een verbeterde therapeutische levering. Deze hoge specificiteit en selectiviteit van de nanogeneeskunde is belangrijk, en daarom moeten de recente ontwikkelingen op dit gebied worden begrepen voor een beter vandaag en een meer welvarende toekomst.
Recensie
Inleiding
In feite boekt nanotechnologie vooruitgang op alle gebieden van techniek en wetenschap, en wetenschappers brengen een revolutie teweeg in alle industrieën en mensenlevens door dingen te ontwerpen die op de kleinste schaallengte kunnen werken, atoom voor atoom [1]. Nanotechnologie omvat de studie van bij uitstek kleine structuren. Nanotechnologie kan uitgebreid worden gedefinieerd als de studie, creatie, ontwerp, synthese en implementatie van functionele materialen, systemen en apparaten door het beheersen van materie binnen het groottebereik van 1-100 nm op nanometerschaal. Bovendien is de manipulatie van innovatieve fenomenen en verbeterde eigenschappen van materie op deze nanometerschaal, ook wel moleculaire nanotechnologie genoemd, een magisch punt op schaallengte waar de kleinste kunstmatige apparaten de moleculen en atomen van het universum ontmoeten [2,3,4 ].
Het vroege begin van het concept van nanotechnologie en nanogeneeskunde kwam voort uit het kritische idee van Feynman dat kleine nanorobots en aanverwante apparaten konden worden ontwikkeld, gefabriceerd en in het menselijk lichaam konden worden geïntroduceerd om cellen op moleculair niveau te repareren. Hoewel later in de jaren tachtig en negentig, werd dit innovatieve concept bepleit in de beroemde geschriften van Drexler [5, 6] en in de jaren negentig en 2000 in de populaire geschriften van Freitas [7, 8]. Feynman kwam met het eerste bekende voorstel voor een nanomedische procedure om hartaandoeningen te genezen. In het algemeen zal miniaturisering van medische hulpmiddelen zorgen voor meer accurate, beheersbare, betrouwbare, veelzijdige, kosteneffectieve en snelle benaderingen voor een betere kwaliteit van het menselijk leven [9]. In 2000 werd voor de allereerste keer het National Nanotechnology Initiative gelanceerd; vanaf dat moment hebben modellering van elektronica en moleculaire structuren van nieuwe materialen, oprichting van fotonische en elektronische apparaten op nanoschaal [10, 11], ontwikkeling van 3D-netwerken, nanorobotica [12] en komst van multifrequentie-krachtmicroscopie [13] geplaveid de weg naar de opkomst van moleculaire nanotechnologie.
Nanodeeltjes worden beschouwd als de essentiële bouwstenen van nanotechnologie. Aanwezigheid van sterke chemische bindingen, uitgebreide delokalisatie van valentie-elektronen die variëren met de grootte, en structurele modificaties in nanodeeltjes leiden tot verschillende fysische en chemische eigenschappen, waaronder smeltpunten, optische eigenschappen, magnetische eigenschappen, soortelijke warmte en oppervlaktereactiviteit. Deze ultrafijne nanodeeltjes vertonen volledig nieuwe en verbeterde eigenschappen in vergelijking met hun bulk-tegenhanger vanwege variatie in specifieke kenmerken zoals grootte, verdeling en van de deeltjes die aanleiding geven tot een grotere oppervlakte-tot-volumeverhouding [14,15,16]. Naarmate het gebied van nanogestructureerde materialen is geëvolueerd, worden veel verschillende labels en terminologieën gebruikt, waaronder 3D-nanodeeltjes, nanokristallen, nanofilms, nanobuisjes, nanodraden en kwantumdots met een veelbelovend potentieel van oneindig aantal eigenschappen [17]. Vanwege de verscheidenheid aan potentiële toepassingen (inclusief industriële en militaire), hebben regeringen miljarden dollars geïnvesteerd in onderzoek naar nanotechnologie. De VS hebben 3,7 miljard dollar geïnvesteerd via hun National Nanotechnology Initiative, en de Europese Unie heeft ook 1,2 miljard gesubsidieerd, en 750 miljoen dollar is geïnvesteerd door Japan [18].
Tegenwoordig is nanotechnologie een van de meest innovatieve, vooruitstrevende gebieden van wetenschappelijk onderzoek, en het blijft zich met duizelingwekkende snelheden ontwikkelen [19]. Door vooruitgang in nanotechnologie kwamen veel geavanceerde technologieën beschikbaar voor de toediening van medicijnen. Onderzoekers hebben uitgebreid onderzoek gedaan naar het potentieel van nanodevices voor doelspecifieke en gecontroleerde afgifte van verschillende micro- en macromoleculen, waaronder medicijnen, eiwitten, monoklonale antilichamen en DNA (deoxyribonucleïnezuur) in veelsoortige biomedische toepassingen zoals kanker [20, 21], vaccinatie [22] , tandheelkundige [23], inflammatoire [24] en andere gezondheidsstoornissen. Daarom is het tegenwoordig een noodzaak om efficiënt gebruik van nanotechnologietoepassingen te demonstreren, variërend van in-vivo-beeldvormingssysteem tot gecontroleerde medicijnafgifte, om de huidige vooruitgang te markeren en aanwijzingen te krijgen voor naderend onderzoek op medisch gebied.
Farmaceutische nanosystemen
Farmaceutische nanotechnologie kan worden ingedeeld in twee hoofdcategorieën nanotools, namelijk nanomaterialen en nanodevices. Nanomaterialen kunnen verder worden gecategoriseerd op basis van drie basisparameters, waaronder structuur, dimensie en fasesamenstelling. Nanostructuren worden verder ingedeeld in polymere en niet-polymere structuren, waaronder nanodeeltjes, micellen, dendrimeren, geneesmiddelconjugaten, metalen nanodeeltjes en kwantumdots [25]. Op basis van hun afmetingen worden nanomaterialen ingedeeld in vier groepen, namelijk nul-, één-, twee- en drie nanodimensiematerialen. Naar fasesamenstelling kunnen deze nanomaterialen in drie groepen worden ingedeeld. Nanodevices zijn onderverdeeld in drie groepen, waaronder micro-elektromechanische systemen/nano-elektromechanische systemen (MEMS/NEMS), microarrays en ademhalingscellen. Deze structuren en apparaten kunnen worden gefabriceerd met een hoge mate van functionele eigenschappen voor gebruik in de geneeskunde om op moleculair niveau met cellen te interageren, waardoor een mate van integratie tussen biologische systemen en de nieuwste technologie mogelijk is die voorheen niet haalbaar was [26]. Gedetailleerde classificatie van farmaceutische nanotools wordt beschreven met hun voorbeelden in tabel 1.
Productiebenaderingen
Nanosizing-technologieën zijn van groot belang geworden voor de formulering van slecht in water oplosbare geneesmiddelen. Door de deeltjesgrootte te verkleinen tot nanoschaal, nemen de oplossnelheid en biologische beschikbaarheid toe vanwege de toename van het oppervlak, volgens de Noyes-Whitney-vergelijking [27]. Benaderingen die worden gebruikt voor de fabricagematerialen zijn onderverdeeld in bottom-up-technieken, top-down-technieken en de combinatie van bottom-up en top-down-technieken. Bij bottom-up technieken is sprake van een opbouw van moleculen. Enkele van de technieken die de bottom-upbenadering volgen voor de productie van materialen op nanoschaal, omvatten technieken in de vloeibare fase op basis van inverse micellen, chemische dampafzetting (CVD), sol-gelverwerking en moleculaire zelfassemblage. De componenten die door bottom-up worden geproduceerd, zijn aanzienlijk sterker dan de componenten op macroschaal vanwege de covalente krachten die ze bij elkaar houden. Bij top-down-technieken worden materialen gemicroniseerd door te snijden, te snijden en te vormen voor de vervaardiging van nanomaterialen. Voorbeelden zijn frezen, fysieke dampafzetting, hydrodermale techniek galvaniseren en nanolithografie [28]. Verschillende fabricagebenaderingen met hun respectievelijke typen worden beschreven in Tabel 2.
Biomedische toepassingen van geavanceerde nanotechnologie
Beeldvorming
In de afgelopen tien jaar zijn enorme vorderingen gemaakt, waarbij gebruik is gemaakt van de nanotechnologische hulpmiddelen voor beeldvorming en therapie in onderzoek dat met name gericht is op kankercellen. Nanodeeltjes, met een grootte van 10-100 nm, bieden een zeer geschikt medium om modificaties op moleculair niveau uit te voeren, zoals de plaatsspecifieke beeldvorming en targeting in kankercellen [29]. Het volgende gedeelte geeft een overzicht van recente ontwikkelingen in de beeldvormingstechnieken.
Radionuclide-beeldvorming
Omdat kleine moleculen niet kunnen worden bekeken met de niet-invasieve techniek, worden de plaatsgerichte contrastmiddelen gebruikt om een geselecteerde biomarker te identificeren die onmogelijk kan worden gescheiden van de normale omringende weefsels [30]. De radionuclidebeeldvorming is ontwikkeld met het concept dat het tot expressie gebrachte eiwit wordt onderzocht met een radiofarmaceutisch of isotoop-gelabeld middel of cel en verder in vivo wordt gevolgd [31]. De beeldvorming met positronemissietomografie (PET) wordt bij kankerpatiënten met succes gebruikt om de multidrugresistentie in beeld te brengen via P-glycoproteïnetransport met behulp van 99 m tetrofosmine en sestamibi als de radioactief gelabelde substraten voor het P-glycoproteïne [32, 33]. Het mechanisme van beeldvorming wordt bepaald door het type modaliteit dat voor de beeldvorming wordt gebruikt, zoals nanodragers waaronder liposomen [34], dendrimeren [35], Bucky balls [36] en talrijke polymeren en copolymeren [37]. Ze kunnen worden gevuld met het grote aantal beeldvormende deeltjes zoals optisch actieve verbindingen en radionucliden voor detectie met beeldvormingsapparatuur. De BODIPY (boriumdipyrromethane)-gelabelde jasplakinolide-analogen zijn gebruikt om de langlevende actinefilamenten in de levende cellen te visualiseren [38, 39].
De enorme groei van nanotechnologie leidt het onderzoek in de moleculaire beeldvorming met veel contrastmiddelen. Om een geschikte beeldvorming te verkrijgen, moet het geselecteerde contrastmiddel een langere halfwaardetijd, een laag achtergrondsignaal, specifieke epitoopbinding en verbeterd contrast met ruisverbetering hebben. Een groot aantal beschikbaarheid van dragers kan meer vooruitgang in beeldvorming definiëren, met bijzondere aandacht voor de moleculaire en cellulaire mechanismen van de ziekte; dit zal meer kansen creëren voor de rationele ontwikkeling van beeldvormings- en medicijnafgiftesystemen [30].
Kwantumpunten
Halfgeleider quantum dots worden nu gebruikt als een nieuwe klasse van fluorescerende labels. Deze halfgeleider nanokristallen zijn een veelbelovend hulpmiddel voor het visualiseren van de biologische cellen vanwege hun gemakkelijke oppervlaktechemie, waardoor biocompatibiliteit en daarmee conjugatie met verlenging van de fluorescentietijd mogelijk is [29, 40]. De visualisatie-eigenschappen van kwantumdots (fluorescentiegolflengte) zijn sterk afhankelijk van de grootte. De optische eigenschappen van kwantumdots zijn afhankelijk van hun structuur, aangezien ze zijn samengesteld uit een buitenste schil en een metalen kern. Grafeem-quantumdots (GQD), een soort groene fluorescente koolstofnanomaterialen, worden bijvoorbeeld gemaakt door grafeemoxide solvotherm te snijden en blijken de visualisatie-eigenschappen te domineren [41].
Quantum dot core bestaat meestal uit cadmiumselenide, cadmiumsulfide of cadmiumtelluride. De buitenste schil is op de kern gefabriceerd met een hoge bandafstand-energie om elektrische isolatie te bieden met behoud van fluorescentie-eigenschappen van kwantumdots. De nauwkeurig afgestemde kern en schillen met verschillende afmetingen en samenstellingen met visualisatie-eigenschappen van specifieke golflengten zorgen voor een groot aantal biomarkers [40]. Quantum dots worden geconjugeerd met verschillende liganden om specifieke binding aan biologische receptoren te verkrijgen. De tumorgerichte liganden zijn gekoppeld aan amfifiele polymere kwantumdots en worden gebruikt om de beeldvormingsstudies van prostaatkanker bij muizen uit te voeren [42]. Evenzo bieden kwantumdots aanzienlijke voordelen ten opzichte van de conventionele kleurstoffen, zoals emissie met smalle bandbreedte, hogere fotostabiliteit en uitgebreid absorptiespectrum voor de enkele excitatiebron. Bovendien is de uitdaging van hydrofobiciteit in kwantumstippen overwonnen door ze in water oplosbaar te maken. Een voorbeeld van de waterige kwantumdots met lange retentietijd in biologische vloeistoffen is de ontwikkeling van sterk fluorescerende metaalsulfide (MS) kwantumdots vervaardigd met thiolbevattende geladen groepen [43]. Bovendien maakten de unieke fluorescentie-eigenschappen van kwantumdots ze tot geschikte beeldvormende hulpmiddelen voor de kankercellen [42]. Quantum dots gekoppeld aan A10 RNA-aptameer geconjugeerd met doxorubicine (QD-Apt-Dox) is het voorbeeld van gerichte beeldvorming van kankercellen [44]. Er is echter verhoogde toxiciteit van kwantumdots waargenomen als gevolg van de opname van zware metalen, wat resulteert in hun beperkte gebruik voor de in vivo beeldvorming. Desalniettemin richten recente benaderingen zich op de vermindering van toxiciteit en de verbetering van de biocompatibiliteit van kwantumstippen met de lichaamscellen. Het is ook de moeite waard om te vermelden dat kwantumdots met een diameter van minder dan 5,5 nm snel en efficiënt uit de urine worden uitgescheiden, wat resulteert in verminderde toxiciteit. Dit fenomeen werd aangetoond door de synthese van cadmiumvrij, CulnS2 /ZnS (koper-indiumsulfide/zinksulfide) als de kern en schil van de kwantumdots, wat resulteerde in verbeterde stabiliteit in de levende cellen voor beeldvorming van lymfeklieren met een duidelijke vermindering van acute lokale toxiciteit [45, 46].
Biosensoren
Een van de grootste successen op het gebied van nanomaterialen sinds de afgelopen jaren is de ontwikkeling van biosensoren. Biosensoren zijn de apparaten die het biologische sensorelement bevatten dat is aangesloten of geïntegreerd in de transducer. Biosensor vertoont hun werking door herkenning van specifieke moleculen in het lichaam op basis van hun structuur, waaronder antilichaamantigeen, enzymsubstraat en receptorhormoon. De twee belangrijkste eigenschappen van biosensoren, inclusief hun specificiteit en selectiviteit, zijn afhankelijk van dit herkenningssysteem. Deze basiseigenschappen van de biosensoren worden vooral gebruikt voor de concentratie die evenredig is met de signalen [47,48,49].
Om de biosensor met hoge efficiëntie te produceren, is het substraat dat is geselecteerd voor de dispersie van het sensormateriaal een vereiste. Verschillende soorten nanomateriaal, waaronder kwantumdots [50], magnetische nanodeeltjes [51], koolstofnanobuizen (CNT's) [52] en gouden nanodeeltjes (BNP's) [53] worden op de biosensoren toegepast. De onderscheidende chemische, fysische, magnetische, optische en mechanische eigenschappen van nanomateriaal leiden tot hun verhoogde specificiteit en gevoeligheid voor detectie. Biosensoren die BNP's bevatten, hebben een compatibele omgeving geboden voor de biomoleculen die de concentratie van geïmmobiliseerde biomoleculen op het oppervlak van de elektrode hebben verhoogd. Het heeft geresulteerd in een verhoogde gevoeligheid van de biosensoren [54, 55]. De meest gebruikte elektrode-oppervlakken in de biosensoren zijn de glasachtige koolstofelektrode (GCE), die zijn gemodificeerd van BNP's. Bovendien hebben ze de beste gevoeligheid en elektrochemische stabiliteit laten zien. In dit opzicht kunnen methyleenblauw (MB) en BNP's gemakkelijk worden geassembleerd en gewijzigd door middel van laag voor laag (LBL) techniek in de vorm van films op GCE, om de concentratie van humaan choriongonadotrofine (HCG) te detecteren [56]. Vanwege het grote oppervlak van de nanodeeltjes om anti-HCG te laden, kunnen deze immunosensoren worden gebruikt voor het detecteren van de HCG-concentraties in het menselijk bloed of urinemonsters. Evenzo hebben CNT's geweldige toepassingen gevonden in biomedische technologie, bio-analyse, bio-sensing en nano-elektronica [57,58,59]. Bovendien hebben meerwandige koolstofnanobuizen (MWNT) in de vorm van bio-nanocomposietlagen van polymeren het potentieel om te worden gebruikt voor de DNA-detectie [60]. Bovendien hebben magnetische nanodeeltjes ook brede toepassingen gevonden vanwege hun magnetische eigenschappen, waaronder contrastmiddel voor magnetische resonantiebeeldvorming (MRI) [61], hyperthermie [62], immunoassay [63], weefselherstel [64], celscheiding [65], GMR-sensor [66], en medicijn- of genafgifte [67].
Evenzo is er ook een nieuw type magnetische chitosan-microsferen (MCMS) geproduceerd door eenvoudigweg chitosan en met koolstof beklede magnetische nanodeeltjes te gebruiken [68]. In deze studie werd hemoglobine ook met succes geïmmobiliseerd op het MCMS-gemodificeerde GCE-oppervlak door glutaaraldehyde als verknopingsmiddel te gebruiken. Een andere belangrijke toepassing van biosensoren is in de optische technologie, die de detectie van verschillende soorten DNA-oligonucleotiden omvat met behulp van SsDNA-CNT-sondes als biosensoren [69]. Evenzo hebben op liposomen gebaseerde biosensoren ook veel aandacht gekregen, omdat ze zijn gebruikt bij het bewaken van de organofosforpesticiden, waaronder paraoxon en dichloorvos op de minimumniveaus [70].
Magnetische nanodeeltjes
Magnetische nanodeeltjes (MNP's) bieden exclusieve magnetische eigenschappen omdat ze het vermogen hebben om op moleculair of cellulair niveau van de biologische interacties te werken, waardoor ze de beste verbindingen zijn als contrastmiddelen in MRI en als dragers bij medicijnafgifte. De recente ontwikkelingen in nanotechnologie hebben aandacht gekregen omdat het heeft geholpen bij de wijziging van de eigenschappen en kenmerken van MNP's voor biomedische toepassingen. In dit opzicht is aangetoond dat de levertumor en metastasebeeldvorming via RES-gemedieerde opname van superparamagnetische ijzeroxiden (SPIO's) in staat zijn om de laesies te differentiëren die zo klein zijn als slechts 2-3 mm [70, 71]. Bovendien zijn deze ultrakleine supermagnetische ijzeroxiden (USPIO's) ook zeer effectief in de beeldvorming van de metastase van de lymfeklieren met een diameter van slechts 5 tot 10 mm [72]. Bovendien is het belang van deze niet-invasieve benadering ook aangetoond bij de detectie van lymfatische verspreiding, aangezien het wordt beschouwd als een belangrijk onderdeel in de stadiëring en bij het identificeren van de behandelingsbenaderingen voor de borst, colon- en prostaatkanker [73].
Druglevering
Nanotechnologie is vanwege hun verschillende fysieke, optische en elektronische eigenschappen een aantrekkelijk instrument voor disciplines variërend van materiaalkunde tot biogeneeskunde. De meest effectieve onderzoeksgebieden van nanotechnologie zijn nanogeneeskunde die nanotechnologieprincipes toepast voor de behandeling, preventie en diagnose van ziekten. Bovendien zijn er veel producten van nanogeneeskunde op de markt gebracht als gevolg van de toename van het onderzoek naar nanogeneeskunde in de afgelopen decennia, over de hele wereld. Momenteel wordt nanogeneeskunde beïnvloed door medicijnafgiftesystemen, goed voor meer dan 75% van de totale verkoop [74]. In dit opzicht hebben op nanodeeltjes gebaseerde medicijnafgifteplatforms het vertrouwen van wetenschappers gekregen omdat ze de meest geschikte vehikels zijn bij het aanpakken van de farmacokinetische nadelen die gepaard gaan met conventionele medicijnformuleringen [75]. Daarom zijn er verschillende nanovormen geprobeerd als medicijnafgiftesystemen zoals liposomen, vaste lipidenanodeeltjes, dendrimeren en vaste metaalbevattende NP's, om de therapeutische werkzaamheid van geneesmiddelen te verbeteren [76, 77]. Enkele van de belangrijkste interessegebieden worden hieronder besproken.
Oogologie
Het toedienen van medicijnen via de oogheelkundige route is zeer aantrekkelijk maar uitdagend voor de farmaceutische wetenschappers. Het oog is een klein ingewikkeld orgaan met meerdere compartimenten. Zijn biochemie, fysiologie en anatomie hebben het zeer ondoordringbaar gemaakt voor het xenobioticum. Veel voorkomende aandoeningen die oculaire toediening vereisen, bevatten de ooginfecties zoals conjunctivitis samen met de cornea-aandoeningen zoals glaucoom. De meest voorkomende geneesmiddelklassen die bij de oculaire toediening worden gebruikt, omvatten mydriatica of cycloplegische miotica, anti-infectieuze, anti-inflammatoire, diagnostische en chirurgische adjuvantia. Voor de kleine oogafwijking is ook gentherapie nodig, en op dit gebied wordt veel werk verzet. Door nanodragers ondersteunde benaderingen hebben de aandacht van de wetenschappers getrokken vanwege hun geschiktheid en specificiteit. Er is gemeld dat deeltjesafgiftesystemen zoals microsferen en nanodeeltjes en vesiculaire dragers zoals liposomen, niosomen, farmacosomen en discomen de farmacokinetische en farmacodynamische eigenschappen van verschillende soorten geneesmiddelmoleculen verbeterden [76]. Er zijn veel nieuwe gecontroleerde medicijnafgiftesystemen ontstaan, waaronder hydrogels, muco-adhesieve polymeren, micro-emulsies, dendrimeren, iontoforetische medicijnafgifte, op siRNA gebaseerde benaderingen, stamceltechnologie, niet-virale gentherapie en lasertherapie met de sclera-pluggen [78] . Verschillende systemen voor medicijnafgifte zijn gekostumeerd voor de toediening van medicijn via de oculaire route. Het belangrijkste doel van alle medicijnafgiftesystemen is het verbeteren van de verblijfsperiode, het verbeteren van de permeabiliteit van het hoornvlies en het vrijmaken van het medicijn in de achterste oogkamer, wat leidt tot een verhoogde biologische beschikbaarheid en een betere therapietrouw van de patiënt [79].
Abrego et al. bereide PLGA (polymelkzuur co-glycolzuur) nanodeeltjes van pranoprofen voor oogheelkundige toediening in de vorm van hydrogel. Deze hydrogelformulering heeft geschikte reologische en fysisch-chemische eigenschappen voor de oculaire afgifte van pranoprofen met verbeterde biofarmaceutische omtrek van het geneesmiddel. Bovendien versterkte het de lokale ontstekingsremmende en pijnstillende resultaten van het medicijn, wat resulteerde in een verbeterde therapietrouw van de patiënt [80]. In een ander onderzoek werden met cefuroxim beladen nanodeeltjes van chitosan ontwikkeld met behulp van een dubbele verknoping in dubbele emulsietechniek. De gevolgtrekking wijst op chitosan-gelatinedeeltjes als krachtige praktische kandidaten voor DD op intraoculair niveau [81]. Bovendien werden met diclofenac geladen N-trimethylchitosan-nanodeeltjes (DC-TMCN's) ontwikkeld voor oogheelkundig gebruik om de oculaire biologische beschikbaarheid van het geneesmiddel te verbeteren [82]. Bovendien zijn supramoleculaire assemblages van op chitosan gebaseerd dexamethasonfosfaat ontwikkeld voor verbeterde pre-corneale verblijftijd van geneesmiddelen vanwege de muco-adhesieve eigenschappen ervan. Deze nanodeeltjes hebben een sterke wisselwerking met zowel het oogoppervlak als het medicijn en beschermen het medicijn tegen metabolische afbraak, wat leidt tot verlengde pre-corneale residentie [83]. Glaucoom, een oogziekte, werd behandeld met op brimonidine gebaseerde beladen vaste lipidenanodeeltjes met aanhoudende afgifte met behulp van glycerylmonostearaat als vast lipide [84, 85]. Evenzo werden met daptomycine beladen chitosan-gecoate alginaat (CS-ALG) nanodeeltjes ontwikkeld met een geschikte grootte voor oculaire toepassingen en een hoge inkapselingsefficiëntie (tot 92%). Deze studie onthulde dat het daptomycine-nanodragersysteem in de toekomst zou kunnen worden gebruikt om dit antibioticum rechtstreeks in het oog af te geven, om te dienen als een prospectieve therapie tegen bacteriële endoftalmitis en als een efficiënt alternatief voor chitosan-nanodeeltjes [86].
Een van de belangrijkste oorzaken van het falen van transplantaten op korte en lange termijn bij hoornvliestransplantatie is de immunologische afstoting van het transplantaat. Voor dit doel werd een op PLGA gebaseerd biologisch afbreekbaar nanodeeltjessysteem van dexamethason-natriumfosfaat (DSP) voorbereid, resulterend in de aanhoudende afgifte van de corticosteroïden om de afstoting van het hoornvliestransplantaat te voorkomen [87]. Bovendien werden MePEG-PCL (polyethyleenglycol-polycaprolacton) nanodeeltjes van curcumine gerapporteerd, en ze vertoonden verhoogde efficiëntie, verbeterde retentie van curcumine in het hoornvlies en significante verbetering in de preventie van de cornea-neovascularisatie ten opzichte van vrij curcumine [88]. Evenzo werden met zilver nanodeeltjes doordrenkte weefselkleefstof (2-octyl cyanoacrylaat) ontwikkeld met verbeterde mechanische sterkte en antibacteriële werkzaamheid. Deze gedoteerde kleefstof (zilveren nanodeeltjes) ondersteunden het gebruik van weefselkleefstoffen als een levensvatbaar supplement of alternatief voor hechtingen [89].
Pulmonologie
Longziekten waarschijnlijk astma, chronische obstructieve longziekte (COPD) en longkanker komen vaak voor en zijn vaak levensbedreigend. Er wordt bijvoorbeeld beschreven dat COPD de vierde belangrijkste doodsoorzaak is en dat longcarcinoom de meest voorkomende doodsoorzaak door kanker wereldwijd is. Nanodeeltjes worden onder de loep genomen als een keuze om de therapie van deze ernstige ziekten te verbeteren [90]. Verschillende met medicijnen beladen nanodeeltjes zijn gebruikt voor hun lokale en systemische effecten bij de behandeling van longziekten. Toediening van curatieve middelen aan de plaats van actie voor longziekten kan een effectieve behandeling van chronische longinfecties, longkankers, tuberculose en andere ademhalingspathologieën mogelijk maken [91]. De nanodragers die voor dit doel worden gebruikt, omvatten liposomen, op lipiden of polymeren gebaseerde micellen, dendrimeren en polymere NP's [92]. Polymere NP's zijn van prenominaal belang, omdat de polymeren kunnen worden gecopolymeriseerd, aan het oppervlak gemodificeerd of bio-geconjugeerd voor het verbeteren van de targetingcapaciteit en distributie van de ingekapselde middelen. De algemeen gebruikte nanodragers bij de toediening van geneesmiddelen aan de longen bevatten natuurlijke polymeren zoals gelatine, chitosan en alginaat en synthetische polymeren zoals poloxameer, PLGA en PEG [93].
Er werd waargenomen dat PLGA-NP's de meest geschikte reeks kenmerken vertonen als dragers voor pulmonale eiwit / DNA-afgifte, terwijl gelatine-NP's een aangename wederzijdse keuze zijn [94]. Evenzo werden anisotrope of Janus-deeltjes van doxorubicine en curcumine geformuleerd om de geneesmiddelen tegen kanker voor de behandeling van longkanker via inademing te laden. De deeltjes werden geformuleerd met behulp van de biocompatibele en biologisch afbreekbare materialen binaire mengsels. Deze deeltjes vertoonden geen geno- en cytotoxische gevolgen. De kankercellen internaliseren deze Janus-deeltjes en stapelen ze op in de kern en het cytoplasma, wat leidt tot langdurige retentie. Bovendien werden polyamidoamine (PAMAM) dendrimeren geëvalueerd als nanodragers voor pulmonale afgifte van het model zwak oplosbare anti-astma farmaceutische beclometasondipropionaat (BDP) met behulp van G3, G4 en G4 [12] dendrimeren. Deze studie toonde aan dat BDP-dendrimeren potentieel hebben voor longinhalatie met behulp van luchtstraal- en vibrerende gaasvernevelaars. Verder werd waargenomen dat de aërosolkenmerken werden beïnvloed door het ontwerp van de vernevelaar in plaats van de vorming van dendrimeren [95]. Bovendien werden gemanipuleerde nanodeeltjes (ENP), bestaande uit anorganische metalen, metaaloxiden, metalloïden, organische biologisch afbreekbare en anorganische biocompatibele polymeren efficiënt gebruikt als dragers voor de afgifte van vaccins en geneesmiddelen en voor de behandeling van een verscheidenheid aan longziekten. Eigenschappen en effectieve effecten van ENP's op de longen zijn weergegeven in Fig. 1. Anorganisch ENP (zilver, goud en koolstof ENP), metaaloxiden ENP (ijzeroxide, zinkoxiden en titaniumdioxide) en organisch ENP (op lipiden gebaseerd, op basis van polysacchariden, op basis van polymeermatrix) werden ontwikkeld en geëvalueerd op pulmonale immuunhemostase. Behalve dat het relatief veilige dragers zijn, wezen moderne studies uit dat ENP-kabel gunstige resultaten oplevert met ontstekingsremmende eigenschappen (bijv. Zilver en polystyreen) en afdruk van de long die het behoud van immuunhomeostase (bijv. polystyreen) vertoont. Verdere kennis van de mechanismen kan helpen om de nuttige effecten van ENP op pulmonale immuunhomeostase en/of behandeling van inflammatoire longziekte [96] beter te begrijpen.
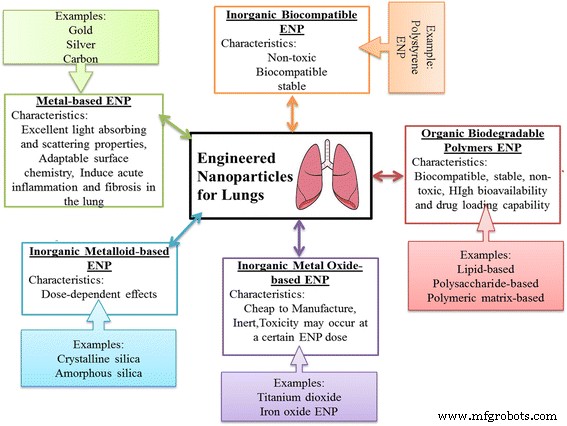
Eigenschappen en effectieve effecten van ENP's op de longen
Het is belangrijk om te vermelden dat gefunctionaliseerd kationisch lipo-polyamine (Star:Star-mPEG-550) recentelijk is ontwikkeld voor de siRNA (korte interferentie-RNA) in vivo afgifte aan de pulmonale vasculaire cellen. Deze uitgebalanceerde lipideformulering intensiveert de siRNA-retentie in de longen van de muis en zorgde voor een significante demontage van het doelgen. De resultaten werden nuttig bevonden en met verminderde toxiciteit van de levering van miRNA-145-remmer aan de longen door gebruik te maken van de gefunctionaliseerde kationische lipopolyamine-nanodeeltjes om de pulmonale arteriopathie te rekruteren en de functie van het hart te corrigeren bij ratten met intense pulmonale arteriële hypertensie (PAH) [97].
Cardiovasculair systeem
Hart- en vaatziekten is de aandoening die het cardiovasculaire systeem, vaatziekten van de hersenen en de nieren en perifere arteriële aandoeningen aantast. Ondanks alle vooruitgang in farmacologische en klinische behandeling, is hartfalen wereldwijd de belangrijkste oorzaak van morbiditeit. Veel nieuwe therapeutische strategieën, waaronder celtransplantatie, genafgifte of therapie, en cytokinen of andere kleine moleculen, zijn onderzocht om hartfalen te behandelen [98]. In ontwikkelingslanden worden onvoldoende mensen getroffen; meer dan 80% van de sterfgevallen als gevolg van cardiovasculaire aandoeningen vinden plaats in onderontwikkelde landen en komen bijna gelijkmatig voor bij mannen en vrouwen [99]. Mathers et al. in 2008 zijn er naar schatting 9,4 miljoen doden per jaar [100]. Dit concludeert 45% van de sterfgevallen veroorzaakt door coronaire hartziekten en 51% van de sterfgevallen door hartinfarcten [101]. Er zijn veel verschillende soorten dragers voor medicijnafgifte, zoals polymere micellen, liposomen, dendrimeren, door lipoproteïne ondersteunde farmaceutische dragers en dragers van nanodeeltjes.
Op chitosan gebaseerde liposomen van sirolimus met een invangefficiëntie van ≥83% werden ontwikkeld voor de behandeling van restenose en het is bewezen dat ze een nieuw platform zijn voor efficiënte gerichte toediening [102]. Evenzo hebben met galzout verrijkte niosomen van carvedilol met 85% invangefficiëntie geresulteerd in een verbeterde biologische beschikbaarheid van het geneesmiddel, en dus werd een beter therapeutisch effect [103] verkregen. Remming van restenose in door een ballon beschadigde halsslagader wordt bereikt bij ratten door de ontwikkeling van op PLGA gebaseerde nanodeeltjes die AGL 2043 en AG1295 inkapselen, selectieve blokkers van van bloedplaatjes afgeleide groeifactoren (PDGF) receptoren [104]. Angiogenic therapy of myocardial ischemia with vascular endothelial growth factor (VEGF) is a favorable approach to overcome hypoxia and its sequel effects. Polymeric particles loaded with VEGF have been proved a promising system for delivery of cytokines to rat myocardial ischemic model. This approach could be further explored for clinical studies [105]. Coenzyme Q10 (CoQ10) owing to its role in mitochondrial electron transport chain appears to be a reliable candidate to treat myocardial ischemia (MI) but its poor biopharmaceutical characteristics needed to be addressed by developing promising delivery approaches. Polymeric nanoparticles were developed to encapsulate CoQ10 to overcome its poor pharmaceutical properties and administered to MI-induced rats. Cardiac function was analyzed by determining ejection fraction before and after 3 months of therapy. Results showed significant betterment in the ejection fraction after 3 months [106].
Oncology
Cancer is a prime cause of mortality around the globe. The World Health Organization determines that 84 million people die of cancer between 2005 and 2015. The eventual target of cancer therapeutics is to increase the life span and the quality of life of the patient by minimizing the systemic toxicity of chemotherapy [107]. Chemotherapeutic agents have widely been studied in oncology for the past 25 years, but their tumor specificity is unsatisfactory and therefore exhibit dose-dependent toxicity. To overcome this limitation, recent interest has been centered on developing nanoscale delivery carriers that can be targeted directly to the cancer cell, deliver the drug at a controlled rate, and optimize the therapeutic efficacy [108, 109]. Passive and active targeting is used to deliver the drug at its tumor site. The passive phenomenon called the “enhanced permeability and retention (EPR) effect,” discovered by Matsumura and Maeda, is the dominated pathway used for chemotherapeutics [110, 111]. Active targeting is achieved by grafting ligand at the surface of nanocarriers that bind to receptors or stimuli-based carriers, e.g., dual reverse thermosensitive [112], photo-responsive [113], magnetic nanoparticles [114], and enzymatically activated pro-drugs [115]. Nanoparticles (NPs) can be conjugated with various smart therapeutic carriers like polymeric nanoparticles [116], micelles [117], liposomes [118], solid lipid nanoparticles (SLNs) [119], protein nanoparticles [120], viral nanoparticles [121], metallic nanoparticles [122], aptamers [123], dendrimers [124], and monoclonal antibody [125] to improve their efficacy and decrease the systemic toxicity. Table 3 summarizes the different approaches for drug deliveries which are widely studied to target the tumor with maximize therapeutic response and minimum toxicity.
Biodegradable poly (o-caprolactone) nanocarriers loaded with tamoxifen were developed for the management of estrogen receptor-specific breast cancer [126]. This study suggested that the nanoparticle preparations of selective estrogen receptor modulators deliver the drug in the specific estrogen receptor zone resulting in enhanced therapeutic efficacy. Similarly, a nanoconjugation of doxorubicin and cisplatin was developed by Chohen et al. [127], which have exhibited enhanced efficiency and reduced side effects of the loaded drugs in the treatment of localized progressive breast cancer. Likewise, chemotherapeutic drug oxaliplatin-loaded nanoparticulate micelles were prepared by Cabral et al. [128], with sustained release of loaded drug in the tumor microenvironment, resulted in enhanced antitumor effect [128]. Furthermore, SLN loaded-5-FU resulted in enhanced bioavailability and sustained release of the encapsulated anticancer drug, leading to enhanced antitumor effect [129].
Conclusions
Nanotechnology is subjected to inordinate progress in various fronts especially to make innovations in healthcare. Target-selective drug delivery and approaches for molecular imaging are the areas of prime importance for research where nanotechnology is playing a progressive role. This review provides readers with a wide vision on novel ongoing potentialities of various nanotechnology-based approaches for imaging and delivery of therapeutics. In order to obtain effective drug delivery, nanotechnology-based imaging has enabled us to apprehend the interactions of nanomaterials with biological environment, targeting receptors, molecular mechanisms involved in pathophysiology of diseases, and has made the real time monitoring of therapeutic response possible. Development of analytical technologies to measure the size of particles in nanometer ranges, and advent of latest manufacturing approaches for nanomaterials, has resulted in establishment of more effective methods for delivery of therapeutics for the treatment of ophthalmological, pulmonary, cardiovascular diseases, and more importantly cancer therapy. These new drug therapies have already been shown to cause fewer side effects and be more effective than traditional therapies. Furthermore, the imaging techniques have enhanced the determination of tumor location in human bodies and their selective targeting. Altogether, this comparatively new and thriving data suggest that additional clinical and toxicity studies are required further on the “proof-of-concept” phase. Nanomedicine cost and manufacturing at larger scale is also a matter of concern that needs to be addressed. Notwithstanding, future of nanomedicines is propitious.
Afkortingen
- AIE:
-
Aggregation-induced emission
- BDP:
-
Beclometasone dipropionate
- BODIPY:
-
Boron dipyrromethane
- CNTs:
-
Carbon nanotubes
- COPD:
-
Chronic obstructive pulmonary disease
- CulnS2 /ZnS:
-
Copper indium sulfide/zinc sulfide quantum dots
- CVD:
-
Chemische dampafzetting
- DNA:
-
Deoxyribonucleic acid
- ENPs:
-
Engineered nanoparticles
- EPR:
-
Enhanced permeability and retention
- GCE:
-
Glazige koolstofelektrode
- GNPs:
-
Gouden nanodeeltjes
- GQD:
-
Grapheme quantum dots
- HCG:
-
Human chorionic gonadotrophin
- MEMS:
-
Microelectromechanical systems
- MI:
-
Myocardial ischemia
- MNPs:
-
Magnetic nanoparticles
- MSNs:
-
Mesoporous silica nanoparticles
- MWNT:
-
Multi-walled carbon nanotubes
- NEMS:
-
Nanoelectromechanical system
- PAH:
-
Pulmonary arterial hypertension
- PCL:
-
Poly caprolactone
- PDGF:
-
Platelet-derived growth factors
- PEG:
-
Poly ethylene glycol
- PET:
-
Positron emission tomography
- PLGA:
-
Poly lactic-co-glycolic acid
- ROS:
-
Reactive oxygen species
- SiRNA:
-
Short interference RNA
- SLNS:
-
Solid lipid nanoparticles
- SPIOs:
-
Superparamagnetic iron oxides
- VEGF:
-
Vascular endothelial growth factor
Nanomaterialen
- Raspberry Pi-gestuurde aquaponics
- Nanovezels en filamenten voor verbeterde medicijnafgifte
- Biocompatibele FePO4-nanodeeltjes:medicijnafgifte, RNA-stabilisatie en functionele activiteit
- Omgevingsgevoelige metaal-organische raamwerken als medicijnafgiftesysteem voor tumortherapie
- Op cellen gebaseerde medicijnafgifte voor kankertoepassingen
- Zebravis:een veelbelovend real-time modelsysteem voor door nanotechnologie gemedieerde neurospecifieke medicijnafgifte
- 131I-getraceerde PLGA-lipide nanodeeltjes als dragers van medicijnafgifte voor de gerichte chemotherapiebehandeling van melanoom
- Nieuwe biocompatibele Au Nanostars@PEG-nanodeeltjes voor in vivo CT-beeldvorming en eigenschappen voor nierklaring
- Onderzoek naar fysisch-chemische kenmerken van een op nanoliposoom gebaseerd systeem voor dubbele toediening van geneesmiddelen
- Onderkoeling van water gecontroleerd door nanodeeltjes en ultrageluid
- Compact 3D LiDAR-beeldvormingssysteem



