Effecten van micro-omgevings-pH van liposoom op chemische stabiliteit van geladen geneesmiddel
Abstract
Liposoom is een veelbelovend dragersysteem voor het afleveren van bioactieve moleculen. De succesvolle levering van pH-gevoelige moleculen wordt echter nog steeds beperkt door de intrinsieke instabiliteit van nuttige ladingen in een fysiologische omgeving. Hierin hebben we een speciaal liposoomsysteem ontwikkeld dat een zure micro-omgeving in de interne waterige kamer bezit om de chemische stabiliteit van pH-gevoelige ladingen te verbeteren. Met curcumine beladen liposomen (Cur-LP's) met gevarieerde interne pH-waarden (pH 2,5, 5,0 of 7,4) werden bereid. Deze Cur-LP's hebben een vergelijkbare deeltjesgrootte van 300 nm, vergelijkbare fysieke stabiliteiten en analoge in vitro afgifteprofielen. Interessant is dat de chemische stabiliteit van liposomaal curcumine in 50% foetaal runderserum en de werkzaamheid tegen kanker in vitro beide micro-omgeving pH-afhankelijk zijn (Cur-LP-2.5> Cur-LP-5.0> Cur-LP-7.4). Deze serumstabiliteit heeft nog ruimte om verder te worden verbeterd om de toepasbaarheid van Cur-LP te verbeteren. Kortom, het creëren van een zure micro-omgeving in de interne kamer van liposoom is haalbaar en efficiënt om de chemische stabiliteit van pH-gevoelige nuttige ladingen te verbeteren.
Achtergrond
Liposoom, een kunstmatig membraanvehikel, heeft een groot potentieel voor medicijnafgifte laten zien vanwege zijn medicijnlaadcapaciteit, biologische afbreekbaarheid en biocompatibiliteit [1,2,3,4]. Het klassieke liposoom is vergelijkbaar met levende cellen in structuur, meestal bestaande uit een fosfolipide dubbellaag en een waterige binnenkamer [5,6,7]. Vanwege deze structuur is liposoom in staat om de onoplosbare medicijnmoleculen op te lossen en te voorkomen dat het geladen medicijn uit de ruwe fysiologische omgeving [8,9,10]. Bovendien kan het oppervlak van liposoom worden aangepast om de bloedcirculatietijd te verlengen en/of specifieke weefsels aan te pakken [11,12,13,14,15]. Met deze bovengenoemde voordelen zijn verschillende liposoomsystemen klinisch goedgekeurd [8, 9, 16].
Hoewel de afgifte van veel geneesmiddelen is verbeterd door opname in liposoom, wordt de afgifte van sommige pH-gevoelige geneesmiddelen nog steeds beperkt door de instabiliteit van het geneesmiddelmolecuul zelf in een fysiologische omgeving (neutrale pH-waarden). In het algemeen wordt liposoom bereid in een neutrale bufferoplossing en dus bevinden de geladen geneesmiddelmoleculen zich ook in een neutrale omgeving na opname in liposoom. Dienovereenkomstig zouden die moleculen die alleen stabiel zijn in een zure omgeving nog steeds instabiel zijn, zelfs in de vorm van liposoom. Daarom is de ontwikkeling van een nieuwe benadering voor het verbeteren van de stabiliteit van pH-gevoelige geneesmiddelen van groot belang voor een succesvolle levering van deze nuttige lading door liposoom.
Zoals hierboven vermeld, heeft liposoom een waterige ruimte in zijn binnenste kamer, die kan worden gebruikt om de nuttige lading van geneesmiddelen te voorzien van een zure micro-omgeving (Fig. 1). In dit huidige werk gebruiken we curcumine als een modelgeneesmiddel en streven we naar een nieuwe benadering voor het verbeteren van de chemische stabiliteit van medicijnmoleculen die in liposoom zijn geladen. Het is algemeen bekend dat curcumine een lipofiel molecuul is en vanwege de verschillende biologische activiteiten ervan op grote schaal wordt gebruikt in voedsel, medicijnen en cosmetica [17,18,19,20,21]. De afgifte ervan wordt echter sterk beperkt door zijn onoplosbaarheid en instabiliteit in biologische vloeistoffen [22,23,24,25]. Tot nu toe moet het zijn klinische belofte nog waarmaken, deels vanwege pH-gemedieerde instabiliteit [26]. Daarom is curcumine een geschikt modelgeneesmiddel voor dit werk.
Schema's van het liposoom met gevarieerde micro-omgevingszuurgraad in de binnenste waterige kamer
Methoden
Materialen
Fosfolipiden (sojalecithine voor injectiegebruik) werden gekocht bij Shanghai Tai-Wei Pharmaceutical Co., Ltd., (Shanghai, China). Cholesterol werd verkregen van Amresco (Solon, OH, VS). Poloxamer 188 (F68) werd vriendelijk geschonken door BASF (China) Co., Ltd., (Shanghai, China). Curcumine werd geleverd door Sigma (St. Louis, MO, VS). Foetaal runderserum (FBS) werd gekocht bij HyClone (Logan, UT, VS). Alle andere chemische reagentia die in dit onderzoek werden gebruikt, waren van analytische kwaliteit of beter.
Bereiding van met curcumine geladen liposomen (Cur-LP's)
De liposomen met gevarieerde micro-omgevings-pH-waarden werden bereid met behulp van de verdampingsmethode volgens eerdere werken met enkele aanpassingen [27, 28]. In het kort werden fosfolipiden (75 mg) en cholesterol (5 mg) opgelost in 0,5 ml ethanol met daarin 2 mg/ml curcumine. De ethanoloplossing werd gemengd met 5 ml 0,001 M PBS met 1% (w /v ) F68 dat diende als oppervlakteactieve stof om de grootteverdeling te verkleinen. Na 1 minuut magnetisch roeren (magnetische mixer met constante temperatuur, DF-101S, Zhengzhou Greatwall Scientific Industrial and Trade Co., Ltd., Zhengzhou, China), werd de resulterende emulsie onder vacuüm en donker gedurende 30 minuten bij 35 ° C verdampt tot ethanol verwijderen. De zuurgraad in de binnenkamer van Cur-LP werd tijdens de bereiding aangepast met behulp van PBS met gevarieerde pH-waarden van 2,5, 5,0 of 7,4. De resulterende suspensie werd gecentrifugeerd bij een lage snelheid (3000 rpm, 5 min) om vrij curcumine neer te slaan. Het supernatant werd vervolgens met hoge snelheid (16 krpm, 10 min) gecentrifugeerd en de pellets werden vóór verder gebruik opnieuw gesuspendeerd in PBS (pH 7,4). Door deze procedure kregen deze LP's een identieke externe omgeving. De verkregen liposomen met verschillende micro-omgevings-pH-waarden werden respectievelijk gepresenteerd als Cur-LP-2.5, Cur-LP-5,0 en Cur-LP-7,4. Blanco liposomen werden ook gefabriceerd zoals hierboven.
Karakterisatie van liposoom
De hydrodynamische grootte, grootteverdeling en zeta-potentiaal zijn de drie basisparameters voor liposoomsystemen. De grootte en zeta-potentiaal van LP werden bepaald door respectievelijk dynamische lichtverstrooiing (DLS) en elektroforetische lichtverstrooiing (ELS), met behulp van ZetasizerNano ZS90 (Malvern Instruments Ltd., Malvern, VK) bij 25 ° C [29]. De meetcyclus werd automatisch bepaald door het instrumentensysteem. De deeltjesgrootte werd weergegeven door intensiteitsverdeling en de grootteverdeling werd geëvalueerd door polydispersiteitsindex (PDI).
Bepaling van de inkapselingsefficiëntie (EE)
EE, een belangrijke parameter voor kwaliteitscontrole, is van groot belang bij de ontwikkeling van op liposomen gebaseerde toedieningssystemen. De EE-bepaling was gebaseerd op de hogesnelheidscentrifugatiemethode. In het kort, 100 μl Cur-LP's werd gecentrifugeerd bij lage snelheid (3000 tpm, 5 min) om niet-opgeloste vrije curcumine neer te slaan, en 50 μl supernatant werd onderworpen aan hogesnelheidscentrifugeren (16 krpm, 10 min) om Cur- LP's van de kleine opgeloste curcumine. De pellets werden opnieuw gesuspendeerd in 500 μl PBS (d.w.z. 10-voudige verdunning), waarvan een aliquot van 10 l werd gemengd met 300 μl ethanol door vortexen en sonicatie gedurende 30 s. De fluorescentie-intensiteit van curcumine in de resulterende oplossing werd bepaald (excitatiegolflengte (Ex), 458 nm; emissiegolflengte (Em), 548 nm) en gepresenteerd als F e , d.w.z. de fluorescerende intensiteit van ingekapselde curcumine. Nog eens 50 μl verse Cur-LP met ingekapselde en vrije curcumine werd ook 10-voudig verdund met PBS en 10 μl van de verdunde oplossing werd gemengd met 300 μl ethanol. De fluorescentie-intensiteit van de resulterende oplossing werd gemeten en gepresenteerd als F t , d.w.z. de fluorescerende intensiteit van totale curcumine. De EE werd daarom berekend met de volgende vergelijking: EE = F e /F t .
Scanning Electron Microscopy (SEM)
De morfologie van LP werd waargenomen door de scanning elektronenmicroscopie (SEM, INSPECT F, FEI, Nederland) [30]. In het kort, de LP-suspensie werd 100-voudig verdund met gedestilleerd water en één druppel van de verdunde suspensie werd op een schone glasplaat geplaatst. Na drogen aan de lucht werd het monster vlak voor SEM met goud bedekt.
Fysieke stabiliteit van liposomen
Fysieke stabiliteit is een zeer betekenisvolle parameter voor opslag en transport van een colloïdaal systeem. De fysieke stabiliteit van liposoom werd gepresenteerd door colloïdale stabiliteit en onderzocht volgens een eerdere methode [31]. In het kort werd 100 μl LP aan buizen toegevoegd en op 37 ° C gehouden. Op verschillende tijdsintervallen werd de LP-grootte gemeten en vergeleken met de initiële grootte om de thermodynamische stabiliteit aan te geven. Bovendien werd nog eens 300 μl LP aan buizen toegevoegd en op 37 ° C gehouden. Tegelijkertijd werd 100 μl van de vloeistof van de bovenste laag verzameld. De transmissie van de verzamelde monsters werd gemeten bij 550 nm en vergeleken met de initiële waarde om de kinetische stabiliteit aan te geven.
In vitro-release
Het afgifteprofiel van liposoom speelt een belangrijke rol bij het voorspellen van het lot en de werkzaamheid van liposoom in vivo. De in vitro afgifte van curcumine uit Cur-LP werd bestudeerd met behulp van de dynamische dialysemethode [32]. In het kort werd 1 ml van elke Cur-LP toegevoegd aan een dialysezak (molecuulgewichtgrens, 10 kD), die werd gebruikt om liposoom vast te houden, maar de vrijgekomen curcuminemoleculen permeabel te houden. De met specimen beladen dialysezak werd gedrenkt in 4 ml afgiftemedium (0,001 M PBS met 0,1% Tween 80, pH 7,4) en het afgifteonderzoek werd buiten het licht uitgevoerd (37 °C, 100 tpm). Op elk vast tijdsinterval werd het afgiftemedium verzameld en vervangen door 4 ml vers medium om de zinkomstandigheden te simuleren. Het verzamelde medium werd verdund tot 5 ml met PBS en verder 15-voudig verdund met ethanol. De curcumine in de resulterende oplossing werd gekwantificeerd door fluorescentiespectrofotometrie (Ex 458 nm, Em 548 nm). Bovendien werd curcuminepoeder opgelost in het bovenstaande afgiftemedium en werd de curcumine-oplossing vrijgegeven bij pH 7,4 om te onderzoeken of de dialysezak curcuminemoleculen zou vasthouden.
Chemische stabiliteit van liposomale curcumine
Chemische stabiliteit is een belangrijke parameter voor het voorspellen van het metabolisme, de werkzaamheid en toxiciteit van geneesmiddelen. De chemische stabiliteit van Cur-LP's werd onderzocht in 50% FBS. In het kort werd 100 μl Cur-LP's 10-voudig verdund met PBS (pH 7,4) en vervolgens gemengd met 1 ml FBS. De monsters werden geschud op een horizontale schudder weg van licht (37 ° C, 100 rpm). Op vaste tijdsintervallen werd een aliquot van 10 μl monster verzameld en gemengd met 300 μl ethanol onmiddellijk gevolgd door centrifugeren (16 krpm, 5 min). De resterende curcumine in het supernatant werd gekwantificeerd zoals hierboven.
In vitro werkzaamheid tegen kanker
De voorlopige werkzaamheid tegen kanker van de drie Cur-LP's werd onderzocht met behulp van humane lever-hepatocellulaire carcinoom-HepG2-cellen. In het kort werden HepG2-cellen uitgeplaat op de celkweekplaten met 96 putjes met een dichtheid van 10.000 cellen per putje en gekweekt onder standaardomstandigheden (37 °C/5% CO2 ) gedurende 24 uur in PRIM-1640 kweekmedium aangevuld met 10% FBS. Vervolgens werd het kweekmedium verwijderd en werden de cellen gewassen met PBS. De Cur-LP's werden verdund in serumvrij kweekmedium (4 μg/ml curcumine) en toegevoegd aan cellen, gevolgd door continue incubatie gedurende 1 en 3 dagen bij 37 ° C. De OD-waarde van levensvatbare cellen werd gemeten met een cck-8-assay. De met blanco kweekmedium behandelde cellen dienden als controle en de levensvatbaarheid van de cellen (%) was het OD-waardepercentage van de monsters ten opzichte van de controle.
Statistieken
Alle gegevens worden weergegeven als gemiddelde ± sd (standaarddeviaties). De verschillen tussen twee groepen, geanalyseerd door t . van de Student test, werden als statistisch significant beschouwd wanneer de p waarde was minder dan 0,05.
Resultaten en discussie
Karakterisering van liposoom
De micro-omgevings-pH van liposoom verwijst naar de zuurgraad in de binnenste waterige kamer van liposoom (Fig. 1), die verschilt van de pH in de externe omgeving. In dit werk was de externe omgevings-pH van alle liposoomsuspensies 7,4 tenzij anders vermeld.
Deeltjesgrootte, zeta-potentiaal en inkapselingsefficiëntie (EE) zijn belangrijke parameters voor kwaliteitscontrole van liposoom. De grootte van drie Cur-LP's was vergelijkbaar met elkaar (ongeveer 300 nm, figuur 2a). De PDI van elke formulering was lager dan 0,2, wat wijst op een smalle grootteverdeling. Interessant is dat de negatieve zeta-potentiaal van Cur-LP-7.4 (−9 mV) aanzienlijk lager is dan die van de andere twee Cur-LP's (~ −18 mV). Gewoonlijk zou de negatieve zeta-potentiaal afnemen en zelfs worden omgezet in een positieve waarde met het verlagen van de pH van de disperse fase als gevolg van de toename van H + concentratie. We hebben dit fenomeen inderdaad waargenomen bij het bereiden van Cur-LP's in niet-buffer HCl / NaOH-oplossingen met een pH van 2, 5, 5,0 en 7, 4 (figuur 2b). In het geval van PBS is het bestaan van PO4 3− , HPO4 2− , en/of H2 PO4 − en hun interactie met LP kan leiden tot meer gecompliceerde situaties en andere resultaten. Het is algemeen bekend dat zeta-potentiaal een sleutelrol speelt bij het handhaven van de colloïdale stabiliteit van suspensie op nanoschaal. Over het algemeen leidt een hogere absolute waarde van de zeta-potentiaal tot een stabieler colloïdaal veersysteem.
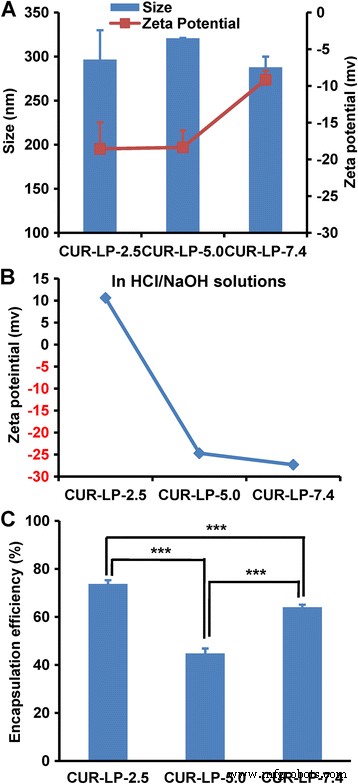
Fysisch-chemische karakterisering van liposomen. een Hydrodynamische grootte en zeta-potentiaal van Cur-LP's vervaardigd in PBS met respectievelijk pH 2,5, 5,0 en 7,4. b Zeta-potentiaal van Cur-LP's vervaardigd in HCl / NaOH-oplossingen met respectievelijk pH 2,5, 5,0 en 7,4. c Inkapselingsefficiëntie van Cur-LP's bereid in PBS. Gegevens weergegeven als gemiddelde ± sd (n = 3). Statistische significantie tussen groepen:***p < 0,001
EE is een punt van zorg tijdens de ontwikkeling van liposomen. Gewoonlijk is het verhogen van EE belangrijk om de kosten te verlagen en de werkzaamheid te vergroten. In dit werk is de EE van Cur-LP-2.5 74% (Fig. 2c), wat de hoogste is van Cur-LP-5,0 (45%) en Cur-LP-7,4 (64%), wat aangeeft dat Cur- LP-2.5 is de beste formulering voor het leveren van curcumine vanaf het punt van EE. De redenen voor de variëteit in EE bij verschillende pH-waarden zijn niet erg duidelijk, maar kunnen verband houden met de oplosbaarheid van curcumine, dat oplosbaar is in alkalische of extreem zure oplosmiddelen [33].
De morfologie van liposomen die door SEM zijn onderzocht, wordt getoond in Fig. 3. De deeltjes van LP-2.5 (Fig. 3a) en LP-5.0 (Fig. 3b) zijn bolvormig en hebben een uniforme deeltjesverdeling. De LP-7.4 vertoont ook een bolachtige vorm, maar hechting tussen deeltjes kan duidelijk worden waargenomen (Fig. 3c), wat aangeeft dat het droogproces tijdens de voorbereiding van het SEM-monster zou leiden tot aggregatie van LP-7.4. Dit kan te wijten zijn aan de relatief lage absolute waarde van zeta-potentiaal van LP-7.4 (figuur 2a). Bovendien is de deeltjesgrootte gemeten door SEM kleiner dan de hydrodynamische grootte gemeten door DLS, wat te wijten is aan het verlies van de hydratatieschil van liposoom na het droogproces voor SEM.
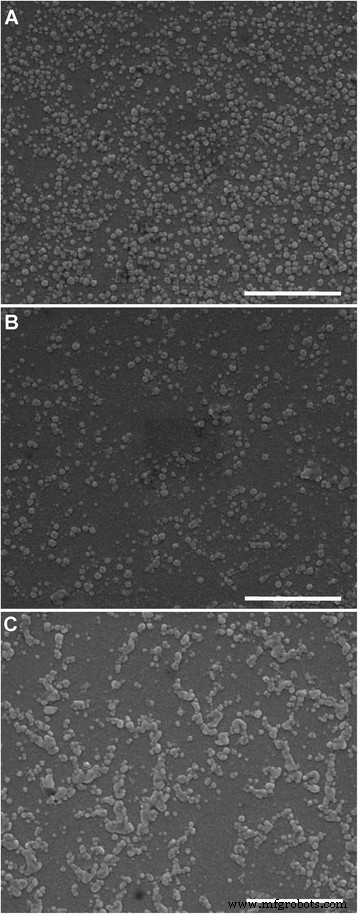
SEM-beelden van liposoom met een micro-omgevings-pH van a 2.5, b 5.0, en c 7.4. Schaalbalk , 1 μm
Fysieke stabiliteit van liposoom
Liposoom is een colloïdaal systeem en de fysieke stabiliteit ervan kan worden weergegeven door colloïdale stabiliteit, die aanzienlijke gevolgen heeft voor de opslag van liposomen en verdere toepassingen [34, 35]. Aggregatie van deeltjes (thermodynamische instabiliteit) en sedimentatie (kinetische instabiliteit) zijn de twee essentiële aspecten van colloïdale instabiliteit. Aggregatie leidt tot een grotere schijnbare grootte en sedimentatie leidt tot veranderingen in de transmissie van suspensie. Wat nog belangrijker is, is dat de toename van de grootte direct van invloed kan zijn op de werkzaamheid van nanosystemen, aangezien is aangetoond dat de deeltjesgrootte een grote invloed heeft op de cellulaire opname, cytotoxiciteit, farmacokinetisch profiel en weefseldistributie [36, 37].
Hier hebben we de aggregatie- en sedimentatie-eigenschappen van drie liposoomsystemen onderzocht om respectievelijk hun thermodynamische en kinetische stabiliteit aan te geven. Zoals weergegeven in figuur 4a, vertoonden de drie LP's geen substantiële veranderingen in hydrodynamische grootte binnen 72 uur, wat aangeeft dat al deze LP's een zeer hoge thermodynamische stabiliteit hebben. Ondertussen was de transmissieverandering van alle drie de LP's minder dan 10% (Fig. 4b), wat wijst op weinig sedimentatie van deeltjes en dus een hoge kinetische stabiliteit. Deze resultaten suggereren dat de drie LP's binnen 72 uur een uitstekende colloïdale stabiliteit hebben en dat de pH van de micro-omgeving geen invloed heeft op de fysieke stabiliteit van liposoom.
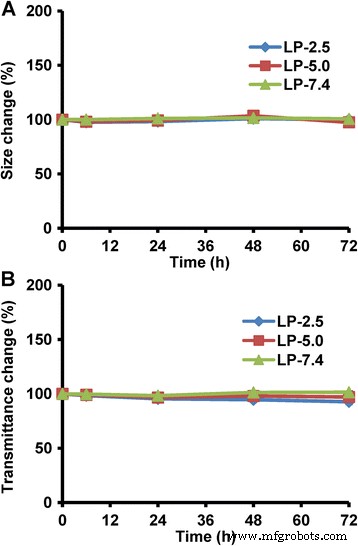
Fysische stabiliteit van liposomen met verschillende pH-waarden in de micro-omgeving (pH 2,5, 5,0 en 7,4). een Thermodynamische stabiliteit die de aggregatie van deeltjes aangeeft. b Kinetische stabiliteit die de sedimentatie van deeltjes aangeeft. De gegevens worden weergegeven als gemiddelde ± sd (n = 3)
In vitro-release
Het geneesmiddelafgifteprofiel van liposoom wordt gewoonlijk onderzocht om de kwaliteit van de formulering te evalueren, een referentie te geven voor het doseringsregime en de effectiviteit in vivo te voorspellen. In het algemeen hebben bijna alle liposomale systemen een eigenschap voor langdurige geneesmiddelafgifte. Hier hebben we het in vitro afgiftegedrag van drie Cur-LP's in PBS (pH 7,4) onderzocht. Ondertussen werd ook de afgifte van curcumine-oplossing onderzocht om te bevestigen of het dialysemembraan de diffusie van curcumine zou beïnvloeden. Zoals getoond in Fig. 5a, werd curcumine zeer snel vrijgemaakt uit de oplossing (>80% na 6 uur), wat aangeeft dat de dialysezak geen effect had op de diffusie van curcumine. In tegenstelling tot de snelle afgifte van curcumine-oplossing, vertoonden alle Cur-LP's een duidelijke eigenschap voor aanhoudende afgifte (Fig. 5b), en de afgifteprofielen leken erg op elkaar, wat aangeeft dat de pH van de micro-omgeving geen significant effect had op curcumine snelheid loslaten. In detail werd curcumine in de eerste 8 uur iets sneller afgegeven, waarschijnlijk vanwege de eerste burst-afgifte (het cumulatieve afgiftepercentage was ongeveer 5%). Na 8 uur kwam curcumine iets langzamer vrij en het cumulatieve afgiftepercentage was binnen 72 uur ~30%. Aangenomen wordt dat de afgiftesnelheid in vivo of in aanwezigheid van serum aanzienlijk sneller zou zijn, gedeeltelijk als gevolg van het metabolisme van lipiden.
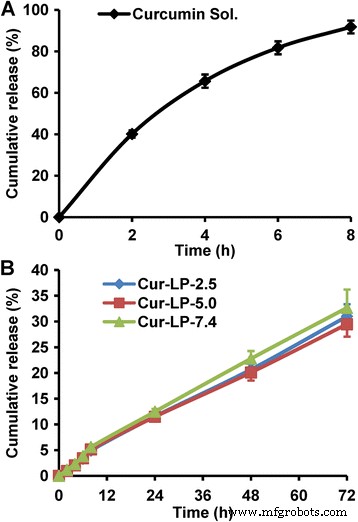
In vitro afgifteprofielen van verschillende curcumineformuleringen in PBS (pH 7,4). een Curcumine-oplossing, waarin curcumine werd opgelost in PBS met 0,1% Tween 80 (pH 7,4). b Cur-LP's met een gevarieerde micro-omgevings-pH van respectievelijk 2,5, 5,0 en 7,4. De gegevens worden weergegeven als gemiddelde ± sd (n = 3)
Interessant is dat de release-profielen van alle drie de Cur-LP's dicht bij rechte lijnen liggen. Daarom werd de lineaire aanpassing aan de drie ontgrendelingsprofielen uitgevoerd. Zoals weergegeven in tabel 1, vertoonden al deze profielen een zeer goede lineariteit met een aanpassingsgraad hoger dan 0,99 (regressievergelijkingen worden ook weergegeven), wat suggereert dat de afgifte van Cur-LP's past bij nulde-orde kinetiek. In andere vergelijkbare onderzoeken bleek de afgifte van curcumine uit liposoom niet-lineair [38, 39]. Vanuit het oogpunt van geneesmiddelenonderzoek en -ontwikkeling is de nulde-orde-afgiftekinetiek het meest ideale afgifteprofiel omdat het een constante geneesmiddelafgiftesnelheid biedt en dus in staat is om het therapeutische effect gedurende lange tijd te behouden, de toedieningstijden te verkorten en bijwerkingen te verminderen . Daarom kunnen de LP's die in dit werk zijn voorbereid, veelbelovende dragers zijn voor gecontroleerde medicijnafgifte.
Effect van micro-omgeving pH op chemische stabiliteit van Cur-LP
De chemische stabiliteit van liposomale curcumine in FBS wordt getoond in Fig. 6. Na incubatie gedurende 2 uur bleef 89% curcumine over voor Cur-LP-2.5, significant hoger dan 74% voor Cur-LP-5,0 en 61% voor Cur-LP -7.4 (p < 0,001). 4 uur na de incubatie bleef 69% curcumine over voor Cur-LP-2.5, significant hoger dan 53% voor Cur-LP-5,0 en 40% voor Cur-LP-7.4 (p <0,01). 6 uur na de incubatie bleef 55% curcumine over voor Cur-LP-2.5, nog steeds significant hoger dan 43% voor Cur-LP-5,0 en 34% voor Cur-LP-7.4 (p <0,05). Het is duidelijk dat de chemische stabiliteit van Cur-LP's micro-omgevings-pH-afhankelijk is:Cur-LP-2.5 > Cur-LP-5.0 > Cur-LP-7.4. Deze pH-afhankelijke chemische stabiliteit van Cur-LP komt overeen met een ander werk, dat de pH-afhankelijke stabiliteit van vrij curcumine aantoonde [26]. De in vitro afgifte werd uitgevoerd in serumvrij medium en de cumulatieve afgifte zou na 72 uur 30% kunnen zijn. De chemische stabiliteitsstudie werd echter uitgevoerd in een serumbevattende oplossing, waarin serumenzymen de vrijgekomen curcumine konden afbreken en ook liposoom konden breken en zo de niet-vrijgegeven curcumine konden afbreken. Dit is de reden waarom 30% curcumine vrijkwam na 72 uur in de in vitro afgiftestudie, maar slechts 55% bleef na 6 uur voor Cur-LP-2.5 in de serumstabiliteitsstudie.
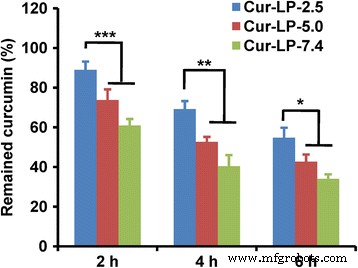
Chemische stabiliteit van liposomale curcumine (Cur-LP's) met verschillende pH-waarden in de micro-omgeving (pH 2,5, 5,0 en 7,4). De stabiliteit werd onderzocht door de resterende curcumine te kwantificeren na het incuberen van Cur-LP's met 50% FBS. De gegevens worden weergegeven als gemiddelde ± sd (n = 3). Statistische significantie tussen groepen:***p < 0.001, **p < 0.01, *p < 0,05
Liposomen bestaan in structuur uit twee delen:de ene is de hydrofobe lipidedubbellaag en de andere is de hydrofiele binnenste waterige kamer. Het is gemakkelijk te begrijpen dat een pH-gevoelig hydrofiel geneesmiddel zich in de binnenste waterige kamer zou bevinden en de stabiliteit ervan aanzienlijk zou worden beïnvloed door de micro-omgevings-pH in de waterige kamer, waar het buffervolume en de buffercapaciteit veel hoger zouden zijn dan die in de lipide dubbellaag. Curcumine is daarentegen een hydrofoob molecuul en zou zich in de lipidedubbellaag bevinden. Om deze reden is het best interessant om de micro-omgeving pH-afhankelijke chemische stabiliteit van liposomale curcumine te vinden. Aangenomen wordt dat de ruimte in de lipidedubbellaag niet absoluut watervrij zou zijn, hoewel deze wel hydrofoob is. Zoals we weten, is het levende celmembraan niet absoluut watervrij in zijn lipidedubbellaag. In plaats daarvan bevat het een bepaald klein volume waterige oplossing voor het transport van in water oplosbare moleculen en ionen. Evenzo zou een bepaald klein volume bufferoplossing met dezelfde componenten als de binnenkamer ook aanwezig zijn in de hydrofobe lipidedubbellaag na succesvolle voorbereiding van liposoom. Het hydrofobe geneesmiddel dat zich in de lipidedubbellaag bevindt, kan dus direct worden beïnvloed door de micro-omgevings-pH van het liposoom. Bovendien kan de zure micro-omgeving de activiteiten verminderen van sommige enzymen die de beste activiteit vertonen in normale fysiologische toestand. Dit draagt ook bij aan de hogere chemische stabiliteit van liposomale curcumine in de lagere pH van de micro-omgeving. Er is gemeld dat liposomen die zijn samengesteld uit eifosfatidylcholine (EPC) snel hun interne pH-gradiënt in buffer (pH 7,4) verloren, en het vermogen om de pH-gradiënt te behouden werd aanzienlijk verbeterd door EPC (faseovergangstemperatuur (T m ) ≈ −5 °C) met de hoge T m (41 °C) lipide DPPC (dipalmitoylfosfatidylcholine) en door toevoeging van cholesterol [40]. In dit huidige werk is het liposoom samengesteld uit sojalecithine (T m is ongeveer 238,2 °C [41]) en cholesterol. Daarom kan worden verwacht dat de micro-omgevings-pH-gradiënt van liposomen die in dit werk zijn bereid, gedurende een lange periode behouden blijft. Dit is een sterke ondersteuning van de resultaten en veronderstellingen die hierboven zijn weergegeven.
In vitro werkzaamheid tegen kanker
We hebben hierboven de micro-omgeving pH-afhankelijke chemische stabiliteit van liposomale curcumine aangetoond. Hier hebben we een voorlopige in vitro-studie uitgevoerd om de werkzaamheid tegen kanker van deze liposomale curcumine te onderzoeken. Interessant is dat de blanco LP's de celgroei op dag 1 konden verbeteren en deze functie tot op dag 3 tot op zekere hoogte konden behouden in vergelijking met de controlegroep (Fig. 7). Dit geeft aan dat blanco LP's voeding aan cellen kunnen leveren, wat consistent is met ons vorige rapport [27]. De vrije curcumine vertoonde weinig werkzaamheid tegen kanker vanwege de vrij beperkte oplosbaarheid. Daarentegen vertoonden Cur-LP's een significante werkzaamheid tegen kanker op een micro-omgeving pH-afhankelijke manier. Na behandeling van 1 dag vertoonden Cur-LP-2.5 en Cur-LP-5.0 een significant sterker vermogen om HepG2-celgroei te remmen dan Cur-LP-7.4 (de levensvatbaarheid van de cellen was 80% voor Cur-LP-2.5 en Cur-LP -5,0 en 90% voor Cur-LP-7.4). Op dag 3 na de behandeling nam de levensvatbaarheid van de cellen aanzienlijk af en Cur-LP-2.5 en Cur-LP-5.0 vertoonden vergelijkbare werkzaamheid tegen kanker en significant hoger dan Cur-LP-7.4. De levensvatbaarheid van de cellen was 24% voor Cur-LP-2.5 (p <0,05 vs Cur-LP-7.4), 21% voor Cur-LP-5.0 (p <0,01 vs Cur-LP-7.4) en 39% voor Cur-LP-7.4. Deze resultaten geven aan dat de werkzaamheid tegen kanker van liposomaal curcumine afhankelijk is van de micro-omgeving pH en tijd. Gezien de hogere EE en chemische stabiliteit van Cur-LP-2.5 dan Cur-LP-5.0, zou liposoom met een micro-omgevings-pH van 2,5 het grootste potentieel hebben voor praktische toepassing.
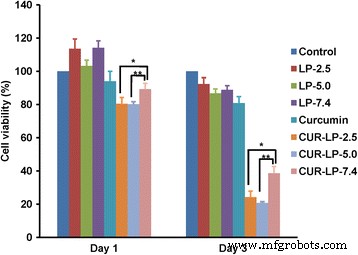
Antikankereffectiviteit van liposomale curcumine met een gevarieerde micro-omgevings-pH (2,5, 5,0 en 7,4). De levensvatbaarheid van HepG2-cellen op dag 1 en 3 na behandeling met blanco LP's, vrije curcumine en Cur-LP's werd onderzocht met een cck-8-assay. De cellen behandeld met serumbevattend blanco kweekmedium dienden als controle. De gegevens worden weergegeven als gemiddelde ± sd (n = 3). Statistische significantie tussen groepen:**p < 0.01, *p < 0.05
Conclusies
Liposoom, als een veelgebruikt medicijnafgiftesysteem, is in staat om de oplosbaarheid van in water onoplosbare geneesmiddelen te verbeteren, de nuttige lading van geneesmiddelen te beschermen tegen de zware fysiologische omgeving en de nuttige lading af te leveren aan een gericht weefsel. De afgifte van pH-gevoelige geneesmiddelen wordt echter nog steeds beperkt door hun natuurlijke instabiliteit in fysiologische omstandigheden (neutrale omgeving). In dit huidige werk stellen we een nieuwe benadering voor voor het verbeteren van de chemische stabiliteit van pH-gevoelige geneesmiddelladingen door de micro-omgevingszuurgraad van liposoom te reguleren. De bevindingen tonen aan dat de chemische stabiliteit en in vitro werkzaamheid van het model pH-gevoelige geneesmiddel curcumine aanzienlijk wordt verbeterd door de micro-omgeving van liposoom aan te zuren. Concluderend, regulering van de micro-omgevings-pH van liposoom is haalbaar om de chemische stabiliteit van pH-gevoelige medicijnladingen te verbeteren, zelfs voor de hydrofobe medicijnen die zich in de lipidedubbellaag bevinden.
Nanomaterialen
- Chemisch frezen van titaniumlegering
- Fysische en chemische eigenschappen van wolfraam
- Chemische eigenschappen van titanium
- Wat is chemische dampafzetting?
- Circuit-effecten
- Nicotinepatch
- Nanovezels en filamenten voor verbeterde medicijnafgifte
- Druggebruik
- Top 4 chemisch bestendige kunststoffen
- Effecten van smeden op koolstofstaal
- Horizontale draaibank bevordert stabiliteit



