IJzer-koolstofevenwichtsdiagram met uitleg [fasediagram]
In dit artikel zullen we het hebben over het Iron Carbon Equilibrium diagram , gebruik van een evenwichtsdiagram, soorten ijzerkoolstofevenwichtsdiagrammen en verschillende fasen en termen die verband houden met het ijzerkoolstoffasediagram.
Wat zijn fasediagrammen?
Fasediagrammen zijn grafische weergaven van de fasen die aanwezig zijn in een legering onder verschillende temperatuur-, druk- en chemische samenstellingsomstandigheden.
Het stollen van metaallegeringen wordt duidelijk begrepen door middel van evenwichtsdiagrammen. Dit zijn grafische weergaven van toestandsveranderingen als gevolg van variaties in temperatuur en concentratie. Aangezien dit diagram de aard en samenstelling van legeringen aangeeft, en de hoeveelheid en samenstelling van fasen in een bepaald systeem, staat het ook bekend als constitutiediagram of fasediagram.
Equilibriumdiagramkenmerken en gebruik
Evenwicht houdt in dat veranderingen die in een systeem optreden als gevolg van een proces dat in één richting verloopt, volledig worden gecompenseerd door veranderingen als gevolg van de omkering van het proces in het systeem. Het wordt dus beschouwd als een dynamische evenwichtstoestand tussen atomaire bewegingen waarbij de resultante nul is.
De snelheden van temperatuur- of samenstellingsveranderingen waren extreem traag tijdens het experimentele werk, zodat de legering "tot rust kwam" voordat een variabele zoals temperatuur opnieuw werd veranderd. De toestand is er daarom eerder een van rust dan van verandering.
Equilibriumdiagram geeft het volgende aan:
1. Temperatuur waarbij de vaste legering begint te smelten en eindigt met smelten.
2. Mogelijke faseveranderingen die optreden als gevolg van verandering van samenstelling of temperatuur.
Welk evenwichtsdiagram representeert ?
Het diagram beschrijft de geschikte omstandigheden voor twee of meer fasen om in evenwicht te bestaan. Het waterfasediagram beschrijft bijvoorbeeld een punt (triple point) waar water in drie verschillende fasen tegelijk kan bestaan. Dit gebeurt net boven de vriestemperatuur (0,01°C) en 0,006 atm.
Gebruik van het evenwichtsdiagram in de metallurgie
- Ontwikkeling van de nieuwe legeringen op basis van applicatie-eisen.
- Productie van deze legeringen.
- Ontwikkeling en implementatie van geschikte warmtebehandelingsprocedures om de chemische, fysische en mechanische eigenschappen van deze nieuwe legeringen te verbeteren.
- Problemen oplossen die zich voordoen tijdens het gebruik van deze nieuwe legeringen, wat uiteindelijk de voorspelbaarheid van het product verbetert.
IJzer-koolstof-evenwichtsdiagram
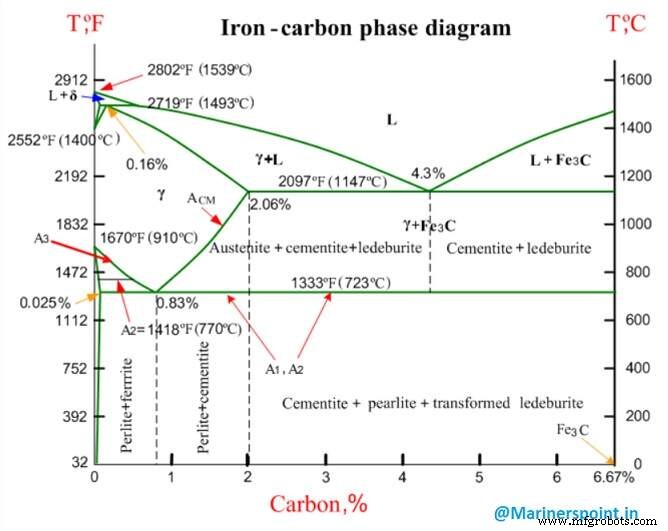
Het IJzerkoolstofevenwichtsdiagram (ook wel het ijzerkoolstoffasediagram genoemd) is een grafische weergave van de respectieve microstructuurtoestanden van de legering ijzer-koolstof (Fe-C), afhankelijk van de temperatuur en het koolstofgehalte.
Het ijzerkoolstoffasediagram wordt vaak gebruikt om de verschillende fasen van staal en gietijzer volledig te begrijpen. Staal en gietijzer zijn zowel ijzer- als koolstoflegeringen. Bovendien bevatten beide legeringen in kleine hoeveelheden sporenelementen.
De grafiek is vrij complex, maar omdat we ons onderzoek beperken tot Fe3C, kijken we alleen naar maximaal 6,67 gewichtsprocent koolstof.
Soorten ijzer-koolstofevenwichtsdiagram
Het binaire ijzer-koolstofevenwichtsdiagram is de basis van staal en gietijzer. Het gaat om transformaties die optreden in legeringen met samenstellingen van zuiver ijzer tot cementiet (6,67 procent koolstof). Er zijn twee versies van het ijzer-koolstofevenwichtsdiagram:
1. IJzer-cementiet systeem. 2. IJzer-grafiet systeem.
Deze twee systemen zijn afhankelijk van de afkoelsnelheid. Snelle afkoeling produceert cementiet en het systeem staat bekend als Iron-cementite system . In dit systeem bereiken de structuren gevormd in de gestolde fasen onvoldoende volledig evenwicht. Dus het ijzer-cementietsysteem is een metastabiel een.
Terwijl langzaam afkoelen grafiet produceert en het systeem bekend als ijzer-grafietsysteem . De structuren die gevormd worden in de gestolde fase bereiken een voldoende volledig evenwicht. Dit is dus een stabiele een.
Soorten ferrolegeringen op ijzerkoolstofevenwichtsdiagram
De gewichtspercentageschaal op de X-as van het ijzerkoolstoffasediagram varieert van 0% tot 6,67% Koolstof. Het metaal staat eenvoudigweg bekend als ijzer of puur ijzer tot een maximaal koolstofgehalte van 0,008 gewichtsprocent koolstof. Bij kamertemperatuur bestaat het in het ferriet staat.
Staal is een ijzer-koolstoflegering met een koolstofgehalte van 0,008 tot 2,14 procent. Staalsoorten binnen dit bereik staan bekend als koolstofarm staal (of zacht staal), gemiddeld koolstofstaal , en hoog koolstofstaal .
Wanneer het koolstofgehalte hoger is dan 2.14 procent bereiken we het gietijzer fase. Gietijzer is extreem hard, maar de brosheid ervan beperkt de toepassingen en vormmethoden ernstig.
IJZER-CEMENTITE-SYSTEEM
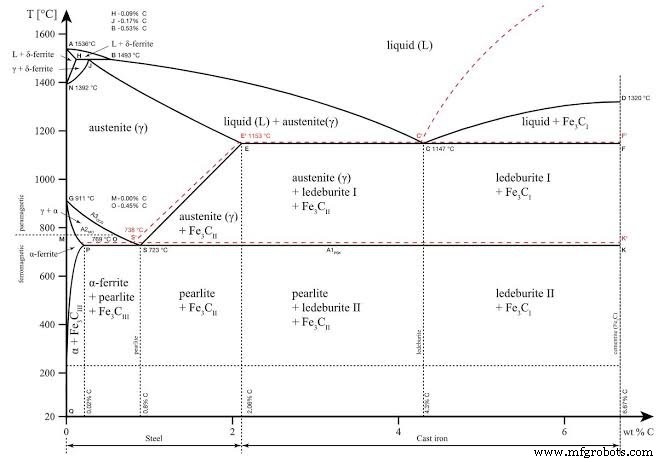
Als een reeks tijd-temperatuur verwarmingscurven wordt gemaakt voor staal met verschillende koolstofgehalten en de bijbehorende kritische punten worden uitgezet, zou een diagram vergelijkbaar met Fig. 2.14 worden verkregen. Dit diagram, dat alleen van toepassing is bij langzame afkoeling, staat bekend als een gedeeltelijk IJzerkoolstoffasediagram . Door naar dit diagram te verwijzen, kan men gemakkelijk de juiste afschriktemperaturen voor elk koolstofstaal waarnemen. De kritieke punten in Fig. 2.14 op de lijn PSK worden aangegeven met A1, die op lijn GS met A3 en die van lijn SE met Acm. P>
IJzer-koolstof-evenwichtsdiagram met uitleg
Austeniet
Austenitisch , vaste oplossing van koolstof en andere bestanddelen in een bepaalde vorm van ijzer bekend als γ (gamma) ijzer. Laten we het voorbeeld nemen van een stuk 0,20 procent koolstofstaal dat is verwarmd tot een temperatuur van rond de 850°C. Boven Ar3, punt (GS-lijn) is dit staal een vaste oplossing (interstitiaal type) van koolstof in gamma-ijzer en wordt austeniet genoemd . Het heeft een kubusvormig rooster in het midden en is niet-magnetisch.
Gewoon austeniet kan tot ongeveer 2 procent koolstof bevatten bij een temperatuur van 1130°C. Bij afkoeling van dit staal beginnen de ijzeratomen een lichaamsgecentreerd kubisch rooster te vormen onder het punt Ar3 (GS-lijn). Deze nieuwe structuur die wordt gevormd, wordt ferriet of alfa-ijzer genoemd en is een vaste oplossing van koolstof in alfa-ijzer met tot 0,008 procent koolstof bij kamertemperatuur.
Als het staal wordt afgekoeld tot Ar1 (PSK-lijn), wordt extra ferriet gevormd. Bij de Arı-lijn wordt het austeniet dat overblijft getransformeerd naar een nieuwe structuur genaamd perliet . De naam perliet is te danken aan zijn parelachtige glans. Het bestaat uit afwisselende platen van ferriet en cementiet en bevat ongeveer 87 procent ferriet. Pearlite kan een fijne tot grove lamellaire of korrelige structuur hebben. Dit is een sterke substantie en kan redelijk goed worden gesneden met snijgereedschap, d.w.z. het perlietbestanddeel in staal is bewerkbaar.
Eutectoid-staal
Naarmate het koolstofgehalte van het staal boven 0,20 procent stijgt, daalt de temperatuur waarbij het ferriet voor het eerst uit de austeniet wordt afgestoten, totdat bij ongeveer 0,80 procent koolstof (punt S) geen vrij ferriet uit de austeniet wordt verwijderd. Dit staal wordt eutectoid staal genoemd en is 100 procent perliet .
Eutectoid Punt
Wat is Eutectoid Point?
Het eutectoïde punt in elk metaal is, zoals eerder gezegd, de laagste temperatuur waarbij veranderingen optreden in een vaste oplossing.
Als het koolstofgehalte van het staal groter is dan eutectoid (0,8 procent koolstof), wordt een nieuwe lijn waargenomen in het ijzerkoolstoffasediagram aangegeven met Acm (S-lijn). De lijn geeft de temperatuur aan waarbij ijzercarbide voor het eerst wordt afgestoten uit de austeniet in plaats van ferriet.
Het ijzercarbide (Fe3C) staat bekend als cementiet . Het is extreem hard, bros en verschijnt als parallelle platen (lamellaire lagen), als ronde deeltjes (sferoïden) of als enveloppen rond de perlietkorrels. Bij punt C staat het eutectische mengsel dat 4,3 procent koolstof bevat bekend als ledeburiet . Dit wordt zelden gezien in langzaam afgekoelde legeringen, omdat het door zijn onstabiele aard tijdens afkoeling na stollen in andere fasen uiteenvalt.
Hypoeutectoïde en hypereutectoïde
Staalsoorten die minder dan 0,80 procent koolstof bevatten, worden hypoeutectoïde genoemd en die welke meer dan 0,8 procent koolstof bevatten, worden hypereutectoïde genoemd staalsoorten. Deze terminologie is alleen van toepassing op gewoon en laaggelegeerd staal. Bij hooggelegeerde staalsoorten wordt de eutectische samenstelling gewijzigd en bestaat de structuur misschien niet eens.
Allereerst moet worden opgemerkt dat het normale evenwichtsdiagram werkelijk het metastabiele evenwicht tussen ijzer en ijzercarbide (cementiet) weergeeft. Cementiet is metastabiel en het ware evenwicht zou tussen ijzer en grafiet moeten zijn.
Hoewel grafiet veel voorkomt in gietijzer (2-4 gew.% C), is het gewoonlijk moeilijk om deze evenwichtsfase in staal (0,03-1,5 gew.% C) te verkrijgen. Daarom moet rekening worden gehouden met het metastabiele evenwicht tussen ijzer en ijzercarbide, omdat dit in de praktijk relevant is voor het gedrag van de meeste staalsoorten.
Iron Graphite-systeem
IJZER-GRAFIET SYSTEEM
Er is al gezegd dat ijzercarbide of cementiet een metastabiel is, hoewel het onder normale omstandigheden de neiging heeft om voor onbepaalde tijd aan te houden. Wanneer cementiet ontleedt, doet het dat volgens de reactie:
Fe3C <——–> 3Fe + C
In de stabiele fase, vrije koolstof of grafiet treedt op in plaats van de fase die bekend staat als cementiet . Bij een kleine mate van onderkoeling wordt grafiet gevormd wanneer gietijzer stolt vanuit de vloeibare toestand. Langzame afkoeling bevordert grafitisatie . Snelle afkoeling onderdrukt de grafitisering geheel of gedeeltelijk en leidt tot de vorming van cementiet.
Een ijzer-grafietsysteem (als stippellijn) wordt getoond in Fig. 2.14. Het geval van een koolstoflegering die 3,5 gewichtsprocent koolstof bevat, wordt als illustratie genomen
Bij punt 1 is de legering in vloeibare toestand. Bij punt 2 op de koellijn kan de reactie die optreedt worden uitgedrukt als:
Afbeelding
> Tussen punt 2 en 3 wordt de overtollige koolstof in het austeniet neergeslagen als vrij grafiet en niet als cementiet. Bij punt 3 vindt de eutectische reactie plaats. Dit wordt uitgedrukt als:
Afbeelding
Het mechanisme van eutectoïde transformatie moet een enkele vaste fase in twee andere transformeren, beide met samenstellingen die verschillen van het origineel.
Als we de eutectoïde ontleding van ijzer als voorbeeld nemen, verandert austeniet met 0,8% C in ferriet (ijzer dat bijna geen koolstof bevat) en cementiet (Fe3C, dat 25 at% koolstof bevat). Daarom moeten koolstofatomen samen diffunderen om Fe3C te vormen, waarbij ferriet overblijft. Kernen van kleine platen van ferriet en cementiet vormen zich aan de korrelgrenzen van het austeniet, en koolstofdiffusie vindt plaats op een zeer lokale schaal net voor het grensvlak (schema hieronder).
Zo groeien de platen, terwijl ze de austeniet opslokken, om perliet te vormen. Het proces van grafitisering wordt gecontroleerd door de afkoelsnelheid te variëren en door de metallische matrix op de juiste manier te legeren.
Termen gebruikt in Iron Carbon Equilibrium Diagram
Eutectic Point
Het eutectoïde punt in elk metaal is de laagste temperatuur waarbij veranderingen optreden in een vaste oplossing.
Op deze punten vinden eutectische reacties plaats, waar een vloeibare fase bevriest tot een mengsel van twee vaste fasen. Dit gebeurt wanneer een vloeibare legering met een eutectische samenstelling wordt afgekoeld tot zijn eutectische temperatuur.
Eutectische legeringen zijn de legeringen die zich op dit punt vormen. Legeringen aan de linker- en rechterkant van dit punt staan bekend als hypoeutectische legeringen en hypereutectische legeringen ('hypo' in het Grieks betekent minder dan, 'hyper' betekent groter dan).
Austeniet
Austeniet, vaste oplossing van koolstof en andere bestanddelen in een bepaalde vorm van ijzer bekend als γ (gamma) ijzer.
Deze fase is een vaste oplossing van koolstof in FCC Fe met een maximale oplosbaarheid van 2,14% C. Bij verdere verwarming wordt het bij 1395°C omgezet in BCC-ferriet. γ-austeniet is onstabiel bij temperaturen onder de eutectische temperatuur (727°C), tenzij het snel wordt afgekoeld.
Alpha-ijzer of ferriet
Bestaande bij lage temperaturen en een laag koolstofgehalte, α-ferriet is een vaste oplossing van koolstof in BCC Fe. Deze fase is stabiel bij kamertemperatuur. In de grafiek kan het worden gezien als een strook aan de linkerrand met de Y-as aan de linkerkant en A2 aan de rechterkant. Deze fase is magnetisch beneden 768°C.
Het heeft een maximaal koolstofgehalte van 0,022% en zal bij 912 °C transformeren in γ-austeniet, zoals weergegeven in de grafiek.
Cementiet
Cementiet, een metastabiele fase van deze legering met een vaste samenstelling van Fe3C, is een metastabiele fase van deze legering. Bij kamertemperatuur ontleedt het extreem langzaam in ijzer en koolstof (grafiet).
Deze ontledingstijd is lang en duurt veel langer dan de levensduur van de applicatie bij kamertemperatuur. Andere factoren, zoals hoge temperaturen en de toevoeging van bepaalde legeringselementen, kunnen deze ontleding beïnvloeden door de vorming van grafiet te bevorderen.
Cementiet is hard en bros, waardoor het ideaal is voor staalwapening. De mechanische eigenschappen worden bepaald door de microstructuur, die wordt bepaald door hoe het wordt gemengd met ferriet.
We hebben geprobeerd alle termen met betrekking tot het ijzerkoolstoffasediagram te behandelen, inclusief de verschillende fasen en termen die erin worden gebruikt om het op een betere manier te begrijpen. Ik hoop dat je dit artikel over ijzerkoolstofevenwichtsdiagram leuk vond . Geef uw feedback in de onderstaande opmerking.
Industriële technologie
- Circuit met een schakelaar
- 3D-printen met zeer sterk materiaal – composiet koolstofvezel-nylon
- Bentley brengt Bentayga uit met 's werelds grootste koolstofvezelwielen
- Racing drone met volledig gesloten monocoque van koolstofvezel
- Porsche begint jong met koolstofvezel kinderwagen
- Elektrische ontladingsbewerking (EDM):mechanica, werkingsprincipes en circuits (met diagram)
- IJzerproductie door hoogoven en kooldioxide-emissies
- Wat zijn de onderdelen van een las? - Leg uit met diagram
- Wat is het ijzer-koolstoffasediagram?
- 11 verschillende soorten lasproces met behulp van diagram
- Verschillende soorten plaatbewerkingen met diagram



