Krypton
Achtergrond
Krypton is chemisch element nummer 36 op het periodiek systeem der elementen. Het behoort tot de groep elementen die bekend staat als de edelgassen. De andere edelgassen zijn helium, neon, argon, xenon en radon. Onder normale omstandigheden is krypton een kleurloos, smaakloos en geurloos gas. De dichtheid bij normale temperatuur en druk is ongeveer 0,5 oz per gallon (3,7 g per liter), waardoor het bijna drie keer zwaarder is dan lucht. Bij extreem lage temperaturen kan krypton bestaan als een vloeistof of een vaste stof. Het kookpunt van krypton is -243,81 ° F (-153,23 ° C), en het vriespunt is slechts iets lager bij -251,27 ° F (-157,37 ° C).
Natuurlijk krypton is een mengsel van zes stabiele isotopen. Isotopen zijn atomen met hetzelfde aantal protonen maar met een verschillend aantal neutronen. Het aantal protonen (het atoomnummer) bepaalt welk element aanwezig is, terwijl het totale aantal protonen en neutronen het atoomgewicht van het atoom bepaalt. De isotopen van krypton hebben allemaal 36 protonen en zijn genoemd naar hun atoomgewicht. Krypton-84, dat 48 neutronen heeft, is de meest voorkomende isotoop en vormt 57% van het natuurlijke krypton. De andere stabiele isotopen van krypton zijn krypton-86 (50 neutronen, 17,3%); krypton-82 (46 neutronen, 11,6%); krypton-83 (47 neutronen, 11,5%); krypton-80 (44 neutronen, 2,25%); en krypton-78 (42 neutronen, 0,35%)
Krypton kan ook bestaan als een onstabiele, radioactieve isotoop. Deze isotopen ontstaan tijdens kernreacties. Ongeveer 20 radioactieve isotopen van krypton zijn geproduceerd. Al deze isotopen behalve krypton-85 zijn zeer onstabiel, met halfwaardetijden van enkele uren of minder. (De halfwaardetijd van een radioactieve stof is de tijd die nodig is voor de helft van de atomen in een monster van de stof om radioactief verval te ondergaan.) Krypton-85, dat 36 protonen en 49 neutronen heeft, is veel stabieler, met een half -levensduur van 10,73 jaar.
Krypton wordt gebruikt met argon in fluorescentielampen om hun helderheid te verbeteren en met stikstof in gloeilampen om hun levensduur te verlengen. Het wordt ook gebruikt in flitslampen om gedurende een zeer korte tijd een zeer helder licht te produceren, voor gebruik bij hogesnelheidsfotografie. Radioactief krypton-85 kan worden gebruikt om kleine gebreken in metalen oppervlakken te lokaliseren. Het gas heeft de neiging zich op te hopen in deze gebreken en de radioactiviteit ervan kan worden gedetecteerd.
Geschiedenis
De edelgassen waren tot voor kort volledig onbekend voor de mensheid. De eerste aanwijzing van hun bestaan kwam in 1785, toen de Engelse chemicus Henry Cavendish ontdekte dat lucht een kleine hoeveelheid van een onbekende stof bevatte die minder reactief was dan stikstof. Tot het einde van de negentiende eeuw was er verder niets over deze stof bekend.
Ondertussen ontdekte de Britse astronoom Joseph Norman Lockyer in 1868 een nieuw element. Door het licht van de zon te analyseren, ontdekte hij een onbekend element dat hij helium noemde, van het Griekse woord helios (zon). Helium was al meer dan een kwart eeuw niet bekend op aarde.
In 1894, de Engelse natuurkundige Lord Rayleigh (John William Strutt) en de Schotse 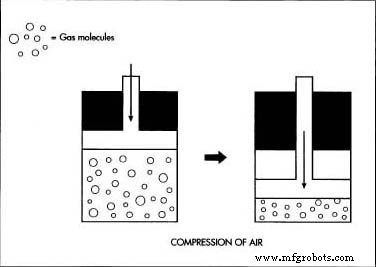 Gefilterde lucht wordt onder hoge druk gecomprimeerd, waardoor de temperatuur stijgt. De samengeperste lucht wordt vervolgens gecodeerd door snel uit te zetten in een kamer. Deze plotselinge uitzetting absorbeert warmte van de spoelen en koelt de perslucht af. Het proces van compressie en expansie wordt herhaald totdat de meeste gassen in de lucht zijn omgezet in vloeistoffen. scheikundige William Ramsay ontdekte een verschil in de dichtheid van stikstof uit de lucht en stikstof uit ammoniak. Ze ontdekten al snel dat de atmosferische stikstof was vermengd met een kleine hoeveelheid van een onbekende stof. Door magnesium te gebruiken om de stikstof te absorberen, konden ze de stof isoleren, die ze argon noemden, van het Griekse woord argos (inactief), omdat het niet reageerde met andere stoffen.
Gefilterde lucht wordt onder hoge druk gecomprimeerd, waardoor de temperatuur stijgt. De samengeperste lucht wordt vervolgens gecodeerd door snel uit te zetten in een kamer. Deze plotselinge uitzetting absorbeert warmte van de spoelen en koelt de perslucht af. Het proces van compressie en expansie wordt herhaald totdat de meeste gassen in de lucht zijn omgezet in vloeistoffen. scheikundige William Ramsay ontdekte een verschil in de dichtheid van stikstof uit de lucht en stikstof uit ammoniak. Ze ontdekten al snel dat de atmosferische stikstof was vermengd met een kleine hoeveelheid van een onbekende stof. Door magnesium te gebruiken om de stikstof te absorberen, konden ze de stof isoleren, die ze argon noemden, van het Griekse woord argos (inactief), omdat het niet reageerde met andere stoffen.
In 1895 ontdekten Ramsay en zijn assistent Morris William Travers dat het mineraal cleviet bij verhitting argon en helium afgaf. Dit was de eerste keer dat helium op aarde werd gedetecteerd. In 1898 haalden Ramsay en Travers drie nieuwe elementen uit lucht, die was afgekoeld tot een vloeistof. Ze noemden deze elementen krypton, van het Griekse woord kryptos (verborgen); neon, van het Griekse woord neos (nieuwe); en xenon, van het Griekse woord xenos (vreemd).
In 1900 merkte de Duitse chemicus Friedrich Dom op dat het radioactieve element radium helium en een onbekend radioactief gas vrijmaakte tijdens het verval. In 1910 bepaalden Ramsay en zijn assistent Robert Whytlaw-Gray de dichtheid van dit onbekende gas en noemden het niton, van het Latijnse woord nitere (om te glanzen), omdat het door zijn radioactiviteit gloeide als het werd afgekoeld tot een vloeistof. Niton, later bekend als radon, was het laatste edelgas dat werd ontdekt. In 1904 kreeg Ramsay de Nobelprijs voor Scheikunde voor zijn onderzoek naar edelgassen.
De edelgassen stonden vroeger bekend als de edelgassen of de inerte gassen. Later werd aangetoond dat sommige heel gewoon waren en dat sommige niet volledig onreactief waren. Helium is het op één na meest voorkomende element in het universum en argon vormt ongeveer 1% van de atmosfeer van de aarde. In 1962 creëerde Neil Bartlett xenon-platinahexafluoride, de eerste chemische verbinding van een edelgas. Verbindingen van radon werden in hetzelfde jaar gemaakt en verbindingen van krypton in 1963. Deze elementen werden niet langer als zeldzaam of inert beschouwd, maar werden bekend als de edelgassen. Net als de zogenaamde edele metalen (goud, zilver, platina, enz.), reageerden ze niet met zuurstof.
Krypton speelde een belangrijke rol in de wetenschap van 1960-1983, toen de lengte van de meter werd gedefinieerd als 1.650.763,73 keer de golflengte van het oranjerode licht dat door krypton-86 wordt uitgezonden. De meter werd later gedefinieerd in termen van de lichtsnelheid in een vacuüm, maar krypton wordt nog steeds gebruikt in wetenschappelijk onderzoek.
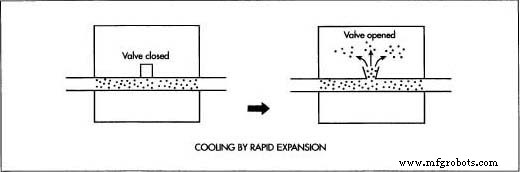 Om krypton, evenals de andere gassen, te scheiden van de vloeibare lucht, de lucht wordt langzaam opgewarmd in een proces dat gefractioneerde destillatie wordt genoemd. Werkend in de veronderstelling dat elke vloeistof zijn eigen specifieke temperatuur heeft waarbij deze in een gas verandert, scheidt gefractioneerde destillatie de gassen één voor één in de lucht.
Om krypton, evenals de andere gassen, te scheiden van de vloeibare lucht, de lucht wordt langzaam opgewarmd in een proces dat gefractioneerde destillatie wordt genoemd. Werkend in de veronderstelling dat elke vloeistof zijn eigen specifieke temperatuur heeft waarbij deze in een gas verandert, scheidt gefractioneerde destillatie de gassen één voor één in de lucht.
Ruwe Mcateials
Hoewel sporen van krypton in verschillende mineralen worden gevonden, is de belangrijkste bron van krypton de atmosfeer van de aarde. Lucht is ook de belangrijkste bron voor de andere edelgassen, met uitzondering van helium (verkregen uit aardgas) en radon (verkregen als bijproduct van het verval van radioactieve elementen). Op zeeniveau bevat droge lucht 78,08% stikstof en 20,95% zuurstof. Het bevat ook 0,93% argon, 0,0018% neon, 0,00052% helium, 0,00011% krypton en 0,0000087% xenon. Andere componenten van droge lucht zijn onder meer koolstofdioxide, waterstof, methaan, stikstofmonoxide en ozon.
Krypton kan ook worden verkregen uit de splijting van uranium, die voorkomt in kerncentrales. In tegenstelling tot lucht, die alleen de stabiele isotopen van krypton bevat, produceert dit proces zowel stabiele isotopen als radioactieve isotopen van krypton.
Het fabricageproces
Vloeibare lucht maken
- 1 Lucht wordt eerst door filters geleid om fijnstof zoals stof te verwijderen. De schone lucht wordt vervolgens blootgesteld aan een alkali (een sterk basische stof), die water en kooldioxide verwijdert.
- 2 De schone, droge lucht wordt onder hoge druk gecomprimeerd. Omdat compressie de temperatuur van de lucht verhoogt, wordt deze vervolgens gekoeld door koeling.
- 3 De gekoelde, gecomprimeerde lucht gaat door spoelen die door een lege kamer wikkelen. Een deel van de lucht, die wordt samengeperst tot een druk die ongeveer tweehonderd keer groter is dan normaal, mag uitzetten in de kamer. Deze plotselinge uitzetting absorbeert warmte van de spoelen en koelt de perslucht af. Het proces van compressie en expansie wordt herhaald totdat de lucht is afgekoeld tot een temperatuur van ongeveer -321 F (-196 ° C), waarna de meeste gassen in de lucht worden omgezet in vloeistoffen.
De gassen scheiden
- 4 Gassen met zeer lage kookpunten worden niet omgezet in vloeistoffen en kunnen direct van de andere worden verwijderd. Deze gassen omvatten helium, waterstof en neon.
- 5 Een proces dat fractionele destillatie wordt genoemd, scheidt de verschillende elementen die in vloeibare lucht worden aangetroffen. Dit proces is gebaseerd op het feit dat de verschillende stoffen bij verschillende temperaturen van vloeistof naar gas zullen worden omgezet.
- 6 De vloeibare lucht mag langzaam opwarmen. Naarmate de temperatuur stijgt, worden de stoffen met de laagste kookpunten gassen en kunnen ze uit de resterende vloeistof worden verwijderd. Argon, zuurstof en stikstof zijn de eerste stoffen die worden omgezet in gassen als de vloeibare lucht opwarmt. Krypton en xenon hebben hogere kookpunten en blijven in vloeibare toestand wanneer de andere componenten van lucht gassen zijn geworden.
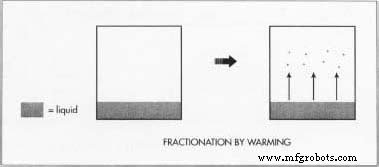
Krypton scheiden van xenon
- 7 De vloeibare krypton en xenon worden geabsorbeerd op silicagel of op actieve kool. Vervolgens worden ze opnieuw onderworpen aan gefractioneerde destillatie. Het vloeibare mengsel wordt langzaam verwarmd totdat het krypton in een gas is omgezet. Het xenon heeft een wat hoger kookpunt en blijft als vloeistof achter.
- 8 Het krypton wordt gezuiverd door het over heet titaniummetaal te leiden. Deze stof heeft de neiging om alle elementen te verwijderen, behalve edelgassen.
Het scheiden van de isotopen van krypton
- 9 Voor de meeste doeleinden is de krypton nu klaar om te worden verpakt. Voor sommige wetenschappelijke doeleinden is echter slechts één van de zes stabiele isotopen van krypton gewenst. Om deze isotopen te scheiden, wordt een proces gebruikt dat bekend staat als thermische diffusie. Dit proces hangt af van het feit dat de isotopen iets verschillende dichtheden hebben.
- 10 Het kryptongas wordt in een lange verticale glazen buis geplaatst. Een verwarmde draad loopt verticaal door het midden van deze buis. De hete draad zorgt voor een convectiestroom in de buis. Deze stroom van hete lucht heeft de neiging om de lichtere isotopen naar de bovenkant van de buis te dragen, waar ze kunnen worden verwijderd.
Verpakking en verzending
- 11 Kryptongas is verpakt in bollen van sterk glas zoals Pyrex bij normale druk of in stalen jerrycans onder hoge druk. Omdat het een zeer niet-reactieve stof is, is krypton zeer veilig. Het is niet-toxisch, niet-explosief en niet-ontvlambaar, dus het vereist geen ongebruikelijke voorzorgsmaatregelen tijdens verzending.
Kwaliteitscontrole
De belangrijkste factor bij de kwaliteitscontrole van de kryptonproductie is ervoor te zorgen dat het eindproduct alleen krypton bevat. Het proces van fractiedestillatie is zo ontwikkeld dat het zeer zuivere producten uit lucht produceert, waaronder krypton.
Willekeurige monsters van krypton worden getest op zuiverheid door spectroscopische analyse. Dit proces omvat het verhitten van een stof totdat deze licht uitstraalt. Het licht gaat dan door een prisma of een rooster om een spectrum te produceren, op dezelfde manier als zonlicht een regenboog produceert. Spectroscopische analyse is bijzonder geschikt voor het bestuderen van gassen, omdat verwarmde gassen de neiging hebben scherpe, heldere lijnen te produceren op een spectrum van pure krypton, het is mogelijk om te zien of er onzuiverheden aanwezig zijn.
Bijproducten/afval
Krypton is slechts een van de vele waardevolle elementen die worden geproduceerd door de gefractioneerde destillatie van vloeibare lucht. Meer dan driekwart van de lucht bestaat uit stikstof. Stikstof wordt gebruikt om een breed scala aan chemische verbindingen te produceren, met name ammoniak. Omdat het veel minder reactief is dan zuurstof, wordt stikstof gebruikt om veel stoffen te beschermen tegen oxidatie. Vloeibare stikstof wordt gebruikt bij vriesdrogen en koelen.
Ongeveer een vijfde van lucht bestaat uit zuurstof. De staalindustrie is de grootste verbruiker van zuivere zuurstof. Zuurstof wordt gebruikt om overtollig koolstof uit staal te verwijderen in de vorm van koolstofdioxide. Zuurstof wordt ook gebruikt om afvalwater te zuiveren en vast afval te verbranden. Vloeibare zuurstof wordt gebruikt als raketbrandstof.
De edelgassen die worden verkregen uit andere lucht dan krypton zijn argon, neon en xenon. Argon wordt gebruikt in bepaalde soorten gloeilampen. Door een elektrische stroom door een glazen buis met neon onder lage druk te leiden, ontstaat het bekende neonbord. Xenon wordt gebruikt in stroboscooplampen om intense, korte lichtflitsen te produceren.
De Toekomst
De toekomstige productie van krypton zal waarschijnlijk worden beïnvloed door de toekomst van de productie van kernenergie. Omdat krypton kan worden geproduceerd als een bijproduct van kernsplijting, kunnen kerncentrales in de toekomst een belangrijke bron van krypton worden. Aan de andere kant, als kernsplijting grotendeels wordt vervangen door kernfusie of door andere vormen van energieproductie, zal krypton waarschijnlijk bijna volledig een product van de atmosfeer blijven.
Productieproces
- Wat is VMC-bewerking?
- Gids voor aluminium lasermarkering
- MIG-lassen versus TIG-lassen
- Gids voor lasermarkering
- Overwegingen voor Zwitserse machinale bewerking met hoge productie
- Gids voor CNC-prototyping
- Het fabricageproces van de schacht begrijpen
- Wat is fiberlasermarkering?
- Elektrolytisch polijsten versus passiveren
- Wat is RVS-passivering?
- Hoe u vistuig ontwerpt en bouwt in bedrijfstijd



