Eerste-principes onderzoek van adsorptiegedrag van kleine moleculen op penta-grafeen
Abstract
Het gasadsorptiegedrag van kleine moleculen CO, H2 O, H2 S, NH3 , SO2 , en NO op ongerept penta-grafeen (PG) werden onderzocht met behulp van eerste-principeberekeningen om hun potentieel voor gebruik als geavanceerde gasdetectiematerialen te onderzoeken. Resultaten laten zien dat, behalve voor CO, H2 O, H2 S, NH3 , en SO2 worden fysiek geadsorbeerd op het oppervlak van penta-grafeen met aanzienlijke adsorptie-energie en matige ladingsoverdracht, terwijl NO de neiging heeft om chemisch te worden geadsorbeerd op het oppervlak van penta-grafeen. Bovendien kunnen de elektronische eigenschappen van PG effectief worden gewijzigd na H2 O, H2 S, NH3 , SO2 , en NO worden geadsorbeerd, en penta-grafeen heeft potentieel voor gebruik in gassensoren via het ladingsoverdrachtsmechanisme.
Achtergrond
Gasdetectie, met name de detectie van vervuild of giftig gas, is altijd een focus geweest van onderzoek in verband met toepassingen op het gebied van monitoring van milieuvervuiling, industriële controle, landbouwproductie en medische diagnose [1]. De laatste tijd zijn er steeds meer tweedimensionale materialen voorspeld en gesynthetiseerd [2,3,4]. Tweedimensionale materialen zijn uitgebreid onderzocht en gebruikt als gasgevoelige elementen omdat ze fascinerende eigenschappen vertonen, zoals een groot oppervlak, ultrahoge mobiliteit van de drager en lage elektrische ruis [5]. Er is gemeld dat de elektronische eigenschappen van tweedimensionale materialen kunnen worden veranderd nadat bepaalde specifieke gasmoleculen erop zijn geadsorbeerd [6, 7].
Onder tweedimensionale materialen hebben met name grafeen en zijn analogen de aandacht getrokken vanwege hun opmerkelijke fysieke eigenschappen en potentieel voor toepassingen in zowel nano-elektronica als nanomechanica [8,9,10,11,12]. Hoewel grafeen algemeen wordt beschouwd als een van de meest geschikte gastheermaterialen voor elektronische apparaten van de volgende generatie [13], is de stabiele sp 2 hybridisatie van koolstofbindingen en zero-gap karakter maken het inefficiënt voor gasadsorptie, wat nadelig is voor het ontwerp van gassensoren. Bovendien is grafeen een geleider met een uitstekende elektrische geleidbaarheid [8]. In vergelijking met halfgeleiders is het moeilijk om de weerstandsinformatie te meten tijdens het proces van gasadsorptie en grafeen is ongevoelig voor de concentratievariaties van gassen. Grafeen moet dus worden gefunctionaliseerd om de band gap te openen en als halfgeleider te werken [10]. Voor de beperking van experimentele karakterisering is het adsorptiegedrag van moleculen op het oppervlak van grafeen uitgebreid onderzocht door middel van eerste-principes berekeningen, die van belang zijn voor de toepassing van grafeen [14,15,16].
Penta-grafeen (PG), dat kan worden geëxfolieerd uit bulk T12-koolstof, is een van de meest recent voorgestelde grafeenallotropen en bestaat uit herhalende koolstof-pentagonstructuren [17]. Sommige onderzoeken hebben voorspeld dat PG stabiel is met vaste roosterconstanten [17, 18]. Het heeft een honingraatstructuur en is een veelbelovende metaalvrije, goedkope katalysator voor CO-oxidatie bij lage temperatuur [19]. Met stikstof gedoteerd PG vertoont een zeer hoge katalytische activiteit en is competitiever met veel op metaal gebaseerde en op koolstof gebaseerde katalysatoren voor CO-oxidatie bij lage temperatuur vanwege de zeer kleine energiebarrière van de snelheidsbeperkende stap [20]. Er is ook gemeld dat met overgangsmetaal gedoteerd PG een potentieel waterstofopslagmateriaal is [21]. Bovendien is PG, in tegenstelling tot grafeen, een intrinsieke quasi-direct-band-gap halfgeleider met een bandgap in het bereik van 1,52-4,48 eV [8, 17, 22], wat een enorm potentieel voor toepassing in halfgeleidergassensoren impliceert. Bovendien heeft PG een unieke hybride obligatiestructuur die zowel sp 3 en sp 2 koolstof bindingen. Door het tetraëdrische karakter van de sp 3 hybridisatie van koolstofbindingen, PG is niet ideaal vlak, maar oscilleert eerder uit het vlak op een periodieke gegolfde manier [17], wat wijst op meer mogelijke posities voor gasadsorptie als een detectie-element.
Onderzoeken naar de interactie tussen kleine gasmoleculen en ongerept PG waren tot nu toe schaars. Vanwege de beperking van experimentele methoden werden in deze studie dichtheidsfunctionaaltheorie (DFT) -berekeningen uitgevoerd om het adsorptiegedrag van kleine gasmoleculen (d.w.z. CO, H2) te onderzoeken. O, H2 S, NH3 , SO2 , en NO) op het nieuwe koolstofmateriaal PG. Dit onderzoek zal werknemers helpen bij het analyseren en voorspellen van de prestaties van PG toegepast in gassensoren.
Methoden
In deze studie werden de berekeningen van structurele optimalisaties uitgevoerd door eerste-principeberekeningen op basis van DFT [23] zoals geïmplementeerd in Dmol 3 code [24]. Er wordt verondersteld dat de lokale dichtheidsbenadering (LDA) gunstig is voor het bestuderen van gas-molecuul-adsorptiesystemen [25, 26], en de LDA-PWC werd geselecteerd voor de structurele optimalisaties in dit onderzoek. Om te voorkomen dat de van der Waals-interacties in de studie van gas-molecuul-adsorptie worden verwaarloosd, werd de methode van Ortmann, Bechstedt en Schmidt [27] gebruikt. De 2 × 2 × 1 Monkhorst-Pack mesh [28] werd gebruikt voor de Brillouin-zone integratie, waarbij de zelfconsistente veldtolerantie werd ingesteld op 1 × 10 − 5 Ha. Het systeem zou de grondtoestand bereiken wanneer de convergentieprecisie van energie voor de maximale energieverandering, de maximale kracht en de maximale verplaatsing 1 × 10 − 5 was Ha, respectievelijk 0,002 Ha/Å en 0,005 Å. Multi-core parallel computing werd uitgevoerd [29] en spinpolarisatie werd toegepast bij de berekeningen van de adsorptie van NO. Een 3 × 3 supercel met een vacuümruimte van 30 Å [21] werd gemodelleerd op basis van de eenheidscel met twee sp 3 -gehybridiseerde koolstof (C1) atomen en vier sp 2 -gehybridiseerde koolstofatomen (C2) [17], zie Fig. 1, waar C1- en C2-atomen worden onderscheiden als respectievelijk zwarte en grijze bollen. Gasmoleculen bevonden zich horizontaal ten opzichte van het substraat op een initiële afstand van 3,5 . Om de meest gunstige adsorptieposities van de gasmoleculen te verkrijgen, zijn vier mogelijke locaties onderzocht, namelijk de bovenkant van het C1-atoom (T1), de bovenkant van het C2-atoom (T2), het midden van de groeven in PG (T3 ), en de tegenovergestelde positie van T2 (T4 ), zoals weergegeven in Afb. 1.
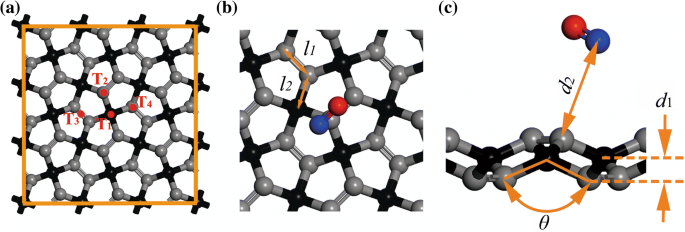
Structuur en geometrie van PG:a 3 × 3 supercel, b vooraanzicht van eenheidscel, en c zijaanzicht van de adsorbaat-PG-atomen. De afstand tussen twee C2-atomen, de afstand tussen C1- en C2-atomen, de dikte van PG en de C2-C1-C2-engel worden gedefinieerd als l 1 , l 2 , d 1 , en θ , respectievelijk
Om het adsorptievermogen van het systeem kwantitatief te evalueren, wordt naast LDA-PWC ook adsorptie-energie (E een ), overboeking (Q ), en adsorptieafstand (d 2 , zoals geïllustreerd in Fig. 1) werden berekend met behulp van de gegeneraliseerde gradiëntbenadering (GGA) -functionaliteiten met Perdew-Wang 1991 (PW91) en Perdew-Burke-Ernzerh (PBE) in het onderzoek. d 2 wordt gedefinieerd als de dichtstbijzijnde atomaire afstand tussen de PG en het gasmolecuul in de evenwichtstoestand. V geeft de Mulliken-lading van het gasmolecuul [30, 31] aan, en een negatieve waarde betekent ladingsoverdracht van PG naar het gasmolecuul. De adsorptie-energie wordt berekend door
$$ {E}_a\kern0.5em =\kern0.5em {E}_{\left(\mathrm{PG}\kern0.5em +\kern0.5em \mathrm{molecuul}\right)}\kern0.5em -\kern0.5em {E}_{\mathrm{PG}}\kern0.5em -\kern0.5em {E}_{\mathrm{molecuul}}, $$ (1)waar E (PG + molecuul) , E PG , en E molecuul zijn de totale energieën van respectievelijk het adsorbaat-PG-evenwichtssysteem, het geïsoleerde PG en het geïsoleerde gasmolecuul. Bij de berekeningen van elektronische structuren van de adsorptiesystemen zijn de DFT-berekeningen met behulp van de PBE-uitwisselingscorrelatiefunctie met de GGA gebruikt voor een hogere nauwkeurigheid [2, 32].
Resultaten en discussie
Na structurele optimalisatie zijn de berekende structurele parameters van ongerepte PG gerapporteerd in dit artikel (l 1 = 1.342 Å, l 2 = 1.551 Å, θ = 133,9°, d 1 = 0.612 Å) bleken consistent te zijn met die van eerder werk [17]. Door de laagste E . te selecteren (PG + molecuul) of E een op de vier adsorptieposities T1 tot T4 (zie tabel S1 van aanvullend bestand 1), zijn de gunstigste adsorptieconfiguraties voor gassen op monolaag-PG uitgezet in figuur 2 en de gunstigste adsorptieposities (d.w.z. T1 , T2 , T3 , of T4 ) staan vermeld in Tabel 1. De berekende resultaten in de volgende tekst zijn verkregen op basis van deze gunstigste adsorptieconfiguraties. Recente studies hebben aangetoond dat monolaag InSe, grafeen en blauwe fosfor veelbelovend zijn voor gebruik in gassensoren [14, 33, 34]. In de huidige studie is de berekende E een waarden van CO, H2 O, en NH3 zijn respectievelijk − 0,531, − 0,900 en − 1,069 eV (zie tabel 1), terwijl ze respectievelijk − 0,120, − 0,173 en − 0,185 eV zijn voor InSe [33]. Voor CO, H2 O, NH3 , en NO op het oppervlak van grafeen, de berekende E een waarden zijn respectievelijk − 0.014, − 0.047, − 0.031 en − 0.029 eV [14]. Ondertussen, E een waarden voor H2 S en SO2 gassen op PG zijn respectievelijk − 1.345 en − 1.212 eV, wat veel groter is dan respectievelijk − 0.14 en − 0.20 eV voor blauwe fosfor [34]. Het is duidelijk dat de berekende E een waarden van deze gasmoleculen op PG zijn veel groter dan deze verkregen uit de andere materialen, wat aangeeft dat deze gasmoleculen gemakkelijk kunnen worden geadsorbeerd op het oppervlak van PG [35]. Aangezien de berekende E een waarde van CO veel kleiner is dan die van andere gassen, kan de adsorptie van CO de zwakste zijn. Ondertussen is de adsorptie-energie van NO in Tabel 1 kleiner dan die van sommige van die gefysisorbeerde (niet-covalente) adsorbaten, zoals H2 S, NH3 , en SO2 . Dit kan worden verklaard door de reden dat, anders dan bij fysieke adsorptie, de chemische adsorptie van NO duidelijke vervorming van PG induceert, wat extra energie verbruikt en de berekende adsorptie-energie vermindert E een , zoals geïntroduceerd in aanvullend bestand 1. Evenzo kan duidelijke vervorming ook worden waargenomen bij de chemische adsorptie van NO2 op het oppervlak van antimoneen [5], wat kan resulteren in de relatief lage adsorptie-energie. Verder, behalve voor NO, zijn de waarden van d 2 vermeld in Tabel 1 zijn duidelijk groter dan de som van de covalente stralen van het overeenkomstige atoom in het gasmolecuul en het C-atoom in de PG (d.w.z. l C-O = 1.38 Å, l C-H = 1,07 Å, l C-N = 1.46 Å, l C-S = 1.78 Å) [36], waaruit blijkt dat deze gasmoleculen de neiging hebben om fysiek te worden geadsorbeerd. Wat betreft NO, de waarde van d 2 in het adsorptiesysteem is 1,541 Å, wat in het bereik van covalente bindingen ligt, wat aangeeft dat er in dit geval chemische bindingen kunnen bestaan.
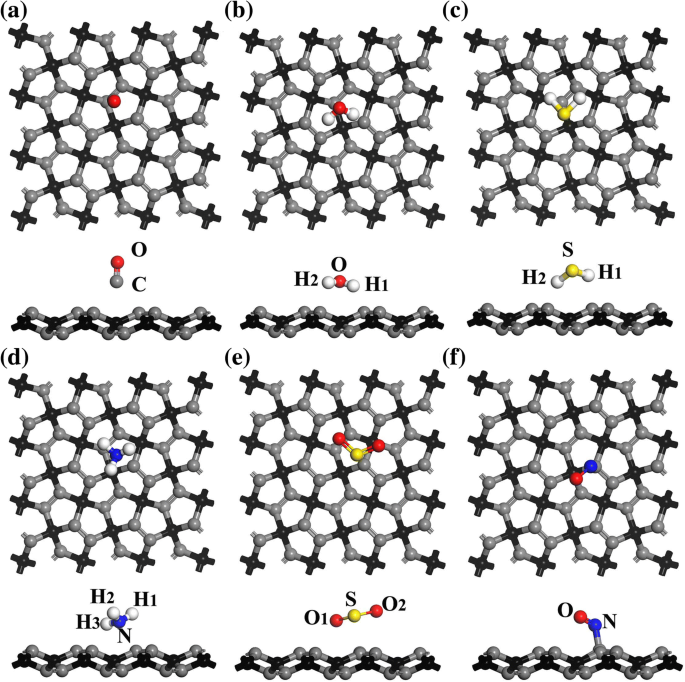
Boven- en zijaanzichten van de gunstigste adsorptieconfiguraties voor a CO, b H2 O, c H2 S, d NH3 , e SO2 , en f NEE op PG. De grijze, rode, witte, gele en blauwe bollen vertegenwoordigen respectievelijk C-, O-, H-, S- en N-atomen
Eerdere onderzoeken naar InSe en boorfosfide hebben aangetoond dat geadsorbeerde moleculen de soortelijke weerstand van het substraat veranderen door als ladingsacceptors of donoren te fungeren [33, 37]. De Q waarden voor CO, H2 O, H2 S, NH3 , SO2 , en NO op het oppervlak van PG zijn respectievelijk 0,023, 0,082, 0,133, 0,169, -0,109 en -0,03 e (zie tabel 1), wat aangeeft dat gassen van CO, H2 O, H2 S en NH3 doneer elektronen aan PG terwijl SO2 en NO verkrijgt elektronen van PG. Het is vermeldenswaard dat de Q waarden van CO, H2 O, NH3 , en NO op het oppervlak van InSe zijn respectievelijk 0,006, 0,014, -0,025 en 0,018 e [33], en die voor CO, H2 O, NH3 , en NO op het oppervlak van grafeen zijn respectievelijk 0,012, -0,025, 0,027 en 0,018 e [14], wat aangeeft dat de winst of het verlies van elektronen van de gasmoleculen op PG duidelijker is dan die op InSe en grafeen. Bovendien, hoewel chemische adsorptie kan optreden tussen NO en PG, is de ladingsoverdracht slechts − 0.030 e. Dit kan worden verklaard door het feit dat de Mulliken-ladingsverdelingen van N- en O-atomen behoorlijk verschillend zijn (zie tabel S2 in aanvullend bestand 1) voor en na chemische adsorptie. De versterkingselektronen van het O-atoom compenseren de verlieselektronen van het N-atoom, waardoor de totale ladingsoverdracht van NO niet groot is, terwijl de interactie van elektronen tussen NO en PG nog steeds duidelijk is. Volgens het detectiemechanisme van ladingsoverdracht van kleine gasmoleculen op het oppervlak van InSe en InN [33, 38], wordt gespeculeerd dat PG een groot potentieel heeft voor gebruik in gassensoren op basis van het ladingsoverdrachtsmechanisme.
Verder werden ook berekeningen van de gasadsorptie op PG uitgevoerd met behulp van twee GGA-functionals, PW91 en PBE. De berekende waarden van E een , V , en d voor gasmoleculen op PG staan vermeld in tabel 2. De E een waarden berekend door PW91 en PBE zijn kleiner dan die berekend door de LDA, terwijl zowel PW91 als PBE een grotere d geven 2 vergeleken met de LDA. Anders dan de LDA, heeft de GGA meestal de neiging om de adsorptie-energie te onderschatten en de bindingsafstand te overschatten, wat consistent is met de resultaten van eerdere werken [26, 31]. Het is vermeldenswaard dat de tendensen van de resultaten van deze drie functionalen consistent zijn. Bijvoorbeeld, de berekende waarden van E een van CO het kleinst zijn, en de berekende waarden van E een van H2 S en SO2 groter zijn dan die van andere gasmoleculen. Bovendien zijn de berekende waarden van d 2 van NO voor de LDA-, PW91- en PBE-functionaliteiten zijn respectievelijk 1.514, 1.592 en 1.591 Å, die allemaal in het covalente bindingsbereik liggen [36].
Om een beter begrip te krijgen van de invloed van gasmoleculen op de elektronische eigenschappen van PG, werd de staatsdichtheid (DOS) van het molecuul-PG-systeem berekend, zie Fig. 3. Uiteraard nabij het Fermi-niveau (E f , bijvoorbeeld in het bereik van -2,5 tot 2,5 eV), zijn er duidelijke bijdragen van de elektronische niveaus van H2 O, H2 S, NH3 , SO2 , en NEE tegen de adsorptiesystemen, wat aangeeft dat het bestaan van deze gasmoleculen een grote invloed kan hebben op de elektronische eigenschappen van PG [5, 37]. Bijvoorbeeld voor H2 S, een schijnbare bijdrage van elektronische niveaus bevindt zich op 0 eV; zie afb. 3c. Wat betreft CO op het oppervlak van PG, de orbitale pieken van CO in het adsorptiesysteem bevinden zich op -8,0, -5,7, -2,9 en 4,0 eV, en er is geen duidelijke orbitale bijdrage in de buurt van E f . Bovendien is band gap ook een kritische factor bij het bepalen van de elektronische eigenschappen van materialen [26, 34].
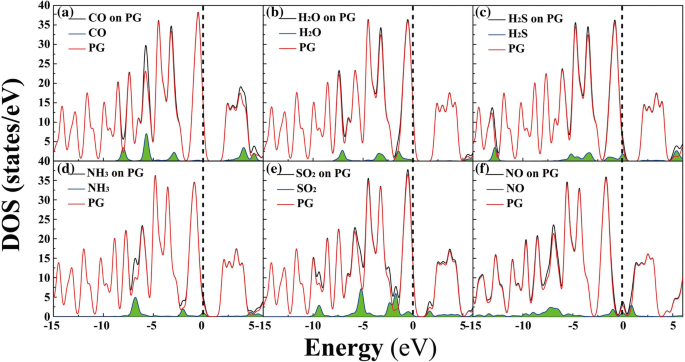
Totale elektronische toestandsdichtheid (DOS) voor molecuul-PG-systemen (zwart), en geprojecteerde DOS voor kleine moleculen (blauwe lijn met groene schaduw) en PG (rood) in het adsorptiesysteem:a CO, b H2 O, c H2 S, d NH3 , e SO2 , en f NEE. Het Fermi-niveau staat op nul (zie de streepjeslijn)
De bandhiaten en bijbehorende bandstructuren van de adsorptiesystemen worden getoond in Fig. 4, waar de bandhiaten van CO, H2 O, H2 S, NH3 , SO2 , en NO op PG zijn respectievelijk 2,15, 2,02, 1,86, 1,81, 1,61 en 0 eV. Als contrast is de band gap van ongerepte PG 2,21 eV (zie aanvullend bestand 1:figuur S2). Het is duidelijk dat, behalve voor CO, de gasadsorpties van H2 O, H2 S, NH3 , SO2 , en NO hebben een duidelijke invloed op de elektronische eigenschappen van PG, en deze zijn consistent met de resultaten van DOS. Al deze resultaten kunnen erop wijzen dat, behalve voor CO, de elektronische eigenschappen van PG effectief kunnen worden gewijzigd na H2 O, H2 S, NH3 , SO2 , en NO worden geadsorbeerd, wat essentieel is voor gasdetectie.
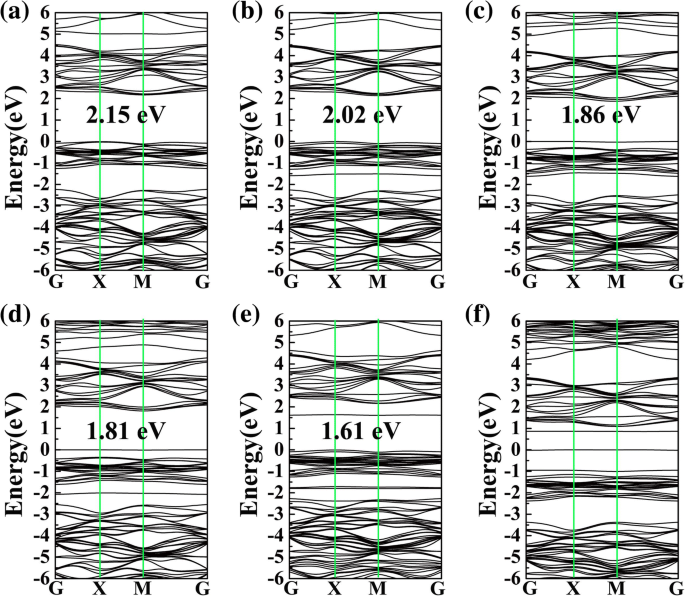
Bandstructuren van CO (a ), H2 O (b ), H2 S (c ), NH3 (d ), SO2 (e ), en NEE (f ) op het oppervlak van PG
Aangezien de d 2 waarde van NO op PG in het bindingsbereik ligt en dat de elektronische niveaus van NO in het systeem zich voornamelijk rond E bevinden f , wordt gespeculeerd dat er een chemische adsorptie optreedt. Op weg naar een diep begrip van het adsorptiemechanisme tussen NO en PG, zijn de geprojecteerde toestandsdichtheid (PDOS) van NO op PG en de elektronenlokalisatiefunctie (ELF) uitgezet in Fig. 5. Het is duidelijk dat de pieken van de PDOS van N p en O p atomen bevinden zich voornamelijk op -6,9, -0,9, 0 en 0,8 eV; er is dus een intra-molecuulhybridisatie in NO, zoals getoond in Fig. 5a. Ondertussen kan orbitale vermenging tussen NO en het C-atoom van PG nabij het Fermi-niveau worden waargenomen, wat voornamelijk wordt bijgedragen door de C s , C p , N s , N p , en O p orbitalen. De orbitale menging induceert een chemische binding tussen N in NO en C in PG, zoals weergegeven in figuur 5b; PG kan dus worden gebruikt voor het detecteren of katalyseren van NO-gas [5, 39]. Verder worden, om het adsorptietype van andere gasmoleculen te bevestigen, ook ELF's van andere adsorptiesystemen berekend, zie aanvullend bestand 1:figuur S3. Vanzelfsprekend, voor CO, H2 O, H2 S, NH3 en SO2 , zijn er geen chemische bindingen tussen de gasmoleculen en het substraat, wat aangeeft dat de systemen een neiging hebben tot fysieke adsorptie.
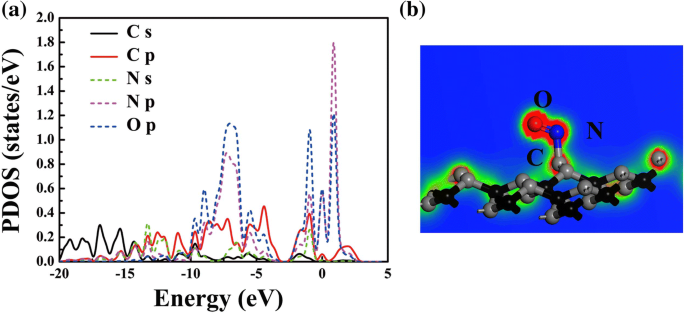
Het atoom geprojecteerde DOS (a ) en elektronenlokalisatiefunctie (ELF) van NO-PG (b )
Conclusies
Samengevat, H2 O, H2 S, NH3 , en SO2 gassen worden fysiek geadsorbeerd op monolaag PG met aanzienlijke adsorptie-energie en matige ladingsoverdracht. Voor zwakke fysieke adsorptie, kleine adsorptie-energie en ladingsoverdracht is ongerept PG niet geschikt voor het detecteren van CO. Voor deze gasmoleculen op het oppervlak van PG, CO, H2 O en H2 S en NH3 elektronen doneren aan PG, terwijl SO2 en NO verkrijgt elektronen van PG. Bovendien zijn er in de buurt van het Fermi-niveau duidelijke bijdragen van de elektronische niveaus van H2 O, H2 S, NH3 , SO2 , en NEE tegen de DOS van de adsorptiesystemen, wat aangeeft dat de elektronische eigenschappen van PG effectief kunnen worden gewijzigd na H2 O, H2 S, NH3 , SO2 , en NO worden geadsorbeerd. Bovendien vertoont de adsorptie van NO op PG een sterke neiging tot chemische adsorptie, en dus kan PG worden gebruikt voor het detecteren of katalyseren van NO-gas. Ongerepte PG heeft daarom een groot potentieel in gasdetectietoepassingen.
Afkortingen
- 2D:
-
Tweedimensionaal
- DFT:
-
Dichtheidsfunctionaaltheorie
- DOS:
-
Dichtheid van staten
- ELF:
-
Elektronenlokalisatiefunctie
- GGA:
-
Gegeneraliseerde gradiëntbenadering
- LDA:
-
Benadering van lokale dichtheid
- PBE:
-
Perdew–Burke–Ernzerh
- PDOS:
-
Geprojecteerde dichtheid van toestanden
- PG:
-
Penta-grafeen
- PW91:
-
De Perdew-Wang 1991
- PWC:
-
Perdew–Wang-correlatie
Nanomaterialen



