Synthese van sferisch zilver-gecoat Li4Ti5O12 anodemateriaal door een Sol-Gel-ondersteunde hydrothermische methode
Abstract
ᅟ
Ag-gecoate sferische Li4 Ti5 O12 composiet werd met succes gesynthetiseerd via een sol-gel-geassisteerde hydrothermische methode met behulp van een mengsel van ethyleenglycol en zilvernitraat als voorloper, en de invloed van de Ag-coatinginhoud op de elektrochemische eigenschappen ervan werd uitgebreid onderzocht. Röntgendiffractie (XRD) analyse gaf aan dat de Ag-coating de spinelstructuur van Li4 niet verandert Ti5 O12 . De elektrochemische impedantiespectroscopie (EIS) analyses toonden aan dat de uitstekende elektrische geleidbaarheid van de Li4 Ti5 O12 /Ag was het gevolg van de aanwezigheid van de sterk geleidende zilvercoatinglaag. Bovendien verbeterde de nanodikke zilverlaag, die gelijkmatig op de deeltjes was aangebracht, de snelheid van dit materiaal aanzienlijk. Als gevolg hiervan is de met zilver beklede bolvormige Li4 Ti5 O12 vertoonde uitstekende elektrochemische prestaties. Met een geschikt zilvergehalte van 5 gew.% is de Li4 Ti5 O12 /Ag leverde de hoogste capaciteit van 186,34 mAh g −1 bij 0,5C, wat hoger is dan die van andere monsters, en behield 92,69% van zijn initiële capaciteit bij 5C na 100 cycli. Zelfs bij 10C na 100 cycli had het nog steeds een capaciteitsbehoud van 89,17%, wat een opmerkelijke cyclusstabiliteit aantoont.
Proefregistratie
ISRCTN NARL-D-17-00568
Hoogtepunten
- 1.
Sferische Li4 Ti5 O12 /Ag-composieten werden gesynthetiseerd via een sol-gel-ondersteunde hydrothermische methode met behulp van ethyleenglycol en een zilvernitraatmengsel als de voorloper voor de coatinglaag, wat de elektronische geleidbaarheid en de elektrochemische prestatie van Li4 aanzienlijk verbeterde. Ti5 O12 .
- 2.
De bolvormige morfologie zou een grote tapdichtheid kunnen induceren en bijgevolg de volumetrische energiedichtheid kunnen verbeteren.
Achtergrond
In de afgelopen tien jaar hebben oplaadbare lithium-ionbatterijen (LIB's) veel voordelen laten zien. Ze zijn licht van gewicht; een klein formaat, hoge spanning en hoge energiedichtheid hebben; en hebben grote belangstelling gewekt als een elektrochemisch energieopslagapparaat om uitlaatemissies te verminderen en voor brandstofbesparing [1, 2]. De prijs van lithiumprecursoren, veiligheids- en levensproblemen en een lage vermogensdichtheid zijn echter obstakels voor de toepassing van LIB's voor grootschalige energieopslag in de toekomst [3]. Daarom zijn er grote inspanningen geleverd om vervangende materialen te ontwikkelen om te voldoen aan de eisen van de veiligheid van de grootschalige opslag [4].
Cube spinel lithiumtitanaat (Li4 Ti5 O12 ) materialen, de anodematerialen van Li-ionbatterijen, zijn een veelbelovend materiaal geworden vanwege hun structurele karakteristiek zonder spanning tijdens het intercalatie- en de-intercalatieproces van Li4 Ti5 O12 [5,6,7,8,9]. Dit materiaal heeft een lithium-invoeg- en extractievoltage van ~ 1,55 V (vs. Li/Li + ), waardoor de vorming van lithiumverbruikende vaste elektrolytinterface (SEI) -films wordt vermeden, wat gunstig zou moeten zijn voor het verbeteren van de veiligheid en goede cycli van de LIB's. Daarom, Li4 Ti5 O12 is uitgegroeid tot een van de potentiële materialen in commerciële toepassingen en wetenschappelijk onderzoek. Li4 Ti5 O12 is bereid via verschillende methoden, bijvoorbeeld vaste toestand, stroomloze afzetting, magnetron en sol-gel-methode. Met betrekking tot de vastestofmethode hebben sommige onderzoeken aangetoond dat deze een eenvoudige syntheseroute en lage synthesekosten heeft vanwege de kortere afstand voor Li + diffusie en elektronenoverdracht, Li4 Ti5 O12 vertoont een uitstekend snelheidsvermogen, maar de reactie in vaste toestand kan geen uniforme morfologie met een smalle grootte opleveren. Het stroomloze depositieproces heeft echter een complexe syntheseroute. Voor de sol-gel-synthese van Li4 Ti5 O12 , hebben verschillende onderzoekers gemeld dat het producten kan opleveren met een uniform homogene verdeling en smalle deeltjes met een goede stoichiometrische controle.
Ondanks deze vele voordelen, zijn de belangrijkste nadelen van Li4 Ti5 O12 zijn de slechte elektronische en ionische geleidbaarheid en de trage Li-ion-diffusiecoëfficiënt, wat resulteert in een slechte snelheidscapaciteit. Talrijke strategieën, waaronder vermindering van de kristallietgrootte [10], dotering met metaalionen met hoge valentie [11,12,13] en coating met geleidende fasen [14,15,16,17], zijn toegepast om het ontladings- / ladingstransport te verbeteren eigenschappen van elektroden. Daarnaast is een andere manier om de elektronische geleidbaarheid te verbeteren het synthetiseren van nanogestructureerde Li4 Ti5 O12 . De nanostructuren zorgen voor een groter elektrode/elektrolyt contactoppervlak om de intercalatiekinetiek te vergroten en de diffusiepaden te verminderen om Li + te versnellen en elektronentransport [18]. Van deze benaderingen is de meest effectieve manier om de elektrochemische eigenschappen van Li4 . te verbeteren Ti5 O12 is geleidende oppervlaktemodificatie. Aslihan et al. [2] gesynthetiseerde Li4 Ti5 O12 via de sol-gel-methode en vervolgens de as-synthesized Li4 Ti5 O12 werd via stroomloze afzetting aan het oppervlak met zilver bekleed. De resultaten toonden aan dat zilvercoating (Ag-coating) een sterk geleidende matrix oplevert voor Li + insertie, verbetering van de elektronische geleidbaarheid. Zhu et al. [19] geprepareerde koolstof-gecoate nano-sized Li4 Ti5 O12 nanoporeuze microbolletjes met een opmerkelijk snelheidsvermogen via een koolstofprecoatingproces in combinatie met een sproeidroogmethode, en gaven aan dat de bolvormige deeltjes ter grootte van een micron een grote tikdichtheid induceren, wat resulteert in een verbetering van de volumetrische energiedichtheid. Echter, hoe Ag-gecoate micron-sized Li4 . te synthetiseren Ti5 O12 sferische deeltjes via een sol-gel-ondersteunde hydrothermische methode is niet gerapporteerd.
Hierin rapporteren we een door sol-gel ondersteunde hydrothermische methode om de bolvormige Li4 ter grootte van een micron te synthetiseren. Ti5 O12 /Ag-composiet met ethyleenglycol en een zilvernitraatmengsel als voorloper, en het gehalte aan de Ag-coating werd aangepast door de hoeveelheid zilverelement in de voorloper te regelen. De elektrochemische eigenschappen van de Li4 Ti5 O12 /Ag met sferische morfologie werden in detail onderzocht.
Experimenteel
Synthese van ongerepte Li4 Ti5 O12 en wijziging van het oppervlak met Ag
Synthese van de sferische voorloper via de Sol-Gel-methode
De sferische voorloper titaniumglycolaat (TG) werd gesynthetiseerd door de sol-gel-methode. Eerst werd langzaam 2 ml tetrabutyltitanaat toegevoegd aan de oplossing, die AgNO3 bevatte. (in een geschikte hoeveelheid om oplosbaar te zijn in 50 ml glycol), onder krachtig roeren om de voorloperoplossing te vormen. Ten tweede werd de voorloperoplossing toegevoegd aan een 150 ml acetonmengsel dat 0,1 ml Tween 80 bevatte, en het roeren werd gedurende 1 uur bij kamertemperatuur voortgezet om precipitaten te vormen. Vervolgens werden de precipitaten 8 uur verouderd, gescheiden door filtratie en tweemaal gewassen met watervrije alcohol. Ten slotte werden de voorloperpoeders verkregen door een warmtebehandeling bij 80 ° C gedurende 6 uur in een oven, gevolgd door malen.
Synthese van sferische Li4 Ti5 O12 /Ag
De bolvormige Li4 Ti5 O12 /Ag werd bereid via de hydrothermische methode. Ten eerste, LiOH·H2 O en de voorloper in een molverhouding van 3,9:1 werden homogeen gemengd door 1 uur te roeren met 40 ml alcohol als medium om een mengsel te vormen, dat vervolgens 12 uur op 180 ° C werd verwarmd in afgesloten Teflon-waren tot precipitaten waren verkregen. Ten tweede werden de precipitaten verzameld via centrifugatie (5000 rpm, 5 min) en verschillende keren verder gewassen met watervrije ethanol. Daarna werden ze 2 uur gedroogd in een oven bij 80 ° C. Ten slotte werden de neerslagen gedurende 2 uur in een moffeloven verwarmd op 700 °C (opwarmsnelheid van 5 °C·min −1 ) in lucht nadat ze waren gemalen en vervolgens op natuurlijke wijze afgekoeld tot kamertemperatuur om sferisch Li4 te verkrijgen Ti5 O12 /Ag-poeder.
Materiaalkarakterisering
De structuur van de Li4 Ti5 O12 monsters werden geïdentificeerd via röntgendiffractie (XRD, Rigaku D/max-PC2200) met behulp van een Cu Kα-stralingsbron (λ =0,15405 nm) met een scansnelheid van 4 °min −1 van 10° tot 80° en werkt op 40 KV en 20 mA. De morfologie en deeltjesgrootte van de materialen werden onderzocht via SEM (scanning-elektronenmicroscopie, Supra 55 Zeiss) en TEM (transmissie-elektronenmicroscopie, JEOL-2100).
Elektrochemische metingen
De elektrochemische prestaties van de producten werden getest met behulp van een CR2025-knoopcel. De werkelektroden werden bereid door 80 gew.% Li4 . te mengen Ti5 O12 /Ag actieve materialen, 10 gew.% geleidende Super-P en 10 gew.% polyvinylideenfluoride (PVDF) bindmiddel in N-methyl-2-pyrrolidon (NMP) oplosmiddel om een uniforme slurry te vormen. Vervolgens werd de slurry op een aluminiumfolie gegoten en 12 uur onder vacuüm bij 80 ° C gedroogd om het resterende oplosmiddel te verwijderen. Vervolgens werd de folie geperst en in schijven gesneden. Een Celgard 2400 polypropyleen microporeus membraan en lithiumfolie werden gebruikt als respectievelijk de separator en de negatieve elektrode. De elektrolytoplossing was 1 M LiPF6 in ethyleencarbonaat (EC), dimethylcarbonaat (DMC) en ethyleenmethylcarbonaat (EMC) in een volumetrische verhouding van 1:1:1. De cellen werden geassembleerd in een met argon gevulde handschoenenkast, waar zowel het vocht- als het zuurstofgehalte onder de 1 ppm werden gehouden. De elektrochemische tests van de producten werden geëvalueerd met behulp van een LAND CT2001A-testsysteem (Wuhan, China). Cyclische voltammetrie (CV) tests werden opgenomen op een CHI600A elektrochemisch werkstation bij een 0,1 mV s −1 scansnelheid van 1,0 tot 2,5 V (vs. Li/Li + ). EIS-metingen zijn uitgevoerd in het frequentiebereik van 100 KHz tot 10 mHz met een verstoring van 5 mV.
Resultaten en discussie
Structurele en morfologische eigenschappen
Het effect van de hoeveelheid Ag-additief op de Li4 Ti5 O12 /Ag-poeders werden onderzocht. De XRD-patronen van de met Ag gecoate sferische Li4 Ti5 O12 composieten worden gegeven in Fig. 1. Het is gemakkelijk te zien dat de belangrijkste diffractiepieken van alle specimens verschijnen bij 18,4°, 35,54°, 43,2°, 57,2°, 62,8° en 66,1° en worden geïndexeerd als de (111), (311), (400), (333), (440) en (531), respectievelijk. Die pieken komen goed overeen met de Li4 Ti5 O12 standaard diffractiepatroon [20], behalve karakteristieke patronen van het Ag-metaal (2θ =38,1°, 44,3°, 64,4°). In geen van de monsters werden onzuiverheidsdiffractiepieken gedetecteerd. Bovendien nam de piekintensiteit van zilver dienovereenkomstig toe naarmate de hoeveelheid Ag toenam.
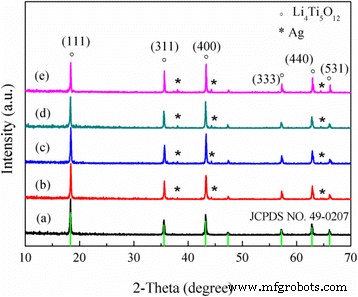
XRD-patronen van de Li4 Ti5 O12 /Ag. (een ) 0 gew.%, (b ) 1 gew.%, (c ) 3 gew.%, (d ) 5 gew.%, en (e ) 7 gew.%
Roosterparameters van de Li4 Ti5 O12 /Ag-monsters met verschillende Ag-coatings worden gegeven in Tabel 1. Er werden geen significante veranderingen waargenomen met de toename van het Ag-gehalte. Zo werd gesuggereerd dat zilver voornamelijk een laag vormt in de vorm van het elementaire Ag op het oppervlak van Li4 Ti5 O12 deeltjes maar dringen niet door in het rooster van spinel Li4 Ti5 O12 . Omdat de ionische straal van Ag + (0,126 nm) is aanzienlijk groter dan die van de Ti 4+ (0,068 nm), de gesynthetiseerde Li4 Ti5 O12 /Ag-monster was slechts een samenstelling van het Ag-metaal en het Li4 Ti5 O12 fase.
Afbeelding 2 toont de SEM-afbeeldingen van de voorbereide voorloper (a1 -e1 ) en Li4 Ti5 O12 /Ag (a2 -e2 ). Zoals getoond in Fig. 2, vertonen alle monsters een uniform bolvormige structuur met een smalle grootteverdeling van 5-10 m, wat gunstig is voor een contact tussen de actieve materialen en de elektrode. Op de SEM-beelden toont de sferische voorloper, titaniumglycolaat (TG) deeltjes, een vloeiende lijn, terwijl de Li4 Ti5 O12 /Ag-deeltjes vertonen een ruwe lijn. Bovendien zou een goede dispersie het contactoppervlak tussen elektrode en elektrolyt kunnen vergroten en het transport van Li + aanzienlijk kunnen versnellen. en elektron. Het oppervlak van de Li4 Ti5 O12 /Ag-monsters zijn niet duidelijk gladder dan die van de bereide voorloper en titaniumglycolaat, en ze bestaan tot op zekere hoogte als een agglomeratie. Bovendien zijn de deeltjesgroottes van verschillende Li4 Ti5 O12 /Ag-composieten zijn veel groter dan die van Ag-vrije Li4 Ti5 O12; het fenomeen agglomeratie wordt echter duidelijker naarmate het zilvergehalte toeneemt.

SEM-beelden van de voorloper en de Li4 Ti5 O12 /Ag. (een ) 0 gew.%, (b ) 1 gew.%, (c ) 3 gew.%, (d ) 5 gew.%, (e ) 7 gew.%
De verdeling van zilver in het binnenste van de micron-sized deeltjes werd verder onderzocht, en TEM- en HRTEM-analyses werden gegeven in Fig. 3. De TEM-afbeeldingen (Fig. 3a) laten zien dat de 5 gew.% Ag-gecoate micron-sized -sferische Li4 Ti5 O12 deeltjes zijn uniform bedekt met een zilverlaag met een dikte van 3 ~ 4 nm, wat aangeeft dat de zilverlaag een geleidend netwerk opbouwt op het oppervlak van het gehele materiaal, wat het lithiumion- en elektronentransport vergemakkelijkt. Zoals getoond in Fig. 3b, is het oppervlak van de micron-sized Li4 Ti5 O12 /Ag-deeltjes zijn niet glad en de d -afstand van de 5 gew.% Ag-gecoate Li4 Ti5 O12 deeltjes is 0,484 nm, wat goed overeenkomt met die van het LTO (111) vlak. Dit suggereert dat er geen nieuwe fase werd gegenereerd op het oppervlak van de LTO-deeltjes, maar dat er een dunne coatinglaag op de deeltjes zat.

(een ) TEM en (b ) HRTEM-beelden van de 5 gew.% verzilverde Li4 Ti5 O12 , waarbij de "lijn" de gecoate zilverlaag aangeeft
Elektrochemische eigenschappen
Figuur 4 toont de eerste laad-ontlaadcurven van de bolvormige Li4 ter grootte van een micron Ti5 O12 /Ag-elektroden gecoat met verschillende Ag-gehalten bij verschillende snelheden. Zoals te zien is in figuur 4, vertonen alle profielen een extreem vlak spanningsplateau van 1,55 V (vs. Li/Li + ), wat wijst op een overgang in twee fasen tussen Li4 Ti5 O12 en Li7 Ti5 O12 voor lithium-insertie [21]. Het spanningsplatform van Li4 Ti5 O12 /Ag-composieten zijn langer dan die van Ag-vrije Li4 Ti5 O12 . Met een toenemend gehalte aan Ag, voor een langer ontladingsplatform van de Li4 Ti5 O12 /Ag-composieten, is het vermogen om het platform te onderhouden sterker, wat suggereert dat een goede elektronische geleidbaarheid de polarisatie van het materiaal tijdens het elektrodereactieproces effectief kan verminderen en het gebruik van het materiaal kan verbeteren.
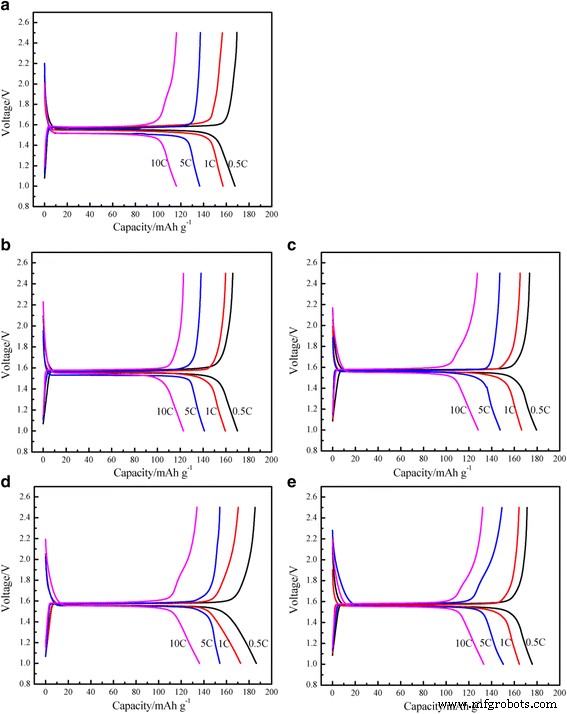
De initiële laad-ontlaadcurven met verschillende stroomdichtheden van de Li4 Ti5 O12 /Ag. (een ) 0 gew.%, (b ) 1 gew.%, (c ) 3 gew.%, (d ) 5 gew.%, (e ) 7 gew.%
Zoals getoond in Fig. 4, Ag-vrij Li4 Ti5 O12 leverde een initiële ontladingsspecifieke capaciteit van 167,62 mAh g −1 met een snelheid van 0,5C, terwijl de geleverde capaciteit van de Ag-gecoate bolvormige Li4 Ti5 O12 composieten namen toe met toenemende hoeveelheid zilver:170,10, 179,54 en 186.34 mAh g −1 voor respectievelijk 1, 3 en 5 gew.%. Maar 7 gew.% Ag-gecoate Li4 Ti5 O12 een wat ander gedrag vertoonden. De geleverde ontladingsspecifieke capaciteit nam af met toenemende hoeveelheid zilver:175,86 mAh g −1 voor 7 gew.%. De 5 gew.% Ag-gecoate Li4 Ti5 O12 kreeg de hoogste initiële ontladingscapaciteit en de initiële ontladingsspecifieke capaciteiten bereikten 186.34, 172.47, 154.12 en 136.06 mAh g −1 bij de specifieke stromen van respectievelijk 0,5, 1, 5 en 10C. Vanwege de slechte elektronische geleidbaarheid en trage Li + diffusie vertoont het materiaal een grote polarisatie bij hoge laad-/ontlaadsnelheden. Het sterk geleidende Ag-additief kan de oppervlakte-intercalatiereactie aanzienlijk verbeteren en de polarisatie verminderen [20, 22]. Zelfs het hoogste Ag-gehalte (7 gew.%) kan het langste spanningsplateau opleveren en het metaalzilver zelf kan niet volledig in het lithium worden geïntercaleerd. In plaats daarvan zal het hoge gehalte aan Ag leiden tot een afname van de specifieke capaciteit van Li4 Ti5 O12 /Ag. Daarom kan een geschikt zilvergehalte niet alleen de geleidbaarheid van de Li4 . effectief verbeteren Ti5 O12 en verminder de polarisatie van de Li4 Ti5 O12 in het reactieproces, maar kan ook het verlies van de omkeerbare capaciteit door de Ag-coating verminderen.
De snelheidsmogelijkheden van de Ag-vrije Li4 Ti5 O12 en 5 gew.% Ag-gecoate Li4 Ti5 O12 composiet werden geanalyseerd bij stroomdichtheden van 0,5, 1, 5 en 10C, en de resultaten worden getoond in Fig. 5. Zoals getoond, is de initiële capaciteit van de 5 gew.% Ag-gecoate Li4 Ti5 O12 composiet bij 5C was 154,12 mAh g −1 . Na 30 cycli werd de capaciteit nog steeds gehandhaafd op 150,50 mAh g −1 , met behoud van meer dan 97,65% van de oorspronkelijke capaciteit. Toen het verder werd verhoogd tot 10C, daalde de ontladingscapaciteit blijkbaar van 136,06 mAh g −1 tot 130,81 mAh g −1 na 30 cycli. Terwijl de retentie-efficiëntie van de capaciteit nog steeds op 96,14% kon worden gehandhaafd. Bovendien zijn de fietsprestaties van de Li4 Ti5 O12 /Ag-composiet was significant beter dan dat van de Ag-vrije Li4 Ti5 O12 tegen verschillende laad-ontlaad tarieven. Zoals getoond in Fig. 6a, met een geschikt zilvergehalte van 5 gew.%, is het met zilver beklede Li4 Ti5 O12 leverde de hoogste capaciteit van 186.34 mAh g −1 bij 0,5C, wat hoger is dan die van andere monsters, en behield 92,69% van zijn initiële capaciteit bij 5C na 100 cycli. Zelfs bij 10C na 100 cycli (Fig. 6b), had het nog steeds een capaciteitsbehoud van 89,17%, wat een opmerkelijke cyclusstabiliteit aantoont. De resultaten suggereerden dat onder de gunstige experimentele omstandigheden de Li4 Ti5 O12 oppervlakte-Ag-coating verbeterde niet alleen de elektronen- en ionische geleidbaarheid, maar verhoogde duidelijk ook het elektronentransport tijdens de lithium-insertie-/extractiereactie en verbeterde de cyclusstabiliteit van de Li4 aanzienlijk Ti5 O12 .
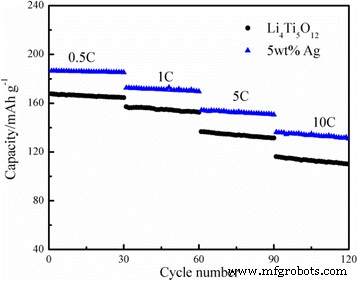
Snelheidscapaciteit van de Ag-vrije en de 5 gew.% Ag-gecoate Li4 Ti5 O12 onder verschillende huidige tarieven
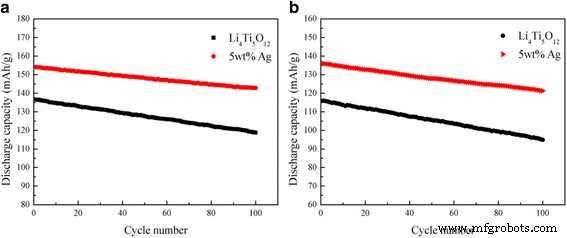
De fietsprestaties van de Ag-free en de 5 gew.% Ag-gecoate Li4 Ti5 O12 bij 5 °C (a ) en 10 °C (b )
Afbeelding 7 toont de cyclische voltammogrammen (CV's) van de Ag-vrije Li4 Ti5 O12 en 5 gew.% Ag-gecoate Li4 Ti5 O12 composiet verkregen met een lage snelheid van 0,1 mV s −1 . Het is duidelijk dat omkeerbare redoxpieken tussen 1,0 en 2,5 V werden verkregen, die worden toegeschreven aan de invoeging en extractie van lithiumionen, wat suggereert dat er geen tussenfase-vorming is tijdens het inbrengen en de-inbrengen van lithium. Ondertussen is het redoxpiekoppervlak van deze twee curven bijna gelijk, wat wijst op een hoge coulombefficiëntie [23]. De potentiaalverschillen tussen de oxidatie- en reductiepieken van de 5 gew.% Ag-gecoate Li4 Ti5 O12 is 0,244 V, wat iets lager is dan die van de Ag-vrije Li4 Ti5 O12 (0,24 V). Dit suggereert dat een geschikte oppervlaktecoating van het sterk geleidende Ag-additief de polarisatie van het Li4 aanzienlijk verminderde. Ti5 O12 monster en verbeterde effectief de elektrochemische prestaties. Bovendien waren de redoxpieken van het 5 gew.% Ag-gecoate Li4 Ti5 O12 zijn scherper en groter dan die van Ag-vrije Li4 Ti5 O12 , wat aangeeft dat een geschikte Ag-coating de dynamische prestaties van de elektrode kan verbeteren.
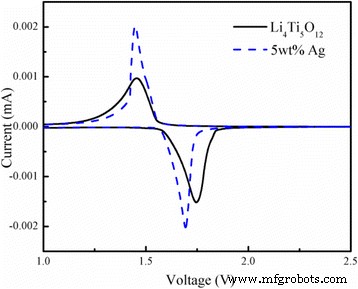
CV-curven van de Ag-vrije en de 5 gew.% Ag-gecoate Li4 Ti5 O12 composiet
Elektrochemische impedantiespectroscopie (EIS) metingen van Ag-vrije Li4 Ti5 O12 en 5 gew.% Ag-gecoate Li4 Ti5 O12 werden uitgevoerd in het frequentiebereik van 10 5 tot 0,01 Hz vóór galvanostatische cycli. Bovendien worden het equivalente circuit (inzet) en bijbehorende impedantiegegevens getoond in Fig. 8. In het equivalente circuit, Rs vertegenwoordigt de weerstand van de elektrolytoplossing, die de elektrische geleidbaarheid van de elektrolyt, separator en elektroden weerspiegelt. (kruising met de Z ′ as met een hoge frequentie), R ct toont de ladingsoverdrachtsweerstand in materialen, CPE is de dubbellaagse en passiveringsfilmcapaciteit, en W is de Warburg-impedantie, die verband houdt met lithiumiondiffusie in het laagfrequente gebied. De parameters die zijn verkregen door te passen zijn weergegeven in tabel 2. Zoals weergegeven in figuur 8, waren beide EIS-curven samengesteld uit een ingedrukte halve cirkel in het hoogfrequente gebied en een schuine rechte lijn in het laagfrequente gebied. De diameter van de halve cirkel staat voor de ladingsoverdrachtsweerstand, en de schuine rechte lijn is gerelateerd aan de Warburg-impedantie [24]. De impedantie van de halve cirkels in het hoogfrequente gebied komt overeen met het ladingsoverdrachtsproces van de elektrode en het vloeibare elektrolytinterface, en de rechte lijn in het laagfrequente gebied kan worden uitgedrukt als het diffusiegedrag van lithiumionen in de oxidestructuur [25,26, 27,28]. Zoals getoond in Fig. 8, is de diameter van de halve cirkel van het 5 gew.% Ag-gecoate Li4 Ti5 O12 is korter dan die van kale Li4 Ti5 O12 , wat aangeeft dat een juiste hoeveelheid Ag-coating de elektronische geleidbaarheid van Li4 . kan verbeteren Ti5 O12 , en dit heeft te maken met het overboekingsproces, waarbij Li + en elektronen bereiken gelijktijdig het elektrodeoppervlak om de reactie te voltooien. Dit hangt voornamelijk af van de redoxreactie over het oppervlak van de actieve materialen. De kleinere ladingsoverdrachtsweerstand van de 5 gew.% Ag-gecoate Li4 Ti5 O12 weerspiegelden een snellere ladingsoverdrachtsreacties op hun elektrode/elektrolyt-interfaces.
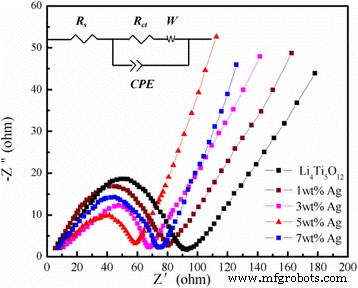
EIS-patronen van de pure Li4 Ti5 O12 en de Li4 Ti5 O12 gecoat met verschillende Ag-gehaltes
De chemische diffusiecoëfficiënt van lithiumionen kan worden berekend uit de grafiek in het laagfrequente gebied met behulp van de volgende vergelijking. (1) [29,30,31,32,33].
$$ {D}_{{\mathrm{Li}}^{+}}=\frac{R^2{T}^2}{2{A}^2{n}^4{F}^4{ C}_{Li}^2{\sigma_w}^2} $$ (1)Hier is \( {D}_{{\mathrm{Li}}^{+}} \) de lithium-ion diffusiecoëfficiënt, R is de gasconstante (8.314 JK mol −1 ), T is de absolute temperatuur (298 K), A is het oppervlak van de elektrode, n is het aantal elektronen per molecuul dat de elektronische overdrachtsreactie bijwoont, F is de constante van Faraday (96.500 C mol −1 ), C Li is de concentratie van lithiumionen in de Li4 Ti5 O12 elektrode, en σ w is de Warburg-factor, die de volgende relatie heeft met Ζ re :
$$ {Z}_{\mathrm{re}}={R}_S+{R}_{\mathrm{ct}}+{\sigma}_w\cdot {\omega}^{- 0,5} $$ (2 )Bovendien is de relatie tussen Z re en de reciproke vierkantswortel van frequentie in de lage frequentie wordt getoond in Fig. 9. Alle parameters verkregen en berekend uit de EIS zijn samengevat in Tabel 2. Zoals getoond in Tabel 2, \( {D}_{\mathrm{ L}{\mathrm{i}}^{+}} \) van de 5 gew.% Ag-gecoate Li4 Ti5 O12 is 6.73 × 10 −11 , wat een orde van grootte hoger is dan die van Li4 Ti5 O12 (8.69 × 10 −12 ). De 5 gew.% Ag-gecoate Li4 Ti5 O12 heeft de grootste lithiumdiffusiecoëfficiënt vergeleken met die van Ag-vrij Li4 Ti5 O12 en 1, 3 en 7 gew.% Ag-gecoat Li4 Ti5 O12 composieten, wat aangeeft dat coating met Ag een effectieve manier is om de elektronische geleidbaarheid te verbeteren. Bijgevolg is de snelheidscapaciteit van de 5 gew.% Ag-gecoate Li4 Ti5 O12 kan aanzienlijk worden verbeterd.
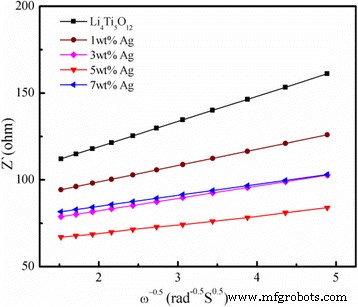
Grafiek van Z re samengespannen tegen ω −0.5 in het lage frequentiegebied voor de Li4 Ti5 O12 en Li4 Ti5 O12 gecoat met verschillende Ag-gehaltes
Conclusies
Anodematerialen bolvormig Li4 Ti5 O12 /Ag-composieten met een hoge tikdichtheid werden bereid met een sol-gel-ondersteunde hydrothermische methode. De elektrochemische tests tonen aan dat de juiste hoeveelheid Ag-coating de elektronische geleidbaarheid van Li4 aanzienlijk kan verbeteren Ti5 O12 en verbeteren de cyclus stabiliteit. Het optimale zilvergehalte is 5 gew.%, wat uitstekende elektrochemische prestaties kan opleveren. Het overmatige zilvergehalte zal echter de elektrochemische eigenschappen van het materiaal verslechteren. Daarom geschikte Ag-gecoate sferische Li4 Ti5 O12 composiet is een superieur lithium-opslagmateriaal met een hoge capaciteit en uitstekende veiligheid, en het heeft echt potentieel als veelbelovend materiaal in lithium-ionbatterijen.
Nanomaterialen
- Koper Tungsten Contact Materiaal Voorbereidingsmethode
- C#-methode
- Hydrothermisch ondersteunde sinterstrategie naar poreus en hol gestructureerd LiNb3O8 anodemateriaal
- Eenvoudige synthese van SiO2@C-nanodeeltjes verankerd op MWNT als hoogwaardige anodematerialen voor Li-ionbatterijen
- Hydrothermische synthese van In2O3 nanodeeltjes hybride tweeling hexagonale schijf ZnO heterostructuren voor verbeterde fotokatalytische activiteiten en stabiliteit
- Weinig gelaagde MoS2/acetyleenzwarte composiet als een efficiënt anodemateriaal voor lithium-ionbatterijen
- Nabehandelingsmethode voor de synthese van monodisperse binaire FePt-Fe3O4-nanodeeltjes
- Effect van de synthesemethode van La1 − xSr x MnO3 manganite nanodeeltjes op hun eigenschappen
- Ingesloten Si/Grafeencomposiet vervaardigd door magnesium-thermische reductie als anodemateriaal voor lithium-ionbatterijen
- Hydrothermisch gesynthetiseerd van CoMoO4-microsferen als uitstekend elektrodemateriaal voor supercondensator
- Nieuwe methode maakt computergeheugen van titaniumoxide



