Analyse van waterige corrosieproducten

Een combinatie van meerdere methoden is vaak vereist om waterige corrosieproducten correct te identificeren, waarbij de meest gebruikte methoden scanning-elektronenmicroscopie (SEM-EDS) / energiedispersieve röntgenspectroscopie (XRD) zijn. Identificatie van de corrosieproducten is belangrijk om toekomstige gebeurtenissen te voorkomen en zal van invloed zijn op de beslissing om de metallurgie te veranderen of de procesomstandigheden aan te passen. Hieronder volgen enkele typische verwachte waterige corrosieproducten voor verschillende legeringen en omstandigheden.
Pourbaix-diagrammen
Pourbaix-diagrammen kunnen een nuttig hulpmiddel zijn voor het bepalen van verwachte waterige corrosieproducten, die vervolgens kunnen worden vergeleken met de waargenomen. Thermodynamisch evenwicht wordt gebruikt om fasestabiliteit in een elektrochemisch gecontroleerd systeem te voorspellen. Het Pourbaix-diagram is verwant aan een fasediagram dat de stabiliteitsgrenzen toont voor een metaal-waterig systeem waar fasestabiliteit gerelateerd is aan pH en standaard elektronische waterstofpotentiaal.
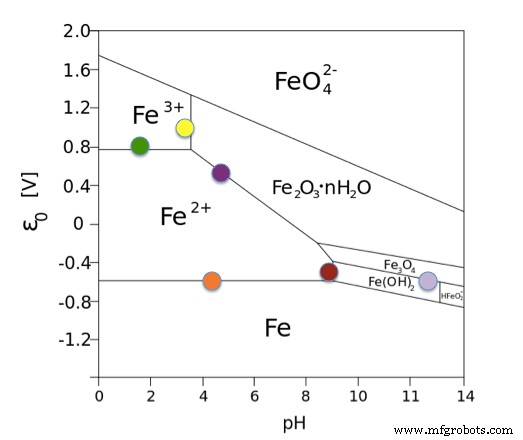 Pourbaix-diagram voor Fe.
Pourbaix-diagram voor Fe.
Bron:Andel Früh, Wikimedia Commons
Deze diagrammen zijn erg handig om te bepalen waar het metaal actief of passief is voor corrosie. Met de komst van verbeterde thermodynamische gegevens zijn er Pourbaix-diagrammen van legeringen met behulp van de CALPHAD-methodologie beschikbaar die kunnen worden gebruikt om mogelijke corrosie- of beschermende schaalsoorten aan te geven. Ze kunnen helpen bij het begrijpen van de waargenomen corrosieproducten op basis van de oxidatietoestand van de voorspelde soorten in oplossing en de verwachte beschermende schaal. Als er inconsistenties zijn, zijn de procesomstandigheden of corrosiechemie niet correct gespecificeerd.
Energiedispersieve spectroscopie (EDS)
Meer recentelijk is energiedispersieve spectroscopie (EDS) gebruikt om corrosieproducten te identificeren, maar deze methode heeft ook de tekortkoming dat het alleen elementen identificeert, geen verbindingen. De verbindingen moeten worden afgeleid door EDS, wat bijna onmogelijk is als het monster verschillende vormen van ijzersulfiden bevat. De eenvoudige olieveldmethoden die vaak worden gebruikt voor de identificatie van corrosieproducten zijn dus vaak misleidend. Er mag niet op worden vertrouwd bij het nemen van serieuze beslissingen met betrekking tot de toestand van apparatuur of de oorzaken van corrosie in een systeem. Röntgendiffractie (XRD) moet worden gebruikt om de aanwezige corrosieproducten positief te identificeren en te begrijpen.
Iron-mild-steel
IJzer en zacht staal in water zullen onoplosbare corrosieproducten van magnetiet ontwikkelen (Fe3 O4 ), lepidocrociet (g-FeOOH) en goethiet (a-FeOOH) afhankelijk van de pH. De hoeveelheid van elk bestanddeel kan variëren met de temperatuur. Beluchte zure 200 ppm chloride-oplossingen bij 25°C (77°F), zoals door weersinvloeden, produceren een roestlaag bestaande uit hematiet (a-Fe2 O3 ) en magnetiet.
Er zijn enkele verschillen in corrosieproducten opgemerkt als het staaloppervlak wordt blootgesteld aan meer geconcentreerde HCl-damp of in HCl-oplossing. Bij lagere blootstelling aan HCl geconcentreerde damp wordt een mengsel van goethiet en akageneiet (b-FeOOH) waargenomen; terwijl bij hogere HCl-dampconcentraties FeCl2 · 4H2 O wordt gevonden. Blootstelling van staal aan HCl-oplossing produceert lepidocrociet, goethiet en hematiet. Ondertussen omvatten corrosieproducten die bekend staan om staal in zeewater akageneiet, goethiet en FeOCl. Dus Cl - corrosieproducten kunnen behoorlijk variëren, afhankelijk van de blootstellingsomstandigheden. Wanneer het Cr-gehalte>4% is, kan het Cr-gehalte de omzetting van magnetiet naar goethiet in de roestlaag bevorderen.
De aanwezigheid van SO4 = produceert lepidocrociet, magnetiet, hematiet en goethiet corrosieproducten en met kortere tijden ferrihydriet (Fe5 O7 (OH)· 4H2 O), dat niet erg thermisch stabiel is en gemakkelijk verandert in goethiet en hematiet.
Waterige CO2 corrosie heeft de neiging om FeCO3 . te produceren afzettingen bij lagere temperaturen. Bij temperaturen boven 100°C (212°F) beide FeCO3 en magnetiet worden waargenomen, maar welke domineert is een functie van de partiële druk van CO2 . In carbonaatoplossingen, amorfe soorten en ferrihydriet, hematiet, mogelijk FeCO3 en ferrohydroxycarbonaat (Fe2 (OH)2 CO3 ) kan worden waargenomen.
Voor waterige H2 S, mackinawiet (FeS) is het minst thermodynamisch stabiele ijzersulfide, maar heeft de snelste vormingskinetiek. Nadat het zich aanvankelijk als een dunne laag op het metaal heeft gevormd, kan het transformeren in andere, stabielere vormen van ijzersulfiden, zoals pyrrhotiet (Fe1-x S) en pyriet (FeS2 ). Bij 25°C (77°F) mackinawiet, greigiet (Fe3 S4 ) en pyrrhotiet worden waargenomen, terwijl bij 80°C (176°F) mackinawiet, pyrrhotiet en pyriet worden gedetecteerd.
Een andere studie bij 120°C (248°F) merkte op dat het mackinawiet na verloop van tijd transformeerde in troilite (FeS) en vervolgens in pyrrhotiet en na verloop van tijd in pyriet. Bij afwezigheid van O2 en Cl, kan het kubische FeS een intermediair sulfide zijn. Deze sulfideaanslag kan ook worden waargenomen als corrosielagen op het metaal. De combinatie van een gemengde H2 S/CO2 oplossing heeft de neiging om de pyrrhotietlaag om te zetten in troilite en wat mackinawiet. De groei en fase-overgangen van polymorfe ijzersulfiden met verschillende stoichiometrische Fe/S-verhoudingen en structuren zijn dus zeer complex en zijn een functie van de blootstellingsomstandigheden.
In NaOH-oplossingen is hematiet het dominante corrosieproduct.
Onder reducerende omstandigheden vormt zich magnetiet op de waterzijdige oppervlakken van de ketel. Hematiet heeft de voorkeur bij wat lagere temperaturen en hogere zuurstofconcentraties.
Austenitisch roestvrij staal
Voor deze legeringen een uniforme 1-3 nm dikke Cr2 O3 film passiveert het metalen oppervlak en minimaliseert vlekken en corrosie. Als deze beschermende film oplost en/of wordt doorbroken, kan corrosie optreden waarbij de corrosie neigt naar een pitting-aanval. (Verwante lectuur:Corrosie van roestvrij staal door theevlekken voorkomen.)
Vanwege de beperkte hoeveelheid corrosieproducten worden de meeste identificaties van de corroderende soorten bereikt met SEM-EDS. XRD-analyse van de afzettingen van HCl-corrosie onthult FeCl2 , hematiet en Cr2 O3 . Blootstelling aan zeewater kan hematiet, magnetiet en Fe produceren (CrO4 )OH. Voor hogere Ni-legeringen zoals 904L in HF, bestaat de afzetting uit NiF2 , hematiet en Cr2 O3 . In zwavelzuur produceert Type 304 een passieve film van oxyhydroxiden, hematiet, FeO, NiO, sulfaat, sulfiet en Fe- en Ni-sulfiden.
Koper en koperlegeringen
Een waterige oplossing zal puur koper oxideren met Cu2 O (cupriet) is het overheersende onoplosbare product met Cu +2 overwegend oplosbare soorten zijn. De aanwezigheid van chloride zal de oplosbaarheid van Cu(I) vergroten zodat CuCl2 - wordt de dominante oplosbare soort. In een mariene omgeving wordt cupriet aanvankelijk gevormd; verdere interactie met Cl - produceert nantokiet (CuCl), dat vervolgens kan transformeren in atacamiet of de isomorfe fase paratacamiet (Cu2 (OH)3 Cl) als het eindpatina-corrosieproduct.
In met zwavel verontreinigde omgevingen zal zich aanvankelijk cupriet vormen, maar er kan ook Cu4 . zijn SO4 (OH)6 . H2 O, Cu4 SO4 (OH)6 (brochantiet), en Cu3 SO4 (OH)4 in het corrosieproduct. Als H2 S is aanwezig in een reducerende omgeving zoals in het geval van microbieel geïnduceerde corrosie (MIC), CuS of Cu8 S5 kan resulteren.
Cu en Zn zijn de belangrijkste elementen in de messingfamilie van legeringen. Vanwege het aanzienlijke evenwichtspotentiaalverschil van Cu en Zn, kan deloying van Zn optreden in waterige omgevingen, wat resulteert in een Zn-verarmde laag en Cu- en Zn-corrosieproducten. Meestal omvatten deze cupriet, CuO, Cu(OH)2 , ZnO en Zn(OH)2 . In mariene omgevingen, amorf zinkkoolwaterstof, Zn5 (CO3 )2 (OH)6 en ZnO kunnen worden waargenomen.
De legering van Sn tot Cu resulteert in de familie van bronslegeringen. In waterige media, SnO2 film kan semi-passief zijn. De defecte cuprietlaag wordt vervolgens gescheiden van de bulklegering door een binnenste beschermende SnO2 . In aanwezigheid van Cl - een buitenste nantokiet wordt soms gevormd, maar met langere tijden in een mariene omgeving CuO, Cu2 CO3 (OH)2 en atacamiet kan worden geproduceerd en in vervuilde wateren kan ook brochantiet aanwezig zijn.
Koper-nikkellegeringen staan bekend om hun corrosiebestendigheid. In een mariene omgeving zal cupriet zich aanvankelijk snel vormen en mogelijk beschermend zijn; maar met blootstelling aan Cl - , nantokiet, CuCl2 en paratacamiet worden geproduceerd. In belucht zeewater dat sulfide bevat, is de belangrijkste soort Cu2 S met mengsels van nantokiet, NiS, cupriet en NiO. (Verwante lectuur:11 toepassingen voor kopernikkel en waarom u het nu zou moeten gebruiken.)
Nikkellegeringen
Legeringen op nikkelbasis worden geselecteerd voor agressieve corrosieve omgevingen waar roestvrij staal niet geschikt is. Door Ni te legeren met verschillende hoeveelheden Cr en Mo en kleine hoeveelheden W, Cu en Fe, kan een hoge corrosieweerstand worden bereikt. De dunne passieve film bestaat uit een binnenste Cr2 O3 rijke laag en een buitenlaag van Cr/Ni-hydroxiden en Mo/Cu of W, die de corrosiebescherming bieden. Elektronendiffractie-analyse suggereert dat deze groepen Ni1-x . zijn Cr2x/3 O en b-Ni1-x Cr2x/3 (OH)2 waarbij Mo mogelijk een deel van de Cr vervangt.
Onder agressieve omstandigheden kunnen defecten in de beschermende film plaatselijke afbraak veroorzaken en zonder herpassivering kan metaal oplossen met daaropvolgende putcorrosie of spleetcorrosie. Corrosieproducten in een spleet voor legering 22, blootgesteld aan hete chloride-pekel, bleken MoO2 te zijn en ma4 O11; W kan worden gesubstitueerd in het molybdaat of als een afzonderlijke oxidesoort.
Onderhoud en reparatie van apparatuur
- Onderhoudsproducten Zep snijdt personeelsbestand 5%
- 5 verrassende koolstofvezelproducten
- Corrosiepreventie en lichtgewicht voertuigen
- Waarom is roestvrij staal corrosiebestendig?
- Beheersing van corrosie in koeltorens
- Corrosieproducten geproduceerd door blootstelling aan hoge temperaturen
- Hoe filiforme corrosie onder coatings te voorkomen
- Analyse van waterige corrosieproducten
- Aluminiumcorrosie vermijden
- WL 3.3354 Graad 3.3354 F
- Sanicro® 35



