Kunstmatige huid
Achtergrond
De huid, het grootste orgaan van het menselijk lichaam, beschermt het lichaam tegen ziekten en fysieke schade en helpt de lichaamstemperatuur te reguleren. Het is samengesteld uit twee grote lagen, de epidermis en de dermis. De epidermis of buitenste laag bestaat voornamelijk uit cellen:keratinocyten, melanocyten en langerhans. De dermis, die voornamelijk bestaat uit bindweefselvezels zoals collageen, levert voeding aan de opperhuid.
Wanneer de huid ernstig beschadigd is door ziekte of brandwonden, kan het lichaam niet snel genoeg handelen om de noodzakelijke vervangende cellen aan te maken. Wonden, zoals huidzweren bij diabetici, genezen mogelijk niet en ledematen moeten worden geamputeerd. Slachtoffers van brandwonden kunnen overlijden aan infectie en het verlies van plasma. Huidtransplantaten zijn ontwikkeld als een manier om dergelijke gevolgen te voorkomen en om misvormingen te corrigeren. Al in de zesde eeuw
Tot het einde van de twintigste eeuw werden huidtransplantaties gemaakt van de eigen huid (autografts) of kadaverhuid (allografts). Infectie of, in het geval van kadaverhuid, afstoting waren primaire zorgen. Terwijl huid die van het ene deel van het lichaam van een patiënt naar het andere wordt getransplanteerd, immuun is voor afstoting, worden huidtransplantaten van een donor op een ontvanger agressiever afgewezen dan enig ander weefseltransplantaat of -transplantaat. Hoewel de huid van een kadaver bescherming kan bieden tegen infectie en vochtverlies tijdens de eerste genezingsperiode van een slachtoffer van brandwonden, is een daaropvolgende transplantatie van de eigen huid van de patiënt vaak nodig. De arts is beperkt tot welke huid de patiënt beschikbaar heeft, een duidelijk nadeel in het geval van slachtoffers van ernstige brandwonden.
Halverwege de jaren tachtig bundelden medische onderzoekers en chemische ingenieurs, werkzaam op het gebied van celbiologie en kunststofproductie, hun krachten om tissue engineering te ontwikkelen om de incidentie van infectie en afstoting te verminderen. Een van de katalysatoren voor tissue engineering was het groeiende tekort aan organen die beschikbaar waren voor transplantatie. In 1984 deelde Joseph Vacanti, een chirurg van de Harvard Medical School, zijn frustratie over het gebrek aan beschikbare levers met zijn collega Robert Langer, een chemisch ingenieur aan het Massachusetts Institute of Technology. Samen vroegen ze zich af of er in het laboratorium nieuwe organen konden worden gekweekt. De eerste stap was om de weefselproductie door het lichaam te dupliceren. Langer kwam op het idee om een biologisch afbreekbare steiger te bouwen waarop huidcellen kunnen worden gekweekt met behulp van fibroblasten, cellen die worden gewonnen uit gedoneerde neonatale voorhuiden die tijdens de besnijdenis worden verwijderd.
In een variant van deze techniek die door andere onderzoekers is ontwikkeld, worden de geëxtraheerde fibroblasten toegevoegd aan collageen, een vezelig eiwit dat in bindweefsel wordt aangetroffen. Wanneer de verbinding wordt verwarmd, vormt het collageen een gel en vangt de fibroblasten op, die zich op hun beurt rond het collageen schikken en compact, dicht en vezelig worden. Na enkele weken worden keratinocyten, ook gewonnen uit de gedoneerde voorhuiden, gezaaid op het nieuwe dermale weefsel, waar ze een epidermale laag vormen.
Een kunsthuidtransplantaat biedt verschillende voordelen ten opzichte van die afkomstig van de patiënt en kadavers. Het elimineert de noodzaak voor weefsel 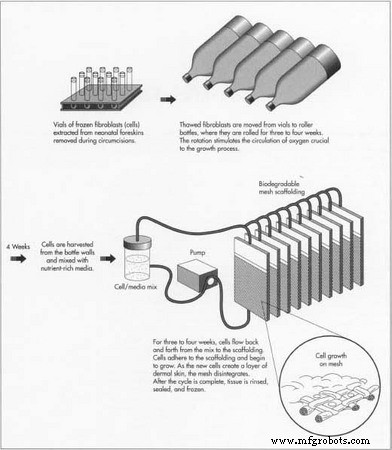 aan het typen. Kunsthuid kan in grote hoeveelheden worden gemaakt en ingevroren voor opslag en verzending, zodat het beschikbaar is als dat nodig is. Elke cultuur wordt gescreend op ziekteverwekkers, waardoor de kans op infectie sterk wordt beperkt. Omdat kunsthuid geen immunogene cellen bevat zoals dendritische cellen en capillaire endotheelcellen, wordt deze niet door het lichaam afgestoten. Ten slotte wordt de revalidatietijd aanzienlijk verkort.
aan het typen. Kunsthuid kan in grote hoeveelheden worden gemaakt en ingevroren voor opslag en verzending, zodat het beschikbaar is als dat nodig is. Elke cultuur wordt gescreend op ziekteverwekkers, waardoor de kans op infectie sterk wordt beperkt. Omdat kunsthuid geen immunogene cellen bevat zoals dendritische cellen en capillaire endotheelcellen, wordt deze niet door het lichaam afgestoten. Ten slotte wordt de revalidatietijd aanzienlijk verkort.
Grondstoffen
De grondstoffen die nodig zijn voor de productie van kunsthuid vallen in twee categorieën, de biologische componenten en de benodigde laboratoriumapparatuur. Het meeste gedoneerde huidweefsel is afkomstig van neonatale voorhuiden die tijdens de besnijdenis zijn verwijderd. Eén voorhuid kan genoeg cellen opleveren om vier hectare entmateriaal te maken. Fibroblasten worden gescheiden van de dermale laag van het gedoneerde weefsel. De fibroblasten worden in quarantaine geplaatst terwijl ze worden getest op virussen en andere infectieuze pathogenen zoals IIV, hepatitis B en C en mycoplasma. De medische geschiedenis van de moeder wordt geregistreerd. De fibroblasten worden bewaard in glazen flesjes en ingevroren in vloeibare stikstof bij -94°F (-70°C). Flesjes worden bevroren bewaard totdat de fibroblasten nodig zijn om culturen te laten groeien. Bij de collageenmethode worden ook keratinocyten uit de voorhuid gehaald, getest en ingevroren.
Als de fibroblasten moeten worden gekweekt op gaasstellingen, wordt een polymeer gemaakt door moleculen van melkzuur en glycolzuur te combineren, dezelfde elementen die worden gebruikt om oplossende hechtingen te maken. De verbinding ondergaat een chemische reactie die resulteert in een groter molecuul dat bestaat uit herhalende structurele eenheden.
Bij de collageenmethode wordt een kleine hoeveelheid rundercollageen gewonnen uit de strekpees van jonge kalveren. Het collageen wordt gemengd met een zure voedingsstof en bewaard in een koelkast bij 39,2 ° F (4 ° C).
Laboratoriumapparatuur omvat glazen flacons, slangen, rolflessen, entpatronen, mallen en diepvriezers.
Het fabricageproces
Het fabricageproces is bedrieglijk eenvoudig. De belangrijkste functie is om de geëxtraheerde fibroblasten te laten geloven dat ze zich in het menselijk lichaam bevinden, zodat ze op de natuurlijke manier met elkaar communiceren om een nieuwe huid te creëren.
Mesh steigermethode
- 1 Fibroblasten worden ontdooid en geëxpandeerd. De fibroblasten worden vanuit de flesjes overgebracht in rolflessen, die lijken op frisdrankflessen van een liter. De flessen worden drie tot vier weken op hun kant gedraaid. De rollende actie zorgt voor de circulatie van zuurstof, essentieel voor het groeiproces.
- 2 Cellen worden overgebracht naar een kweeksysteem. De cellen worden uit de rolflessen gehaald, gecombineerd met een voedingsrijk medium, door buizen gestroomd in dunne, cassette-achtige bioreactoren waarin de biologisch afbreekbare mesh-steiger is ondergebracht, en gesteriliseerd met e-beam-straling. Terwijl de cellen in de cassettes stromen, hechten ze aan het gaas en beginnen te groeien. De cellen worden drie tot vier weken heen en weer gestroomd. Elke dag wordt de overgebleven celsuspensie verwijderd en wordt er verse voeding toegevoegd. Zuurstof, pH, nutriëntenstroom en temperatuur worden geregeld door het kweeksysteem. Terwijl de nieuwe cellen een huidlaag vormen, valt het polymeer uiteen.
- 3 Groeicyclus voltooid. Wanneer de celgroei op het gaas is voltooid, wordt het weefsel gespoeld met meer voedingsrijke media. Er wordt een cryoprotectant toegevoegd. Cassettes worden afzonderlijk bewaard, gelabeld en ingevroren.
Collageenmethode
- 4 Cellen worden overgebracht naar een kweeksysteem. Een kleine hoeveelheid van het koude collageen en de voedingsmedia, ongeveer 12% van de gecombineerde oplossing, wordt aan de fibroblasten toegevoegd. Het mengsel wordt in vormen gedaan en op kamertemperatuur gebracht. Naarmate het collageen opwarmt, geleert het, waardoor de fibroblasten worden vastgehouden en de groei van nieuwe huidcellen wordt gegenereerd.
- 5 Keratinocyten toegevoegd. Twee weken nadat het collageen aan de fibroblasten is toegevoegd, worden de geëxtraheerde keratinocyten ontdooid en op de nieuwe dermale huid gezaaid. Ze mogen enkele dagen groeien en worden vervolgens blootgesteld aan lucht, waardoor de keratinocyten epidermale lagen vormen.
- 6 Groeicyclus voltooid. De nieuwe huid wordt tot gebruik in steriele containers bewaard.
De Toekomst
De medische wereld gebruikt kunstmatige huidtechnologie om de orgaanreconstructie te pionieren. Het is te hopen dat dit zogenaamde gemanipuleerde structurele weefsel op een dag bijvoorbeeld de plastic en metalen prothesen zal vervangen die momenteel worden gebruikt om beschadigde gewrichten en botten te vervangen. Oren en neuzen zullen worden gereconstrueerd door kraakbeencellen te zaaien op polymeergaas. De regeneratie van borst- en urethraweefsel wordt momenteel in het laboratorium bestudeerd. Door deze technologie is het mogelijk dat op een dag levers, nieren en zelfs harten zullen worden gekweekt uit menselijke weefsels.
Productieproces



