Au-Capped GaAs-nanopillar-arrays gefabriceerd door metaalondersteunde chemische etsing
Abstract
GaAs-nanopillar-arrays werden met succes vervaardigd door metaal-geassisteerd chemisch etsen met behulp van Au nanodot-arrays. De nanodot-arrays werden gevormd op substraten door vacuümafzetting door een poreus aluminiumoxidemasker met een geordende reeks openingen. Door een etsmiddel te gebruiken met een hoge zuurconcentratie en een lage oxidatiemiddelconcentratie bij een relatief lage temperatuur, kon het gebied rond het Au/GaAs-grensvlak selectief worden geëtst. Onder de optimale omstandigheden werden Au-capped GaAs nanopillar-arrays gevormd met een geordende periodiciteit van 100 nm en kolomhoogten van 50 nm.
Achtergrond
III-V samengestelde halfgeleiders hebben de aandacht getrokken als materialen van de volgende generatie en potentiële alternatieven voor op silicium gebaseerde halfgeleiders vanwege hun uitstekende eigenschappen, waaronder superieure draaggolfmobiliteit en directe bandafstand. Nanostructuren met geordende periodiciteit en/of hoge aspectverhouding worden beschouwd als een belangrijk element in verschillende toepassingen, waaronder optische en opto-elektronische apparaten vanwege hun lage kosten en hoge conversie-efficiëntie in vergelijking met conventionele op dunne film gebaseerde apparaten [1,2,3,4] . Over het algemeen worden voor het vervaardigen van laagdimensionale halfgeleiders (bijv. nanodraden) droge processen zoals moleculaire bundelepitaxie, damp-vloeistof-vaste stof epitaxie en metaal-organische dampfase-epitaxie gebruikt [1, 5,6,7]. Hoewel deze werkwijzen veel voordelen hebben, waaronder een hoge nauwkeurigheid van het patroonvorming, omvatten hun nadelen hoge kosten en beperkingen van de grootte van het patroonvormingsgebied in praktische toepassingen. Daarom zijn alternatieve methoden nodig die de eenvoudige en kosteneffectieve fabricage van nanostructuren mogelijk maken.
Chemisch etsen met metaalondersteuning, voorgesteld door Li en Bohn in 2000 [8], is een veelgebruikte fabricagemethode vanwege de relatieve eenvoud en lage kosten. Recente studies hebben aangetoond dat metaal-geassisteerd chemisch etsen kan worden toegepast om complexe nanostructuren te fabriceren zoals diepe, rechte nanoporiën, spiraalvormige nanoporiën, hellende kanalen, cycloïden en spiralen [4, 9,10,11,12]. Sinds het rapport van Li et al. hebben de meeste onderzoeken echter de fabricage van siliciumnanostructuren gerapporteerd; weinig onderzoeken hebben zich gericht op de nanofabricage van III-V samengestelde halfgeleiders [13, 14], en de vorming van geordende structuren op nanometerschaal op GaAs-substraten is bijzonder slecht begrepen. Om het toepassingsgebied van metaalgeassisteerd chemisch etsen uit te breiden, is het wenselijk om een nanofabricagemethode voor III-V samengestelde halfgeleiders te ontwikkelen die niet afhankelijk is van de afmetingen van de resulterende patronen.
In een eerdere studie hebben we microbump-arrays van InP [15] en lijnpatronen en pijlerarrays van GaAs [16] gefabriceerd met behulp van metaal-geassisteerd chemisch etsen. De afmetingen van de resulterende patronen (bijv. periodiciteit en breedte van de lijnpatronen) varieerden echter van enkele micrometers tot enkele tientallen micrometers. Voor zover ons bekend, heeft geen enkele studie de vorming gerapporteerd van geordende GaAs-nanostructuren met submicronschaal of kleinere periodiciteit met behulp van metaal-geassisteerd chemisch etsen om de volgende redenen:(1) het is moeilijk om de vorm en grootte van edele metalen te controleren gebruikt als katalysator op nanometerschaal en (2) het etsfenomeen van GaAs is minder goed begrepen in vergelijking met het geval van silicium. Daarom hebben we geprobeerd het etsmechanisme van GaAs op nanometerschaal te verduidelijken. In deze studie laten we zien dat geordende nanopijler-arrays met een periodiciteit van 100 nm kunnen worden gefabriceerd op GaAs-substraten met behulp van metaal-geassisteerd chemisch etsen met een van een patroon voorziene Au-katalysator. De effecten van etsmiddelsamenstelling en etstijd op de morfologie van het geëtste GaAs-substraat worden ook onderzocht.
Methoden
Het principe van de fabricage van GaAs-nanopillar-arrays via metaal-geassisteerd chemisch etsen wordt schematisch weergegeven in Fig. 1. Een doorlopende poreus aluminiumoxidemasker met een geordende reeks openingen werd bereid door anodisatie in twee stappen gevolgd door anodisatie in twee lagen [ 17]. De eerste anodisatie werd uitgevoerd op elektrochemisch gepolijst aluminium (99,99% zuiverheid) bij een constante spanning van 40 V in 0,3 mol dm −3 oxaalzuur bij 30 ° C gedurende 3 uur. De anodisatiespanning van 40 V is algemeen bekend als een zelfordenende voorwaarde die een zeer geordende porierangschikking in anodisch aluminiumoxide produceert [18].
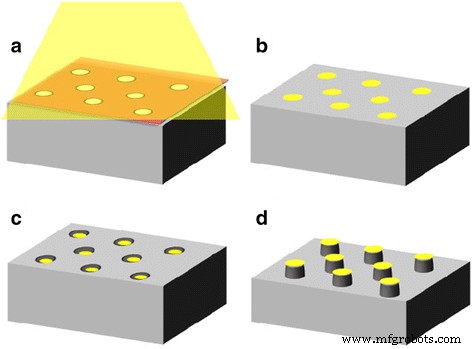
Schematisch model van de fabricage van GaAs nanopillar arrays. een Vacuümafzetting van Au op een GaAs-substraat door een poreus aluminiumoxidemasker. b Verwijdering van het masker. c , d Chemisch etsen van GaAs met Au nanodot-arrays als katalysator
Na de eerste anodisatie werd de eerste geanodiseerde aluminiumoxidelaag verwijderd in een gemengde oplossing van fosforzuur en chroomzuur bij 80 ° C. Vervolgens werd de tweede anodisatie gedurende 1,5 minuut uitgevoerd onder dezelfde omstandigheden als de eerste anodisatie. Gebaseerd op het principe van tweelaagse anodisatie, werd het monster opnieuw geanodiseerd bij een constante spanning van 40 V in 12 mol dm −3 zwavelzuur bij 5 ° C gedurende 8 minuten om een opofferende aluminiumoxidelaag te bereiden. Het doorlopende poreuze aluminiumoxidemasker werd gevormd door de opofferingsaluminiumoxidelaag gedurende 20 minuten bij 30°C op te lossen in 2 gew.% fosforzuur. Verder chemisch etsen werd uitgevoerd in 5 gew.% fosforzuur bij 30 °C gedurende 15 minuten om de poriediameter van het aluminiumoxidemasker te vergroten.
Na het spoelen van het aluminiumoxidemasker in gedestilleerd water, werd het verkregen aluminiumoxidemasker op een n-type GaAs-substraat gezet [Si-gedoteerd, 2.35–2.67 × 10 −3 Ω cm, (100) kristaloriëntatie]. Vervolgens werd een 30 nm dikke Au-laag verdampt door het aluminiumoxidemasker met behulp van een vacuümdepositiesysteem met de weerstandsverwarmingsformule (ULVAC KIKO Inc., VPC-410) met een druk lager dan 1 × 10 −3 Pa (afb. 1a). De dikte van de Au-laag werd gemeten met behulp van een kwartskristalmicrobalans en de afzettingssnelheid van Au was 0,02 nm s −1 . Na metaalafzetting werd het aluminiumoxidemasker 30 min verwijderd in 5 gew.% fosforzuur bij 25°C (Fig. 1b).
Het met Au gecoate GaAs-substraat werd chemisch geëtst in HF met KMnO4 (Fig. 1c). KMnO4 werkt als een oxidatiemiddel in een zure oplossing [19,20,21,22]. De morfologieën van het aluminiumoxidemasker, de afgezette Au-laag en het geëtste GaAs-substraat werden geëvalueerd door veldemissie scanning-elektronenmicroscopie (FE-SEM; JEOL JSM-6701F). De chemische samenstelling van het geëtste GaAs-substraat werd geëvalueerd met behulp van auger-elektronenspectroscopie (AES; JEOL JAMP-9500F). Auger-elektronenspectra kunnen gemakkelijk worden verkregen uit geselecteerde punten of gebieden van het oppervlak. Hier werd een AES-elementaire afbeelding verkregen met een versnellende spanning en emissiestroom van respectievelijk 30 kV en 15 nA.
Resultaten en discussie
Bij metaalgeassisteerd chemisch etsen is het essentieel om de afmetingen van de metaalkatalysator nauwkeurig te regelen om het gewenste ontwerp op het substraatoppervlak te verkrijgen. Omdat de morfologie van de resulterende structuur afhangt van het aanvankelijke geometrische patroon en de afmetingen van de metaalkatalysator, is een metaalkatalysator met patroon vereist om geordende nanostructuren op halfgeleideroppervlakken te fabriceren. In deze studie werd een aluminiumoxidemasker met een geordende reeks openingen gebruikt om de grootte en rangschikking van de metaalkatalysator te regelen. Voor een droog metaalafzettingsproces is de dikte van het masker van cruciaal belang omdat metaalafzetting door een dik masker met nauwe openingen fysiek moeilijk is. In het geval van poreus aluminiumoxide kan de dikte van het masker met hoge reproduceerbaarheid worden aangepast door de anodisatietijd te wijzigen. Hier werd een ongeveer 300 nm dik poreus aluminiumoxidemasker met een doorlopende opening vervaardigd op een GaAs-substraat. Het aluminiumoxidemasker werd geplaatst met het oppervlak naar boven gericht. De boven- en onderdiameters van de openingen in het aluminiumoxidemasker waren respectievelijk ongeveer 80 en 70 nm. De iets grotere diameter van de bovenste opening in vergelijking met de onderste opening werd toegeschreven aan chemisch etsen tijdens de voorbereiding van het aluminiumoxidemasker.
Figuur 2 toont een typische goed geordende Au nanodot-array op een GaAs-substraat. De nanodot-array komt overeen met de configuratie van de zelfgeordende porie-array in het anodische aluminiumoxidemasker, zoals weergegeven in figuur 2a. Hoewel de beheersbaarheid van Au-afzetting verder moet worden verbeterd, is de metaalafzetting door het hierin getoonde aluminiumoxidemasker geschikt voor de grootschalige productie van geordende edelmetaalpuntpatronen op halfgeleidersubstraten in termen van de eenvoud en efficiëntie van het fabricageproces. Merk op dat elke Au nanodot bijna dezelfde diameter had van ongeveer 70 nm; deze diameter werd bepaald door de poriegrootte van het onderste deel van het aluminiumoxidemasker, terwijl de hoogte van Au nanodots voornamelijk werd bepaald door de depositietijd. In deze studie werd de hoogte van elke Au nanodot aangepast tot ~30 nm, zoals weergegeven in figuur 2b.

een Surface en b SEM-afbeeldingen in dwarsdoorsnede van een Au nanodot-array gevormd op een GaAs-substraat door een anodisch poreus aluminiumoxidemasker
Na de vorming van Au-dot-arrays op GaAs-substraten, werden de monsters ondergedompeld in een oplossing van HF en KMnO4 voor metaal-geassisteerd chemisch etsen. Bij conventioneel metaal-geassisteerd chemisch etsen vindt het etsen plaatselijk plaats op het grensvlak tussen de katalysator en het onderliggende substraat, wat resulteert in de vorming van poriën of geulen in de richting loodrecht op het substraat, en de metaalkatalysator zakt in de halfgeleider zoals getoond in Afb. 1c. Het gebruik van een etsmiddel bestaande uit een hoge zuurconcentratie en een lage oxidatiemiddelconcentratie wordt geacht een vlotte consumptie van de gegenereerde positieve gaten te bevorderen (h + ) op de metaal/halfgeleiderinterface. In deze studie wordt verwacht dat de oxidatie van GaAs aan de Au/GaAs-interface direct verloopt via de gegenereerde h + .
Figuur 3 toont een typisch SEM-beeld van het geëtste GaAs-oppervlak met behulp van de Au-katalysator met patroon. Chemisch etsen werd uitgevoerd in een oplossing met 0,001 mol dm −3 KMnO4 en 20 mol dm −3 HF bij een relatief hoge temperatuur van 45°C. In deze studie was de concentratie van KMnO4 was laag (0,001 mol dm −3 ) om lateraal etsen te onderdrukken. Volgens eerdere rapporten van DeJarld et al. en Cheung et al., de laterale etssnelheid nam toe met toenemend oxidatiemiddel (KMnO4 ) concentratie [19, 21].

SEM-opname van het bovenoppervlak van GaAs-substraat na chemisch etsen met Au-ondersteuning in een oplossing van 0,001 mol dm −3 KMnO4 en 20 mol dm −3 HF gedurende 600 s bij 45 °C
Au-katalysatoren, die werden gedetecteerd als cirkelvormige heldere vlekken, werden waargenomen in de poriën in veel gebieden van het GaAs-substraat, zoals weergegeven in figuur 3. De diameter van de poriën waargenomen in figuur 3 viel samen met de afmetingen van de gedeponeerde Au nanodots getoond in Fig. 2. Deze resultaten geven aan dat conventioneel metaal-geassisteerd chemisch etsen, dat schematisch wordt weergegeven in Fig. 1c, alleen plaatsvond op het Au/GaAs-grensvlak en anisotroop loodrecht op het substraat verliep, dwz in de <100> richting.
Bij metaalgeassisteerd chemisch etsen beïnvloeden de etsmiddelsamenstelling en etstemperatuur de dynamiek van dragerdiffusie, oxidatie en productverwijdering [19]. Om nieuwe toepassingen van geëtst GaAs-substraat te openen, hebben we geprobeerd GaAs-nanopillar-arrays te fabriceren door de omstandigheden van metaal-geassisteerd chemisch etsen te veranderen. Figuur 4 toont typische SEM-afbeeldingen in dwarsdoorsnede van geëtste GaAs-oppervlakken die zijn verkregen met behulp van de Au-katalysator met patroon. Door de concentratie van KMnO4 . te verhogen , kan de morfologie van de resulterende structuur worden gewijzigd. In alle gevallen werden GaAs-nanopilaren verkregen die hexagonaal over het gehele monsteroppervlak waren gerangschikt. De punten van de pilaren liepen iets taps toe als gevolg van lateraal etsen. De periodiciteiten van de GaAs-nanopillar-arrays waren ongeveer 100 nm, wat overeenkomt met die van de Au-dot-arrays die als katalysator werden gebruikt en de poriën van het poreuze aluminiumoxide dat als het initiële masker werd gebruikt. Voor zover wij weten, zijn de afmetingen (bijv. periodiciteit) van de structuren verkregen op GaAs via metaal-geassisteerd chemisch etsen in deze studie kleiner dan die gerapporteerd voor andere GaAs-structuren [19,20,21,22].

SEM-afbeeldingen van GaAs-nanopillar-arrays vervaardigd door Au-geassisteerd chemisch etsen in oplossingen die 0,01 mol dm −3 bevatten KMnO4 en 5, 10 of 20 mol dm −3 HF gedurende 5 s om a 20 en b 45 °C
Wanneer het etsen werd uitgevoerd bij een relatief lage temperatuur van 20 ° C, werd Au-katalysator waargenomen aan de punt van elke pilaar, zoals aangegeven door pijlen. Figuur 4a laat zien dat de etssnelheid toenam met toenemende HF-concentratie bij dezelfde oxidatiemiddelconcentratie. Bij de hoge HF-concentratie van 20 mol dm −3 , was de resterende GaAs-kolomhoogte het hoogst.
In tegenstelling tot de verwachting dat de oxidatie van GaAs aan het Au/GaAs-grensvlak verloopt met de gegenereerde h + In het geval van figuur 4 werd geen chemische oplossing waargenomen in het contactgebied tussen de Au-katalysator en het onderliggende GaAs-substraat. Het etspatroon wordt geacht afhankelijk te zijn van de temperatuur van het etsmiddel. Bij lage temperatuur (bijv. 20 °C), de snelheid van h + het verbruik bij de Au/GaAs-interface wordt verondersteld lager te zijn dan de snelheid van h + injectie; dus h + verspreid in het gebied rondom met Au-gecoate GaAs. Uiteindelijk werd een GaAs-nanopilaar gevormd onder het contactgebied tussen de Au-katalysator en het onderliggende GaAs-substraat omdat plaatsselectief etsen plaatsvond op het blootgestelde GaAs-oppervlak. Met andere woorden, de Au nanodots fungeerden ook als een beschermend masker om het oplossen van het GaAs-substraat te voorkomen. Dit etsfenomeen, zoals schematisch weergegeven in figuur 1d, wordt inverse metaalondersteunde chemische etsing genoemd [19, 22]. In 2010 hebben we ook de vorming van InP-microbump-arrays aangetoond met behulp van inverse metaalondersteunde chemische etsing onder UV-straling [15]. In tegenstelling tot conventioneel metaal-geassisteerd chemisch etsen, vindt omgekeerd metaal-geassisteerd chemisch etsen plaats in blootgestelde III-V samengestelde halfgeleideroppervlakken rond metaal-gecoate gebieden door de diffusie van h + van metaalkatalysator en daaropvolgend plaatsselectief chemisch etsen. Een dergelijk uniek etsgedrag is niet waargenomen in siliconenmaterialen.
Wanneer metaal-geassisteerd chemisch etsen wordt uitgevoerd bij een hoge temperatuur van 45°C, wordt de gegenereerde h + zal naar verwachting worden geconsumeerd zodra het de grens tussen Au, GaAs en etsmiddel bereikt, wat resulteert in de bevordering van verticaal etsen. Zelfs in dit geval vond echter omgekeerd metaal-geassisteerd chemisch etsen plaats. Zoals getoond in Fig. 4b, nam de etssnelheid toe met toenemende HF-concentratie op dezelfde manier als het etsgedrag van Fig. 4a. Bij een hoge etstemperatuur van 45 °C en een hoge HF-concentratie van 20 mol dm −3 , werden de Au-katalysatoren losgemaakt van de uiteinden van de GaAs-pilaren omdat de overtollige h + gegenereerd door de relatief hoge temperatuur, zelfs in de korte etstijd van 5 s, bevorderde het laterale etsen van GaAs in aanwezigheid van de Au-katalysator. De vormbeheersbaarheid van de pilaren zal worden verbeterd door de aanvullende optimalisatie van etsomstandigheden (bijv. etsmiddelsamenstelling, concentratie en temperatuur). Pogingen om de effecten van de concentratie van oxidatiemiddel op de vorming van h + te verduidelijken en morfologie van geëtste GaAs zijn momenteel aan de gang.
Om het effect van de etstijd op de geometrie van de geëtste GaAs-structuur te onderzoeken, werd het chemisch etsen verlengd in 20 mol dm −3 HF en 0,01 mol dm −3 KMnO4 bij een relatief lage temperatuur van 20°C. Zoals getoond in de dwarsdoorsnede in figuur 5a, bereikte de diepte van de GaAs-nanopilaren ~ 50 nm. Een van de opvallende kenmerken van de GaAs-nanopillar-arrays die in dit onderzoek zijn verkregen, is dat de punt van elke pilaar bedekt was met Au, zoals weergegeven in de inzet van figuur 5a. Afbeelding 6 toont de AES-elementanalyse van hetzelfde monster. De AES-kaarten voor Ga en Au van de geëtste GaAs geven de aanwezigheid van Au aan de punt van elke pilaar aan, zelfs na met metaal geassisteerd chemisch etsen gedurende 10 s.

SEM-afbeeldingen in dwarsdoorsnede van een GaAs-nanopillar-array vervaardigd door Au-geassisteerd chemisch etsen bij 20 °C voor a 10 en b 60 s in een oplossing van 20 mol dm −3 HF en 0,01 mol dm −3 KMnO4 . Inzet toont een oppervlaktebeeld van een Au-capped GaAs nanopillar array

een Afbeelding van GaAs-substraat na Au-geassisteerd chemisch etsen en bijbehorende AES-kaarten voor b Ga en c Au. De etsomstandigheden waren dezelfde als die in Fig. 5a
Omdat de pilaarhoogte voornamelijk werd bepaald door de etstijd, werd het etsen verder verlengd van 10 s tot 1 minuut om arrays van hogere pilaren op GaAs te vormen. De verlengde etstijd van 1 minuut resulteerde echter in een verminderde pilaarhoogte, zoals weergegeven in figuur 5b. De afname van de pilaarhoogte werd toegeschreven aan lateraal etsen in aanwezigheid van Au-katalysator en het daaropvolgende loslaten van de Au-dots die als katalysator werden gebruikt.
Hoewel metaal-geassisteerd chemisch etsen, dat precies de diffusie van h + regelt, van metaalkatalysator, nog niet volledig is voltooid, biedt de nanofabricage van III-V samengestelde halfgeleiders met behulp van metaal-geassisteerd chemisch etsen een veelbelovend alternatief voor het ontwerpen van geordende driedimensionale structuren zonder het gebruik van droge processen. Bovendien hebben de verkregen Au-capped GaAs-nanopillar-arrays potentiële technologische en wetenschappelijke toepassingen in opto-elektronische apparaten zoals zonnecellen die plasmonische nanostructuren gebruiken om het vangen van licht te verbeteren [23, 24].
Conclusies
Samenvattend hebben we de fabricage aangetoond van geordende GaAs-nanopillar-arrays op GaAs (100) -substraten via Au-geassisteerd chemisch etsen. Au nanodot-arrays met hexagonale roosterpatronen en geordende periodiciteiten van 100 nm werden gevormd door vacuümafzetting door een poreus aluminiumoxidemasker. De Au nanodots hadden een diameter van ongeveer 70 nm, overeenkomend met de diameter van het onderste deel van het aluminiumoxidemasker, en dienden als katalysator en beschermend masker. Bij relatief lage temperaturen zouden Au-capped GaAs-nanopillar-arrays kunnen worden gevormd door plaatsselectief etsen in het omringende blootgestelde GaAs-oppervlak. Deze bevindingen leveren het eerste bewijs voor de meer nauwkeurige controle van nanostructuren op GaAs-substraten met behulp van een haalbare benadering op basis van metaal-geassisteerd chemisch etsen. De onconventionele lithografietechniek voor de nanofabricage van III-V samengestelde halfgeleiders die in deze mededeling wordt gepresenteerd, overwint de nadelen van conventionele methoden en heeft potentiële technologische en wetenschappelijke toepassingen in verschillende onderzoeksgebieden.
Afkortingen
- AES:
-
Auger-elektronenspectroscopie
- FE-SEM:
-
Veldemissie scanning elektronenmicroscopie
Nanomaterialen
- Chemische eigenschappen van titanium
- C#-matrices
- C++-matrices
- C-matrices
- C Multidimensionale arrays
- Java-arrays
- Ontrafeling van de morfologische evolutie en etskinetiek van poreuze silicium nanodraden tijdens metaalondersteunde chemische etsing
- Effecten van micro-omgevings-pH van liposoom op chemische stabiliteit van geladen geneesmiddel
- Verbeterde biocompatibiliteit in anodische TaO x Nanotube-arrays
- TiO2-nanobuisarrays:gefabriceerd op basis van een zacht-hard sjabloon en de korrelgrootte-afhankelijkheid van veldemissieprestaties
- MATLAB - Arrays



