Bereiding van aluminiumoxide nanostaafjes uit chroomhoudend aluminiumoxide slib
Abstract
Uit chroomhoudend aluminiumoxideslib werden nanostaafjes van aluminiumoxide gemaakt en de effecten van doteringselementen, zoals Cr, Fe en Mg, onderzocht. De resultaten laten zien dat de kristaltransformatie van aluminiumoxide wordt beperkt door het gedoteerde Cr en mogelijk wordt gemaakt door het gedoteerde Fe en Mg, dat wordt getransformeerd vanuit θ -Al2 O3 naar α -Al2 O3 in het calcinatieproces. Ondertussen wordt de kristaltransformatie van aluminiumoxide sterk belemmerd door samen gedoteerde elementen uit het chroomhoudende aluminiumoxideslib. De gedoteerde elementen veranderen het verloop van de transformatie van de fasestructuur en transformeren de chemische binding van de aluminiumoxide-nanostaafjes enigszins. De onzuivere elementen zijn gedoteerd in het aluminiumoxidekristal en beperken de kristalgroei van aluminiumoxide nanostaafjes volgens de regels. In het monster dat is bereid uit chroomhoudend aluminiumoxideslib, is meer Cr en Mg maar minder Fe gedoteerd, en het meeste Cr komt voor als Cr(III). Het is mogelijk dat de Fe-doping beperkt wordt door de concurrentie van Cr en Mg. Bovendien wordt de roosterimperfectie van aluminiumoxide veroorzaakt door gedoteerde ionen, zoals Cr, Fe en Mg, en wordt de chemische toestand van O en Al beïnvloed. De bevindingen van deze experimenten bieden essentiële informatie voor het elimineren van vervuiling en het bevorderen van een alomvattend gebruik van het chroomhoudende aluminiumoxideslib.
Achtergrond
Laagdimensionaal nano-aluminiumoxide, zoals aluminiumoxide-nanovezels [1,2,3] en aluminiumoxide-nanostaafjes [4], heeft superieure eigenschappen van hoge sterkte, hoge elastische modulus, chemische stabiliteit, goede thermische isolatieprestaties en lage thermische geleidbaarheid [5, 6,7,8,9], dus het werd op grote schaal toegepast op verschillende gebieden, zoals versterking voor keramische matrixcomposieten en metaalmatrixcomposieten en katalysator, katalysatordrager, adsorbentia, membraanreactor, coatings en anodematerialen [4, 10, 11,12,13,14,15]. Hoge productiekosten hebben de toepassing ervan echter beperkt. Sommige auteurs hebben met succes synthesemethoden van laagdimensionaal nano-aluminiumoxide gerapporteerd, voornamelijk met inbegrip van vastefasemethode, dampfasemethode [16] en vloeistoffasemethode [17, 18]. Onder hen wordt de vloeistoffasemethode op grote schaal toegepast vanwege de milde reactieconditie, homogene producten en lage productiekosten. Er waren veel rapporten over de bereiding van nano-aluminiumoxide met de sol-gelmethode [5, 19,20,21], micro-emulsiemethode [22], hydrothermische methode [23], precipitatiemethode [23], chemische dampafzetting [16], en elektrospinnen [1, 3, 24, 25]. De neerslagmethode is echter geschikt voor laboratoria en industrieën vanwege het lage energieverbruik, de homogeniteit van het product en de controleerbare grootte en vorm.
Het chroomhoudende aluminiumoxideslib is een soort gevaarlijk vast afval, dat wordt geproduceerd in het productieproces van chroomproducten door middel van een niet-calciumroostmethode. Uit elke ton chroomproduct wordt zevenduizend kilogram van het chroomhoudende aluminiumoxideslib gegenereerd. Het is samengesteld uit 55 ~ 65% van Al2 O3 , 7 ~ 13% chroom en weinig verbindingen van silicium, ijzer, magnesium en natrium. De componenten van het chroomhoudende aluminiumoxideslib worden weergegeven in tabel 1, die wordt geleverd door de fabrikant (CITIC Jinzhou Metal Co., Ltd., China).
Als de belangrijkste gevaarlijke stof komt chroom voor in de vorm van Cr(III) of Cr(VI) in het chroomhoudende aluminiumoxideslib, en Cr(VI) wordt beschouwd als de dominante verontreinigende stof vanwege zijn kankerverwekkendheid [26]. Momenteel wordt de oplossingsverontreiniging van het chroomhoudende aluminiumoxideslib voornamelijk ontgiftigd en benut. De eerste zet Cr(VI) om in Cr(III) met een lage toxiciteit en slaat het op als afvalresidu. Zhang Dalei [27] merkte een pyrolysemethode op om Cr(VI) om te zetten in Cr(III) met stro. Duan Suhua [28] wees erop dat de chroomhoudende slak behandeld kon worden met industriële alcohol. De hierboven genoemde methoden nemen echter niet alleen land in beslag, maar veroorzaken ook grote verspilling van hulpbronnen. Bovendien kan de secundaire vervuiling onverwacht optreden. De laatste methode is om de bruikbare componenten van het chroombevattende aluminiumoxideslib te scheiden en te gebruiken. Xue Wendong [29] meldde dat het chroomhoudende aluminiumoxideslib gebruikt kon worden om vuurvast materiaal te maken. De bovenstaande methode kan echter beperkt zijn vanwege de lage toegevoegde waarde. Daarom moeten er enkele nieuwe methoden worden voorgesteld om vervuiling te elimineren en een alomvattend gebruik van het chroomhoudende aluminiumoxideslib te bevorderen, wat niet alleen milieuproblemen kan oplossen, maar ook grote economische voordelen oplevert.
In dit artikel worden nanostaafjes van aluminiumoxide bereid uit het chroomhoudende aluminiumoxideslib door middel van een precipitatiecalcineringsmethode. Ondertussen worden, om de invloed van het enkelvoudig doteringsion op de aluminiumoxide nanostaafjes te onderzoeken, de aluminiumoxide nanostaafjes met niet- of enkelvoudig doteringsionen bereid en gekarakteriseerd. De resultaten zullen technische ondersteuning bieden voor het elimineren van vervuiling en het bevorderen van een alomvattend gebruik van het chroomhoudende aluminiumoxideslib.
Methoden
Materialen
De reagentia (bijv. aluminiumsulfaatoctadecahydraat, chroomsulfaat, ijzersulfaat, magnesiumsulfaat, natriumhydroxide, zwavelzuur en natriumdodecylbenzeensulfonaat) die in dit onderzoek werden gebruikt, waren analytisch zuivere chemicaliën. Het chroomhoudende aluminiumoxideslib werd geleverd door CITIC Jinzhou Metal Co., Ltd. (China). Alle oplossingen werden bereid met gedeïoniseerd water.
Behandeling van het chroomhoudende aluminiumoxideslib
In eerste instantie werd het chroomhoudende aluminiumoxideslib gewassen en gefilterd door gedeïoniseerd water volgens de vast-vloeistofverhouding van 1:5 (g/ml). Als gevolg hiervan zijn de meeste Cr 6+ verbindingen werden gescheiden van het chroomhoudende aluminiumoxideslib. Vervolgens werd de filterkoek opgelost met zwavelzuur volgens de vast-vloeistofverhouding van 1:3 (g/ml), en vervolgens werd de H2 O2 werd gebruikt om de resterende Cr 6+ . te transformeren naar Cr 3+ . Eindelijk werd de chroombevattende slibzuuroplossing van aluminiumoxide met succes verkregen en werden de componenten geanalyseerd door chemische titratie en zichtbaar-lichtspectrofotometer (VIS, 721N, Varian, Amerika) weergegeven in tabel 2.
Synthese van aluminiumoxide nanostaafjes
Twee mol per liter NaOH-oplossing en dodecylbenzeensulfonaatoplossing werden langzaam toegevoegd aan 0,25 mol/L Al2 (SO4 )3 oplossing onder magnetisch roeren bij 85°C, en de pH-waarde van de gemengde oplossing werd ingesteld op 9,0 met NaOH of H2 SO4 oplossing. Na 5 uur roeren en 20 uur rijpen werden de precipitaten gescheiden en verschillende keren gewassen met gedeïoniseerd water en ethylalcohol. Vervolgens werden de monsters gedurende 15 uur bij 40°C vacuüm gedroogd en vervolgens werden de voorlopers bereid. Ten slotte werden de monsters 1 uur lang gecalcineerd bij 250 ° C, 1 uur 400 ° C, 1 uur 770 ° C, 1 uur 900 ° C en 2 uur 1050 ° C, en vervolgens werden de monsters verzameld voor gebruik. Het ongedoteerde aluminiumoxide werd bereid uit puur Al2 (SO4 )3 oplossing, en de met ionen gedoteerde monsters werden bereid met dezelfde methode als hierboven. Ondertussen werden de chloraten van Cr, Fe en Mg toegevoegd in de Al2 (SO4 )3 oplossing volgens de inhoud van het doteringselement in het chroombevattende aluminiumoxideslib (tabel 2) en het met Cr-gedoteerde, Fe-gedoteerde en Mg-gedoteerde aluminiumoxide werden bereid. Gebruikmakend van de chroomhoudende aluminiumoxideslibzuuroplossing als grondstof, werd het aluminiumoxide genoemd dat werd bereid uit het chroomhoudende aluminiumoxideslib.
Karakterisatie van nano-aluminiumoxidestaven
De kristallijne fasen van de monsters werden gekenmerkt door röntgenpoederdiffractie (XRD) met behulp van D/MAX-RB röntgendiffractometer (Rigaku, Japan) met Cu K-straling in het 2θ-bereik van 10 ° -70 ° bij een scan snelheid van 2°/min. Fourier-transformatie-infraroodspectra (FT-IR) van de monsters werden gekarakteriseerd met behulp van Scimitar 2000 Near FT-IR Spectrometer (Thermo-elektron, VS), en de spectra werden opgenomen in het bereik van 4000-400 cm −1 . De thermische stabiliteit van de voorloper werd onderzocht met een thermogravimetrische analysator (TG-DSC, STA449F3, NETZSCH, Duitsland) met een stroomsnelheid van 30 ml / min in luchtatmosfeer en een temperatuur van 15-1200 ° C met een verwarmingssnelheid van 10 ° C/min. De morfologieën, kristalstructuur en elementverdeling van de monsters werden onderzocht met veldemissietransmissie-elektronenmicroscopie (FETEM, Jem-2100F, JEOL, Japan). De röntgenfoto-elektronspectroscopie (XPS) spectra van de monsters werden opgenomen op XPS (ESCAMABMKLL, VG, VK) uitgerust met een halfbolvormige elektronenanalysator en een Al Kα Röntgenbron.
Resultaten en discussie
XRD-karakterisering van de aluminiumoxide-nanostaafjes
XRD-patronen werden opgenomen om de kristalstructuur van de monsters te bevestigen, zoals weergegeven in Fig. 1. Voor de ongedoteerde aluminiumoxide-nanostaafjes tonen de XRD-resultaten het bestaan aan van verschillende kristallijne structuren van aluminiumoxide, waaronder korund (α -Al2 O3 , syn) (JCPDS No. 46-1212) en aluminiumoxide (θ -Al2 O3 , JCPDS No. 35-0121), en de diffractiepieken van θ -Al2 O3 zijn zwakker (Fig. 1 (a)). Over het algemeen wordt het aluminiumoxide getransformeerd vanuit de overgangstoestand θ -Al2 O3 naar stabiele toestand α -Al2 O3 bij 1000 ~ 1200 °C. Vergeleken met het ongedoteerde monster hebben Cr-gedoteerde aluminiumoxide nanostaafjes relatief sterkere pieken van θ -Al2 O3 en relatief zwakkere toppen van α -Al2 O3 (Fig. 1 (b)). Het betekent dat de kristalovergang wordt beperkt door het gedoteerde Cr in het calcinatieproces, dus minder θ -Al2 O3 wordt getransformeerd naar α -Al2 O3 na calcineren bij 1050 °C. Uit Fig. 1 (c) blijkt dat de toppen van α -Al2 O3 zijn sterker en scherper dan die in (a) en (b), wat de grotere kristalgrootte en betere kristalliniteit suggereert. Ondertussen zijn de toppen van θ -Al2 O3 zijn nog zwakker, wat aangeeft dat de kristalovergang wordt vergemakkelijkt door het gedoteerde Fe. Het kan zijn omdat meer θ -Al2 O3 wordt getransformeerd naar α -Al2 O3 na calcineren. Figuur 1 (d) laat zien dat de met Mg gedoteerde aluminiumoxide-nanostaafjes relatief sterkere en scherpere pieken hebben van α -Al2 O3 en relatief zwakkere toppen van θ -Al2 O3 . Er wordt gesuggereerd dat het voorbeeld meer α . bevat -Al2 O3 en minder θ -Al2 O3 , wat te wijten kan zijn aan het feit dat het gedoteerde Mg de kristalovergang van aluminiumoxide in het calcinatieproces bevordert. Voor de aluminiumoxide-nanostaafjes die zijn bereid uit chroomhoudend aluminiumoxideslib, zijn de pieken van α -Al2 O3 bijna verdwijnen, terwijl de toppen van θ -Al2 O3 sterker maar niet scherp genoeg worden (Fig. 1 (e)). Er wordt aangegeven dat de θ -Al2 O3 heeft een slechte kristalliniteit en kleinere kristalgrootte. Dit zou kunnen zijn omdat er meer onzuiverheidselementen van het chroomhoudende aluminiumoxideslib in het aluminiumoxide worden gedoteerd, en de kristalovergang van aluminiumoxide wordt beperkt in het calcineringsproces. Dus de θ -Al2 O3 wordt zelden omgezet in α -Al2 O3 .
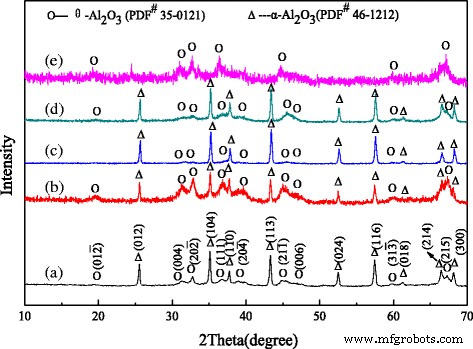
XRD patronen van aluminiumoxide nanostaafjes gedoteerd met verschillende ionen:a ongedoteerd aluminiumoxide, b Cr-gedoteerd aluminiumoxide, c Fe-gedoteerd aluminiumoxide, d Mg-gedoteerde aluminiumoxide, en e het aluminiumoxide bereid uit het chroomhoudende aluminiumoxideslib
FT-IR-spectra van de aluminiumoxide-nanostaafjes
FT-IR-spectra van aluminiumoxide nanostaafjes in het bereik van 4000-400 cm −1 zijn afgebeeld in Fig. 2 [27]. De absorptie pieken bij 3500-3300 en 1635 cm −1 die in alle spectra voorkomen, worden toegeschreven aan de rekvibratie van niet-chemische bindingsassociatie van respectievelijk OH-groepen en H-O-H-buigvibraties, wat aangeeft dat het poriewater en geadsorbeerd water in de monsters voorkomen [30]. De pieken op 2360 cm −1 worden toegeschreven aan de aanwezigheid van koolstofdioxide. Figuur 2 (2) toont het vingerafdrukgebied van FT-IR-spectra van de monsters. Zoals weergegeven in Fig. 2 (2a), voor het ongedoteerde monster, de pieken bij 829, 589 en 449 cm −1 worden toegeschreven aan AlO6 trillingen, die de vorming van α . aangeven -Al2 O3 [1]. Ondertussen zijn de pieken op 762 cm −1 worden toegeschreven aan de buigtrilling van Al–O–Al, en die van 663 en 488 cm −1 worden toegeschreven aan respectievelijk de rektrillingen en buigtrillingen van Al-O, wat wijst op de vorming van θ -Al2 O3 . Afbeelding 2 (2b) laat zien dat de toppen van α -Al2 O3 zijn zwakker dan die in Fig. 2(2a), wat aangeeft dat het Cr-gedoteerde de vorming van α voorkomt -Al2 O3 in het calcinatieproces. Voor het met Fe en Mg gedoteerde aluminiumoxide zijn de pieken van θ -Al2 O3 zwakker worden, en de toppen van α -Al2 O3 weinig wisselgeld hebben (Fig. 2 (2c,d)). In vergelijking met Fig. 2(2a) zijn de pieken roodverschoven of iets blauwverschoven, wat illustreert dat het gedoteerde Fe en Mg profiteren van de groei van α -Al2 O3 en transformeer de chemische binding van de aluminiumoxide-nanostaafjes enigszins. Fig. 2 (2e) is het vingerafdrukgebied van FT-IR-spectra van de aluminiumoxide-nanostaafjes bereid uit het chroombevattende aluminiumoxideslib. De pieken onder 500 cm −1 verdwijnen, wat aangeeft dat er geen α . is -Al2 O3 in de monsters. Bovendien zijn de pieken bij 900–500 cm −1 worden verspreid, wat het gevolg kan zijn van trillingen van M–O en M–O–M (M is Al of het gedoteerde element van aluminiumoxide uit het chroomhoudende aluminiumoxideslib). De bovenstaande resultaten zijn in overeenstemming met de XRD-resultaten.
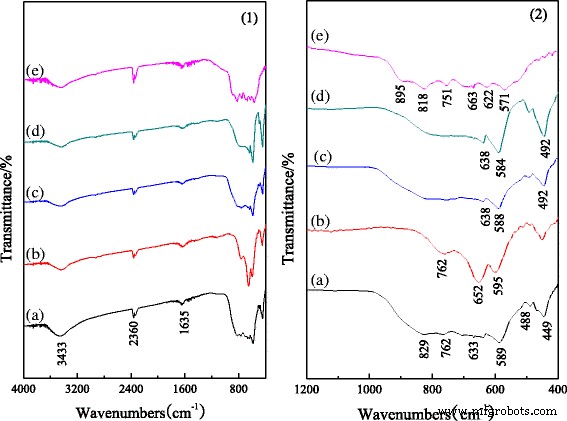
FT-IR-spectra van nano-aluminiumoxidestaafjes gedoteerd met verschillende ionen:a ongedoteerd aluminiumoxide, b Cr-gedoteerd aluminiumoxide, c Fe-gedoteerd aluminiumoxide, d Mg-gedoteerde aluminiumoxide, en e het aluminiumoxide bereid uit het chroomhoudende aluminiumoxideslib
TG-DSC van aluminiumoxide nanostaafjes
Thermogravimetrische analysator (TG) en differentiële scanning calorimetrie (DSC) curven van de aluminiumoxide-nanostaaf-precursoren worden getoond in Fig. 3. De XRD-resultaten geven aan dat de aluminiumoxide-nanostaaf-precursor AlO (OH) is (JCPDS nr. 49-0133). Zoals te zien is in figuur 3a, zijn in de lucht slechts drie stadia te zien in het ongedoteerde monster. Beneden 250 °C wordt ongeveer 40% massaverlies op de TG-curve en overeenkomstige endotherme pieken bij 50 en 150 °C op de DSC-curve geassocieerd met vochtverdamping en geadsorbeerd waterdesorptie. De tweede fase is tussen 250 en 730 ° C, met een totaal massaverlies van ongeveer 35% en twee endotherme pieken bij 320 en 694 ° C. Bij een temperatuur van 320 °C wordt de endotherme piek veroorzaakt door de transformatie van AlO(OH) naar amorf Al2 O3 . Ondertussen wordt de zwakke endotherme piek bij 694 °C toegeschreven aan de transformatie van amorf Al2 O3 naar θ -Al2 O3 . In de derde fase boven 730 °C is er een klein massaverlies en een sterke endotherme piek bij 980 °C, wat voornamelijk het resultaat is van de transformatie van θ -Al2 O3 naar α -Al2 O3 . Vergeleken met het ongedoteerde monster zorgt dotering met metaalionen ervoor dat de endotherme pieken verschuiven. Figuur 3b–e laat zien dat de endotherme pieken zijn verschoven naar een hogere temperatuur en breder werden. Het kan zijn dat de gedoteerde ionen het verloop van fasestructuurtransformatie veranderen, dus de transformatiegraad van θ -Al2 O3 naar α -Al2 O3 is voor elk monster anders. De resultaten komen overeen met de XRD en FT-IR.
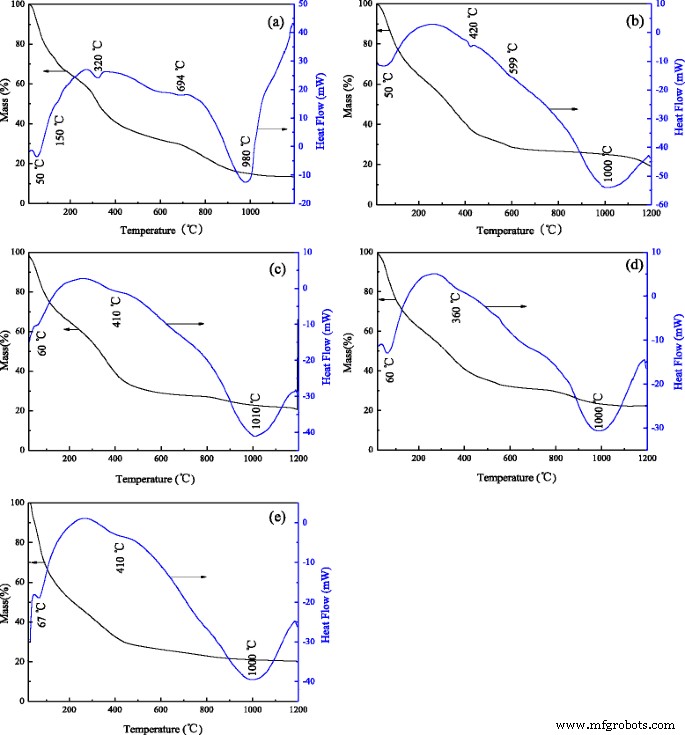
TG en DSC van de nano-aluminastaafprecursoren gedoteerd met verschillende ionen:a ongedoteerd aluminiumoxide, b Cr-gedoteerd aluminiumoxide, c Fe-gedoteerd aluminiumoxide, d Mg-gedoteerde aluminiumoxide, en e Het aluminiumoxide bereid uit het chroomhoudende aluminiumoxideslib
TEM-, SAED- en HRTEM-afbeeldingen van aluminiumoxide-nanostaafjes
Afbeelding 4 geeft de resultaten van TEM, geselecteerde gebiedselektronendiffractie (SAED) en transmissie-elektronenmicroscopie met hoge resolutie (HRTEM). Zoals weergegeven in figuur 4 (a1-a3), zijn de ongedoteerde aluminiumoxide dispersieve nanostaafjes met een diameter van 4-6 nm en een lengte van 20-60 nm. Ondertussen zijn de vlakken (215), (006), (21 \( \overline{1} \)) en (20 \( \overline{4} \)) in overeenstemming met θ -Al2 O3 (JCPDS No. 35-0121), en de (300), (214), (113) en (104) vliegtuigen worden geassocieerd met α -Al2 O3 (JCPDS nr. 46-1212). Verder zou de waargenomen interplanaire afstand van 0,273 en 0,284 nm kunnen worden toegewezen aan de (20 \( \overline{2} \)) en (004) vlakken van θ -Al2 O3 , en de roosterafstand van 0,255 en 0,348 nm kan overeenkomen met de (104) en (012) vlakken van α -Al2 O3 . In vergelijking met het ongedoteerde monster is het met Cr gedoteerde monster nanostaafjes met een diameter van 4-6 nm en een lengte van 50-120 nm (figuur 4 (b1)). Afbeelding 4 (b2) laat zien dat de vlakken (215), (21 \( \overline{1} \)), (20 \( \overline{2} \)) en (111) in overeenstemming zijn met -Al2 O3 , en de (300), (214), (113) en (104) vlakken zijn in overeenstemming met α -Al2 O3 . Zoals weergegeven in figuur 4 (b3), wordt de interplanaire afstand van 0,202 nm, 0,273 nm, 0,284 nm en 0,454 nm toegewezen aan de (21 \( \overline{1} \)), (20 \( \overline{ 2} \)), (004), en (10 \( \overline{2} \)) vlakken van θ -Al2 O3 , en de interplanaire afstand van 0,209 en 0,238 nm zijn toegewezen aan de (113) en (110) vlakken van α -Al2 O3 . Figuur 4 (c1) laat zien dat het Fe-gedoteerde monster het mengsel is van nanostaafjes met een diameter van 5-10 nm en een lengte van 30-100 nm en nanodeeltjes van ongeveer 10 nm. Figuur 4 (c2) laat zien dat de (20 \( \overline{2} \)) vlakken in overeenstemming zijn met θ -Al2 O3 , en de (300), (214), (024), (113), (104) en (116) vlakken zijn in overeenstemming met α -Al2 O3 , het is in overeenstemming met de XRD-resultaten. Ondertussen wordt de waargenomen interplanaire afstand van 0,284 en 0,454 nm toegewezen aan de (004) en (10 \( \overline{2} \)) vlakken van θ -Al2 O3 , en de interplanaire afstand van 0,238 en 0,255 nm zijn toegewezen aan de (110) en (104) vlakken van α -Al2 O3 (Fig. 4 (c3)).
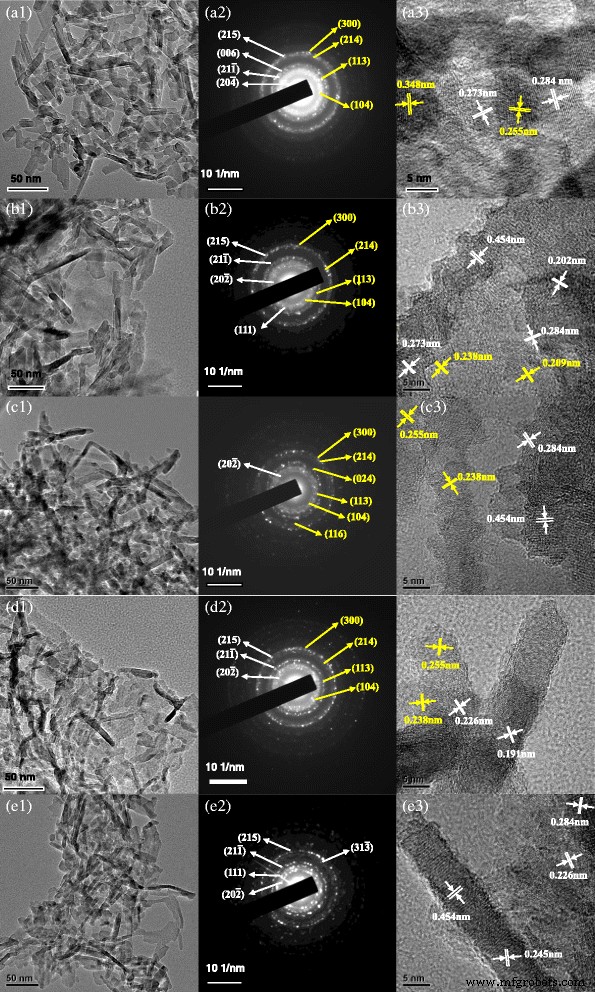
TEM, SAED en HRTEM van aluminiumoxide nanostaafjes gedoteerd met verschillende ionen:a ongedoteerd aluminiumoxide, b Cr-gedoteerd aluminiumoxide, c Fe-gedoteerd aluminiumoxide, d Mg-gedoteerde aluminiumoxide, en e het aluminiumoxide bereid uit het chroombevattende aluminiumoxideslib. (1) TEM; (2) SAED; (3) HRTEM
Zoals weergegeven in figuur 4 (d1-d3), bestaat het met Mg gedoteerde monster uit goed verspreide nanostaafjes met een diameter van 5-10 nm en een lengte van 20-50 nm, en bestaan er tegelijkertijd nanodeeltjes van ongeveer 10 nm. De SAED-resultaten laten zien dat de (215), (21 \( \overline{1} \)) en (20 \( \overline{2} \)) vlakken in overeenstemming zijn met θ -Al2 O3 , en de (300), (214), (113) en (104) vlakken zijn in overeenstemming met α -Al2 O3 . De HRTEM-resultaten laten zien dat de waargenomen interplanaire afstand van 0,226 en 0,191 nm wordt toegewezen aan de (20 \( \overline{4} \)) en (006) vlakken van θ -Al2 O3 , en de interplanaire afstand van 0,255 en 0,238 nm zijn toegewezen aan de (104) en (110) vlakken van α -Al2 O3 . Figuur 4 (e1-e3) laat zien dat het monster dat is bereid uit chroomhoudend aluminiumoxideslib goed verspreide nanostaafjes is met een diameter van 4-6 nm en een lengte van 50-100 nm, en dat er tegelijkertijd nanodeeltjes van ongeveer 5-10 nm bestaan. De SAED- en HRTEM-resultaten laten zien dat (215), (111), (21 \( \overline{1} \)), (31 \( \overline{3} \)), en (20 \( \overline{2 } \)) vlakken zijn in overeenstemming met θ -Al2 O3 , en de waargenomen interplanaire afstand van 0,226, 0,245, 0,284 en 0,454 nm worden toegewezen aan de (20 \( \overline{4} \)), (111), (004), en (10 \( \overline{2 } \)) vlakken ervan. Er zijn echter geen vliegtuigen in overeenstemming met α -Al2 O3 . Als gevolg hiervan zijn de ongedoteerde aluminiumoxide-nanostaafjes goed verspreid dan de andere en hebben de deeltjes een regelmatige vorm. Het kan zijn dat de onzuiverheidselementen zijn gedoteerd in het aluminiumoxidekristal en de kristallijne groei van aluminiumoxide-nanostaafjes volgens de regels hebben beperkt. De vormen en dispergeerbaarheid van de nanostaafjes van aluminiumoxide worden dus beïnvloed door de gedoteerde elementen.
EDS-karakterisering van aluminiumoxide-nanostaafjes-precursor gedoteerd met verschillende ionen
De EDS-resultaten laten zien dat Cr, Fe en Mg zijn gedoteerd in de aluminiumoxide-nanostaafjes-precursor met een molaire hoeveelheid van respectievelijk 2,06, 0,99 en 0,58% (tabel 3). Deze doteringshoeveelheid ligt dicht bij de toevoegingsdosering van het onzuiverheidselement (tabel 2), wat aangeeft dat de meeste onzuiverheidselementen zijn gedoteerd in de aluminiumoxide-nanostaaf-precursor. Ondertussen is voor het monster bereid uit chroomhoudend aluminiumoxideslib de gedoteerde molaire hoeveelheid Cr, Fe en Mg respectievelijk 2,11, 0,14 en 0,96%. De resultaten suggereren dat het grootste deel van Cr en Mg in het monster is gedoteerd, maar dat een kleine hoeveelheid Fe erin is gedoteerd. Het is mogelijk dat de doping van Fe wordt beperkt door de concurrentie van Cr en Mg.
XPS-karakterisering van nanometer-aluminiumoxidevezels gedoteerd met verschillende ionen
Afbeelding 5 toont de XPS-spectra van O1s en Al 2p . Zoals getoond in Fig. 5a, worden de pieken bij 531.90, 531.85, 531.15, 531.20 en 532,00 eV toegeschreven aan de ongedoteerde, Cr-gedoteerde, Fe-gedoteerde en Mg-gedoteerde aluminiumoxide nanostaafjes en het monster bereid uit de chroombevattende aluminiumoxideslib, respectievelijk. De pieken zijn toegewezen aan O 2− van de Al2 O3 [31]. Figuur 5b toont de pieken bij 74,00, 74,25, 74,75, 74,38 en 73,90 eV van Al 2p worden respectievelijk toegeschreven aan de bovenstaande monsters. De pieken worden toegeschreven aan Al 3+ van de Al2 O3 . Ondertussen worden de goede symmetrieën van de curve bewezen door Gauss-fitting, wat aangeeft dat er minder andere zuurstof en aluminium in de monsters worden gevormd. De O1s bindingsenergie (BE) van ongedoteerde en Cr-gedoteerde aluminiumoxide-nanostaafjes en het monster bereid uit het chroombevattende aluminiumoxideslib zijn bijna en hoger dan die van Fe-gedoteerde en Mg-gedoteerde monsters. De volgorde van de kleinste O1s BE gaat als volgt:Fe-gedoteerde, Mg-gedoteerde, Cr-gedoteerde, ongedoteerde aluminiumoxide nanostaafjes en het monster bereid uit het chroomhoudende aluminiumoxideslib. Echter, de Al 2p BE is in tegenstelling. XRD-resultaten laten zien dat een meer voorbijgaande toestand θ -Al2 O3 bevinden zich in de ongedoteerde en Cr-gedoteerde aluminiumoxide-nanostaafjes en het monster bereid uit het chroomhoudende aluminiumoxideslib, en meer α -Al2 O3 zijn in de Fe-gedoteerde en Mg-gedoteerde aluminiumoxide nanostaafjes. Vanwege het coördinatieformulier [AlO4 ] voor θ -Al2 O3 en [AlO6 ] voor α -Al2 O3 , is het mogelijk dat de O1s BE van [AlO6 ] is groter en Al 2p BE is kleiner dan die van [AlO4 ]. Bovendien zijn de roosterimperfecties van Al2 O3 worden veroorzaakt door Cr-, Fe- en Mg-ionen die Al2 . binnengaan O3 rooster. Dus de chemische toestanden van O en Al worden beïnvloed door het roosterdefect en de bindingsenergie wordt veranderd.
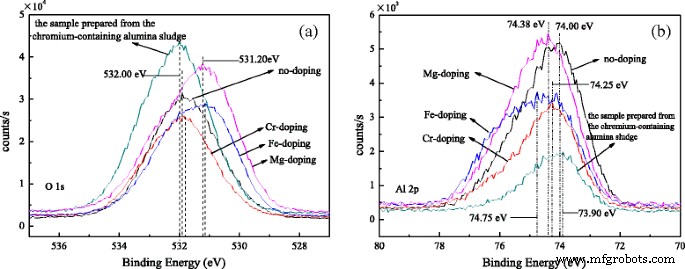
XPS-spectra van a O1s en b Al 2p voor aluminiumoxide nanostaafjes gedoteerd met verschillende ionen
Afbeelding 6 toont de XPS-spectra van het dopingion. Zoals weergegeven in figuur 6a, worden de pieken bij 589,80 en 578,52 eV toegewezen aan Cr 2p 1/2 en Cr 2p 3/2 van Cr(VI), en de pieken bij 587,53 en 577,39 eV worden toegewezen aan Cr 2p 1/2 en Cr 2p 3/2 van Cr(III). Het laat zien dat de Cr voorkomt in de met Cr gedoteerde aluminiumoxide nanostaafjes als Cr(VI) en Cr(III). Het meeste Cr komt echter voor als Cr(III) in het monster dat is bereid uit het chroomhoudende aluminiumoxideslib. Het geeft aan dat het deel van Cr(III) wordt geoxideerd tijdens het calcinatieproces in het met Cr gedoteerde monster, maar minder Cr(III) wordt geoxideerd in de monsters die zijn bereid uit het chroomhoudende aluminiumoxideslib. Voor de monsters die zijn bereid uit het chroomhoudende aluminiumoxideslib, omdat een chemische bindingscombinatie van Cr-O en het onzuivere metallische element wordt gevormd, is de elektrodepotentiaal van Cr 6+ /Cr 3+ wordt verhoogd bij hoge temperatuur, daarom weinig Cr(VI) in het monster. Zoals weergegeven in figuur 6b, worden de pieken bij 724,45 en 711,30 eV toegewezen aan Fe 2p 1/2 en Fe 2p 3/2 van Fe2 O3 , en 722.38 en 710.44 eV zijn toegewezen aan Fe 2p 1/2 en Fe 2p 3/2 van Fe3 O4 . De resultaten laten zien dat Fe in het Fe-dopingmonster voorkomt als Fe(II) en Fe(III). Er wordt gesuggereerd dat het Fe-element tijdens de synthese in het rooster van aluminiumoxidevoorloper wordt ingevoerd en plaatsvindt in het roosteraluminium. Bij het daaropvolgende calcinatieproces wordt een beetje Fe(III) gereduceerd tot Fe(II) door stof in de lucht te reduceren. Er zijn echter geen pieken van Fe in het monster dat is bereid uit het chroomhoudende aluminiumoxideslib, vanwege het geringe aantal Fe in het monster (tabel 3). Zoals weergegeven in Fig. 6c, worden de pieken bij 50,20 tot 50,34 eV toegewezen aan Mg 2p van MgO, wat suggereert dat Mg in het met Mg gedoteerde monster voorkomt als MgO. Echter, de piek van Mg 2p is zeer zwak in het monster dat is bereid uit het chroomhoudende aluminiumoxideslib. Het is mogelijk dat het Mg-gehalte zelden is. De resultaten komen overeen met de EDS. Volgens de resultaten van XRD, FT-IR en XPS wordt geïllustreerd dat de roosterimperfectie van doteringsmonsters met één element wordt gevormd door de onzuiverheden van het metalen element dat het rooster van aluminiumoxide binnendringt. Vanwege de concurrentie van meerdere elementen komt er echter meer Cr in het rooster van aluminiumoxide dat is bereid uit het chroomhoudende aluminiumoxideslib en worden er weinig Fe- en Mg-elementen ingevoerd.
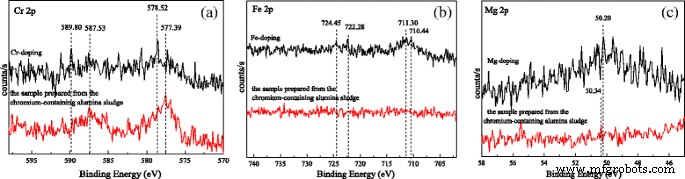
XPS-spectra van a Cr 3+ 2p , b Fe 3+ 2p , en c Mg 2+ 2p
Conclusies
Samenvattend werden de onzuiverheidselementen gedoteerd in nanostaafjes van aluminiumoxide, zoals Cr, Fe en Mg. De kristaltransformatie van aluminiumoxide wordt beperkt door het gedoteerde Cr en vergemakkelijkt door het gedoteerde Fe en Mg, dat wordt getransformeerd vanuit θ -Al2 O3 naar α -Al2 O3 in het calcinatieproces. Verder wordt de kristaltransformatie van aluminiumoxide sterk belemmerd door samen gedoteerde elementen uit het chroomhoudende aluminiumoxideslib. Het verloop van fasestructuurtransformatie, chemische binding, microstructuur en de chemische toestand van O en Al van de aluminiumoxide-nanostaafjes worden beïnvloed door de gedoteerde elementen. In het monster dat is bereid uit chroomhoudend aluminiumoxideslib, wordt de Fe-doping beperkt door de concurrentie van Cr en Mg. Deze studie suggereert dat nanostaafjes van aluminiumoxide kunnen worden bereid uit chroomhoudend aluminiumoxideslib om de kosten te verlagen en vervuiling te elimineren.
Afkortingen
- BE:
-
Bindende energie
- DSC:
-
Differentiële scanning calorimetrie analyse
- EDS:
-
Energie-dispersieve spectrometer
- FETEM:
-
Veldemissie transmissie-elektronenmicroscopie
- FT-IR:
-
Fourier-transformatie infraroodspectra
- HRTEM:
-
Transmissie-elektronenmicroscopie met hoge resolutie
- SAED:
-
Geselecteerd gebied elektronendiffractie
- TEM:
-
Transmissie-elektronenmicroscopie
- TG:
-
Thermogravimetrische analysator
- XPS:
-
Röntgenfoto-elektronenspectroscopie
- XRD:
-
Röntgenpoederdiffractie
Nanomaterialen
- Bereiding van reniumpoeder
- Bereidingsmethoden voor tantaalpoeder
- Conversie van decimale nummering
- Van elektrisch naar elektronisch
- 3 redenen om over te stappen van C naar C++
- Nanocellulose uit blauwgroene algen
- BSA-gecoate gouden nanostaafjes voor NIR-II fotothermische therapie
- Preparatie en magnetische eigenschappen van kobalt-gedoteerde FeMn2O4-spinel-nanodeeltjes
- Op weg naar TiO2-nanovloeistoffen:deel 1:voorbereiding en eigenschappen
- Kleine hoekverstrooiing van vetfractalen op nanoschaal
- Van UI naar AI:een automatiseringsreis



