Kunstmatig hart
Achtergrond
Een natuurlijk hart heeft twee pompen, elk met twee kamers. De rechterboezem pompt zuurstofarm bloed uit het lichaam naar de rechterkamer, die het naar de longen pompt. Het linker atrium stuurt belucht bloed van de longen naar de linker hartkamer, die het naar het lichaam pompt. Bij elke hartslag trekken de twee atria samen, gevolgd door de grote ventrikels.
Congestief hartfalen, het gestaag afnemende vermogen van het hart om bloed rond te pompen, is een van de belangrijkste doodsoorzaken. Deze ziekte wordt veroorzaakt door plotselinge schade door hartaanvallen, verslechtering door virale infecties, klepstoringen, hoge bloeddruk en andere problemen. Volgens de American Heart Association leven naar schatting vijf miljoen Amerikanen met hartfalen en worden elk jaar meer dan 400.000 nieuwe gevallen gediagnosticeerd. Ongeveer 50% van alle patiënten overlijdt binnen vijf jaar. Hartziekten hebben de gezondheidsindustrie in de Verenigde Staten in 1998 ongeveer $ 95 miljard gekost.
Hoewel medicatie en chirurgische technieken de symptomen kunnen helpen beheersen, is de enige remedie voor hartfalen een orgaantransplantatie. In 1998 stonden ongeveer 7.700 Amerikanen op de nationale harttransplantatielijst, maar slechts 30% kreeg een transplantatie. Kunstharten en pomphulpmiddelen zijn dus ontwikkeld als mogelijke alternatieven.
Een kunsthart houdt de bloedcirculatie en zuurstofvoorziening van het hart gedurende verschillende perioden in stand. Het ideale kunsthart moet elke 24 uur 100.000 keer kloppen zonder dat er smering of onderhoud nodig is en moet een constante stroombron hebben. Het moet ook sneller of langzamer pompen, afhankelijk van de activiteit van de patiënt, zonder infectie of bloedstolsels te veroorzaken.
De twee belangrijkste soorten kunstmatige harten zijn de hart-longmachine en het mechanische hart. Het eerste type bestaat uit een oxygenator en een pomp en wordt voornamelijk gebruikt om het bloed te laten stromen terwijl het hart wordt geopereerd. Deze machine kan maar een paar uur werken, omdat het bloed na langere tijd beschadigd raakt.
Een mechanisch hart is ontworpen om de totale werklast te verminderen van een hart dat niet langer op zijn normale capaciteit kan werken. Deze harten bestaan uit apparatuur die het bloed tussen de hartslagen door pulseert of een kunstmatige hulpventrikel (linkerventrikelhulpapparaat, LVAD) gebruikt die een deel van de normale cardiale output pompt. Omdat dergelijke inrichtingen gewoonlijk leiden tot complicaties voor de patiënt, zijn ze in het algemeen gebruikt als tijdelijke vervanging totdat natuurlijke harten voor transplantatie kunnen worden verkregen. Wereldwijd zijn ongeveer 4.000 LVAD's geïmplanteerd. De markt voor deze apparaten wordt geschat op $ 12 miljard per jaar in de Verenigde Staten.
Geschiedenis
Sinds het einde van de negentiende eeuw hebben wetenschappers geprobeerd een mechanisch apparaat te ontwikkelen dat zuurstof in het bloed kan herstellen en overtollige koolstofdioxide kan verwijderen, evenals een pomp om de hartwerking tijdelijk te verdringen. Het duurde bijna 100 jaar voordat John H. Gibbon Jr. in 1953 de eerste succesvolle hart-longmachine op een mens gebruikte. Vier jaar later werd het eerste kunstmatige hart (gemaakt van plastic) in de westerse wereld in een hond geïmplanteerd . Het Nationaal Hartinstituut 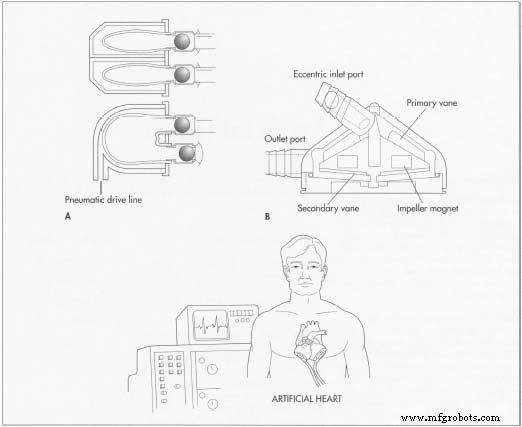 A. Een pneumatisch kunsthart. B. Een gyro centrifugaal kunsthart. richtte het kunsthartprogramma op in 1964, wat leidde tot het eerste totale kunstmatige hart voor menselijk gebruik dat in 1969 werd geïmplanteerd.
A. Een pneumatisch kunsthart. B. Een gyro centrifugaal kunsthart. richtte het kunsthartprogramma op in 1964, wat leidde tot het eerste totale kunstmatige hart voor menselijk gebruik dat in 1969 werd geïmplanteerd.
De nadruk verschoof in 1970 naar linkerventrikelhulpsystemen en bloedcompatibele materialen. In datzelfde jaar werd met succes een LVAD gebruikt. De ontwikkeling van de bloedpomp ging echter door en apparaten werden kleiner, lichter, acceptabeler en klinisch succesvol. Een aantal polyurethaan en kunststof pompen met een lange levensduur werden ook ontwikkeld. In de jaren tachtig legde de Food and Drug Administration (FDA) strengere regels op aan de Medical Devices Standards Act, wat leidde tot hogere ontwikkelingskosten. Veel onderzoeksgroepen moesten afhaken, nu zijn er nog maar een paar over.
De beroemdste wetenschapper is misschien wel Dr. Robert Jarvik, die een kunsthart uitvond, de Jarvik-7. Dit apparaat, gemaakt van aluminium en plastic, verving de twee onderste kamers van het natuurlijke hart en gebruikte twee rubberen membranen voor de pompwerking. Een externe compressor ter grootte van een koelkast zorgde ervoor dat het kunstmatige hart bleef kloppen. Barney Clark was de eerste patiënt die dit hart ontving. Hij overleefde 112 dagen voordat fysieke complicaties veroorzaakt door het implantaat hem het leven kostte. In 1986 werd William Schroeder de tweede Jarvik-7-ontvanger en overleefde hij ongeveer 20 maanden.
De medische gemeenschap realiseerde zich dat een volledig implanteerbaar hart de mobiliteits- en infectieproblemen veroorzaakt door de Jarvik-7 zou kunnen voorkomen. In 1988 begonnen de National Institutes of Health de ontwikkeling van dergelijke harten te financieren en steunden ze een dergelijk programma in 1991 voor een totaalbedrag van $ 6 miljoen. Drie jaar later kwam een elektrische en batterijgevoede implanteerbare LVAD beschikbaar. In 1999 werd Charlie Chappis de eerste patiënt die ooit met een dergelijk apparaat uit een ziekenhuis werd ontslagen. Andere kunstmatige harten van verschillende ontwerpen worden momenteel getest.
Grondstoffen
Een kunsthart of LVAD is gemaakt van metaal, plastic, keramiek en dierlijke onderdelen. Voor de pomp en andere metalen onderdelen wordt een titanium-aluminium-vanadium-legering gebruikt omdat deze biocompatibel is en geschikte structurele eigenschappen heeft. De titanium onderdelen worden gegoten in een gespecialiseerde titanium processor. Behalve voor bloedcontactoppervlakken, wordt het titanium machinaal bewerkt tot een specifieke afwerking. Bloedcontactoppervlakken krijgen een speciale coating van titaniummicrosferen die permanent aan het oppervlak hechten. Met deze coating hechten bloedcellen zich aan het oppervlak, waardoor een levende voering ontstaat.
Een met bloed in contact komend diafragma in de pomp is gemaakt van een speciaal type polyurethaan dat ook getextureerd is om te zorgen voor hechting aan de bloedcellen. Twee buisvormige transplantaten zijn gemaakt van polyester (die worden gebruikt om het apparaat aan de aorta te bevestigen) en de kleppen zijn echte hartkleppen die uit een varken zijn verwijderd. Andere onderdelen waaruit de motor bestaat, zijn gemaakt van titanium of andere metalen en keramiek.
Ontwerp
Er zijn verschillende kritieke problemen bij het ontwerpen van een LVAD. De vloeistofdynamiek van de bloedstroom moet worden begrepen, zodat er voldoende bloed wordt rondgepompt en er geen bloedstolsels ontstaan. Er moeten materialen worden gekozen die biocompatibel zijn; anders kan de pomp defect raken. Het rendement van de motor moet worden geoptimaliseerd zodat er zo min mogelijk warmte wordt gegenereerd. Vanwege mogelijke afkeuring moeten het totale volume en het oppervlak van het gehele apparaat zo klein mogelijk worden gehouden. Een typische LVAD weegt ongeveer 2,4 lb (1.200 g) en heeft een volume van 1,4 pinten (660 ml).
 Or. Robert Jarvik.
Or. Robert Jarvik.
Robert Jarvik werd geboren op 11 mei 1946 in Midland, Michigan, en groeide op in Stamford, Connecticut. Hij ging in 1964 naar de Syracuse University in New York, waar hij architectuur en mechanisch tekenen studeerde. Nadat zijn vader een hartziekte kreeg, schakelde Jarvik over op premedicatie. Hij studeerde in 1968 af met een bachelor of arts in zoölogie, maar werd afgewezen door medische scholen in de Verenigde Staten. Hij ging naar de Universiteit van Bologna in Italië, maar vertrok in 1971 naar de New York University, waar hij een master of arts in beroepsbiomechanica behaalde.
Jarvik solliciteerde naar een baan bij de Universiteit van Utah. De directeur van het Instituut voor Biomedische Technologie en Afdeling Kunstmatige Organen, Willem Kolff, was sinds het midden van de jaren vijftig bezig met het ontwikkelen van een kunsthart. Jarvik begon als zijn laboratoriumassistent en behaalde zijn medische graad in 1976.
Op 2 december 1982 transplanteerden artsen het eerste kunstmatige hart in een mens. Dit apparaat van plastic en aluminium, de Jarvik-7, werd geïmplanteerd in Barney Clark, die het na de operatie nog 112 dagen overleefde. Verschillende andere patiënten kregen Jarvik-7-harten, maar geen enkele leefde meer dan 620 dagen. De belangrijkste voordelen waren dat er niet gewacht moest worden op een mensenhart en dat er geen kans was op afwijzing. De voor de hand liggende valkuil is dat patiënten voor altijd via buizen verbonden waren met een persluchtmachine.
De Jarvik-7 werd uiteindelijk gebruikt als noodmaatregel voor patiënten die wachtten op een natuurlijk hart en bood hoop dat er niet op transplantaties zou worden gewacht. In 1998 werkte Jarvik verder aan een op zichzelf staand apparaat om worden geïmplanteerd in het zieke hart van een persoon om het correct te laten functioneren.
Het fabricageproces
-
1 De meeste componenten worden gemaakt volgens aangepaste specificaties door externe fabrikanten, waaronder machinewerkplaatsen en fabrikanten van printplaten. De varkenskleppen worden in de transplantaten genaaid met hechtingen bij een bedrijf in medische hulpmiddelen dat gespecialiseerd is in hartkleppen.
Zodra alle componenten zijn verkregen, wordt het LVAD-systeem geassembleerd en getest om ervoor te zorgen dat elk apparaat aan alle specificaties voldoet. Eenmaal getest, kan de LVAD worden gesteriliseerd en verpakt voor verzending.
Het vormen van de polyurethaan onderdelen
- 2 Sommige fabrikanten van kunstmatige harten maken hun eigen onderdelen van polyurethaan. Eén proces maakt gebruik van een gepatenteerde vloeibare oplossing die laag voor laag op een keramische doorn wordt gegoten. Elke laag wordt verwarmd en gedroogd totdat de gewenste dikte is bereikt. Het onderdeel wordt vervolgens van de doorn verwijderd en geïnspecteerd. Anders gebruikt een externe fabrikant een spuitgiet- of vacuümgietproces in combinatie met radiofrequentielassen.
Montage
- 3 Elk kunsthart heeft meerdere dagen nodig om in elkaar te zetten en te testen. Het assemblageproces wordt uitgevoerd in een cleanroom om contaminatie te voorkomen. Elk kunsthart bestaat uit maximaal 50 componenten die met speciale lijmen in elkaar zijn gezet. Deze lijmen vereisen uitharding bij hoge temperaturen. Verschillende montagehandelingen vinden parallel plaats, waaronder de montage van de motorbehuizing en componenten, de montage van de percutane buis en de bevestiging van de duwplaten aan het polyurethaanmembraan. Deze subsystemen worden individueel geïnspecteerd, waarna de eindmontage van het complete systeem plaatsvindt. De grafts worden afzonderlijk gemonteerd en tijdens de operatie bevestigd.
Testen
- 4 Nadat de montage is voltooid, wordt elk apparaat getest met behulp van speciale apparatuur die de druk in het lichaam simuleert. Alle elektronische componenten worden getest met elektronische testapparatuur om de goede werking van alle circuits te garanderen.
Sterilisatie/verpakking
- 5 Nadat het kunsthart is getest en geslaagd is, wordt het naar een externe dienst gestuurd voor sterilisatie. Elk apparaat wordt verzegeld in plastic bakjes en teruggestuurd naar de fabrikant van het hart. Het wordt vervolgens verpakt in op maat gemaakte koffers om het te beschermen tegen besmetting en schade te voorkomen.
Kwaliteitscontrole
De meeste onderdelen hebben de keuring al doorstaan voordat ze bij de hartfabrikant aankomen. Sommige componenten worden nog steeds dimensioneel geïnspecteerd omdat ze nauwe toleranties vereisen - in de orde van grootte van een miljoenste van een inch, waarvoor speciaal meetgereedschap nodig is. Om te voldoen aan de FDA-voorschriften, wordt elk onderdeel (inclusief lijmen) dat in het proces wordt gebruikt, gecontroleerd op lot- en serienummer, zodat traceringsproblemen mogelijk zijn.
Bijproducten/afval
Schroot titanium wordt teruggewonnen en gerecycled na omsmelten en hergieten. Anders wordt er weinig afval geproduceerd, aangezien de meeste componenten de inspectie hebben doorstaan voordat ze de verschillende fabrikanten verlaten. Andere defecte onderdelen worden weggegooid. Zodra een apparaat door een patiënt is gebruikt, wordt het teruggestuurd naar de fabrikant van het hart voor analyse om het ontwerp te verbeteren.
De Toekomst
De komende tien jaar komen er een aantal nieuwe toestellen op de markt. Onderzoekers van de Pennsylvania State University ontwikkelen een elektromechanisch hart dat wordt aangedreven door radiofrequentie-energie die door de huid wordt uitgezonden. Een motor drijft drukplaten aan, die afwisselend drukken tegen plastic met bloed gevulde zakjes om pompen te simuleren. Patiënten hebben overdag een batterij bij zich en slapen terwijl het apparaat is aangesloten op een stopcontact. Dit kunsthart zal tegen 2001 op mensen worden getest.
Verschillende onderzoeksgroepen ontwikkelen pompen die het bloed continu laten circuleren, in plaats van een pompende werking te gebruiken, omdat deze pompen kleiner en efficiënter zijn. In Australië ontwikkelt Micromedical Industries Limited een roterende bloedpomp met continue stroom, die naar verwachting in 2001 in een mens zal worden geïmplanteerd. De afdeling cardiologie van de Ohio State University ontwikkelt een plastic pomp ter grootte van een hockeypuck die zelfregulerend is. Deze pomp wordt gedurende enkele weken bij patiënten geïmplanteerd totdat hun eigen hart herstelt.
Thermo Cardiosystems, Inc. werkt ook aan een LVAD met een roterende pomp met continue stroom), die naar verwachting ergens in 2000 zal worden geïmplanteerd, en een LVAD met een centrifugaalpomp met continue stroom. De laatste bevindt zich nog in een vroege ontwikkelingsfase, maar het is de bedoeling dat het 's werelds eerste lagerloze pomp wordt, wat betekent dat er geen onderdelen zullen zijn die slijten. Dit wordt bereikt door de rotor van de pomp magnetisch op te hangen. Beide apparaten zullen beschikbaar zijn met transcutane energieoverdracht, wat betekent dat de apparaten volledig implanteerbaar zullen zijn.
Nu er minder donorharten beschikbaar komen, ontwikkelen anderen ook een kunsthart dat een permanente vervanging is. Deze vervangingen kunnen de vorm hebben van een hulpmiddel voor de linkerventrikel of een volledig kunsthart, afhankelijk van de fysieke conditie van de patiënt. LVAD's worden ontwikkeld door uitvinder Robert Jarvik en de bekende hartchirurg Michael DeBakey. Total kunstmatige harten worden gezamenlijk ontwikkeld door het Texas Heart Institute en Abiomed, Inc. in Massachusetts. In Japan ontwikkelen onderzoekers totale kunstharten op basis van een siliconen kogelkraansysteem en een centrifugaalpomp met een lagersysteem gemaakt van aluminiumoxide-keramiek en polyethyleencomponenten.
Alternatieven voor kunstharten en hartpompen zijn ook in ontwikkeling. Zo is er een speciale klem uitgevonden die de vorm van een ziek hart verandert, wat naar verwachting de pompefficiëntie tot 30% zal verbeteren. Een dergelijk apparaat vereist minimaal invasieve chirurgie om te implanteren.
Productieproces



