Experimentele studie van 5-fluorouracil ingekapselde ethosomen gecombineerd met CO2 fractionele laser om hypertrofisch litteken te behandelen
Abstract
Doelstelling
Deze studie is bedoeld om de permeabiliteit te onderzoeken van ethosomen ingekapseld met 5-florouracil (5-FU) gemedieerd door CO2 fractionele laser op hypertrofische littekenweefsels. Bovendien, therapeutisch en langdurig effect van CO2 fractionele laser gecombineerd met 5-FU ingekapselde ethosomen in hypertrofisch littekenmodel van konijnenoor zal worden geëvalueerd.
Methoden
De doorgedrongen hoeveelheid 5-FU en retentiegehalten van 5-FU werden beide bepaald door middel van hogedrukvloeistofchromatografie (HPLC). Fluorescentie-intensiteiten van ethosomen ingekapseld met 5-FU (5E) gelabeld met Rodanmin 6GO (Rho) werden gemeten met confocale laser scanning microscopie (CLSM). De permeabiliteitsbevordering van 5E gelabeld met Rho in hypertrofisch litteken van konijnenoor gemedieerd door CO2 fractionele laser werd geëvalueerd op 0 uur, 6 uur, 12 uur, 24 uur, 3 dagen en 7 dagen na de bestraling. De openingssnelheden van de microkanalen werden berekend volgens CLSM. Het therapeutische effect van 5EL werd in vivo geëvalueerd op hypertrofisch litteken in konijnenoor. De relatieve dikte van het hypertrofische litteken van konijnenoor voor en na de behandeling werd gemeten met de schuifmaatmethode. Littekenverhogingsindex (SEI) van hypertrofisch litteken in konijnenoor werd gemeten met H&E-kleuring.
Resultaten
De gegevens toonden aan dat de penetratiegraad van de 5EL-groep hoger was dan die van de 5E-groep (4.15 ± 2.22 vs. 0.73 ± 0.33; p < 0,05) na behandeling van 1 uur. Bovendien was de penetratiegraad van 5EL hoger dan die van de 5E-groep (107,61 ± 13,27 vs. 20,73 ± 3,77; p < 0,05) na een behandeling van 24 uur. De retentie-inhoud van de 5EL-groep vertoonde ook een hoger niveau dan de 5E-groep (24.42 ± 4.37 vs.12.25 ± 1.64; p < 0.05). De fluorescentie-intensiteit van Rho in hypertrofische littekenweefsels van de 5EL-groep was op verschillende tijdstippen (1, 6 en 24 uur) hoger dan die van de 5E-groep. De openingssnelheid van de microkanalen werd binnen 24 uur geleidelijk verlaagd en de microkanalen werden 3 dagen na de bestraling met CO2 volledig gesloten fractionele laser. De relatieve dikte en SEI van hypertrofisch litteken van konijnenoor na 7 dagen behandeling in de 5EL-groep waren significant lager dan in de 5E-groep.
Conclusie
CO2 fractionele laser gecombineerd met topische 5E kan effectief zijn bij de behandeling van hypertrofisch litteken in vivo en een nieuwe therapiemethode leveren voor menselijk hypertrofisch litteken.
Achtergrond
Hypertrofisch litteken is een huidaandoening die wordt gekenmerkt door afzettingen van overmatige hoeveelheden collageen die aanleiding geven tot een verheven litteken, maar waarbij de waargenomen mate van keloïden niet wordt bereikt [1]. In de ontwikkelde landen ontwikkelden elk jaar in totaal 100 miljoen patiënten littekens, als gevolg van 55 miljoen electieve operaties en 25 miljoen operaties na een trauma [2]. Na een chirurgische ingreep ontwikkelde ongeveer 60% van de patiënten postoperatief hypertrofische littekens, meestal gedurende de eerste 3 maanden. De meeste hypertrofische littekens zijn 12 maanden na chirurgische ingrepen nog steeds hypertrofisch [3]. Momenteel omvatten de gebruikelijke behandelmethoden chirurgische en niet-chirurgische behandelingen. Druk, bestralingstherapie, chemotherapie en andere medicamenteuze chirurgische behandelingen zijn de belangrijkste therapiebehandelingen. Tot nu toe konden deze therapieën niet het gewenste therapeutische effect bereiken vanwege hun gebreken [4, 5]. Medicamenteuze therapie is een van de meest voorkomende niet-chirurgische behandelingen voor pathologisch litteken tot uitwendige verf op basis van lokale injecties. Vanwege de bijwerkingen van geneesmiddelen zijn lokale injecties vaak beperkt tot kleinschalige en laaggedoseerde behandelingen. Bovendien konden lokale medicijninjecties, vanwege de korte halfwaardetijd van het medicijn, altijd geen langdurige hoge concentraties op littekens handhaven; daarom zijn vaak herhaalde injecties nodig [6]. Gezien de dichtheid van littekenweefsel en ernstige pijn, is injectie over het algemeen niet acceptabel voor patiënten. Ondanks de voordelen, waaronder pijnloos, geen bijwerking voor de lever en handig voor langdurig uitwendig gebruik [7, 8], konden medicijnen het litteken niet binnendringen vanwege de speciale organisatiestructuur van pathologische littekens. Recente rapporten gaven ook aan dat lokale medicatie moeilijk door het littekenweefsel kan dringen [9]. Dus het externe gebruik voor drugs is momenteel beperkt.
Ethosomen zijn een nieuwe lipidedrager die door Touitou in 2000 [10] werd gebruikt en die effectief is bij het afleveren van medicijnen via de huid. Het hoofdbestanddeel van ethosomen is ethanol, dat de strakke opstelling van cuticula-lipidemoleculen kan veranderen, de vloeibaarheid van lipiden kan verbeteren en de flexibiliteit en mobiliteit van het ethanolliposoommembraan kan bevorderen. Ethanol uit ethosomen kan ook de vervorming van het stratum corneum versnellen en het draag- en penetratievermogen van het geneesmiddel door een verstoord stratum corneum in de huid verbeteren [11,12,13]. Omdat littekenweefsel echter anders is dan normaal huidweefsel, heeft het een speciale structuur. In onze vorige studie hebben we aangetoond dat ethosomen een zeer efficiënte drager zijn van geneesmiddelen in menselijke littekens [14]. Het is onontbeerlijk dat het medicijn in littekenweefsel niet goed wordt verdeeld, maar aanzienlijk wordt verminderd van de buitenkant naar de binnenkant van de huid. Het geneesmiddel hoopt zich voornamelijk op in de epidermis en de oppervlakkige laag van de dermis, maar niet in alle lagen van de dermis, wat het anti-littekeneffect vermindert.
Ablatieve fractionele lasertherapie, een cosmetische technologie, is een zeer populaire en algemeen aanvaarde modaliteit die momenteel en voornamelijk wordt gebruikt voor de klinische behandeling van rimpels in het gezicht, oppervlakkige littekens, pigmentatiestoornissen en het verbeteren van de huidtextuur [15,16,17]. Gebaseerd op de dot-matrix fotothermolysetheorie [18], produceert ablatieve fractionele laser een array-achtige opstelling van een kleine laserstraal en verstoort de huidbarrière door ablatieve microscopische verticale kanalen te creëren die worden omgeven door een zone van thermische schade, waardoor een wondgenezingsreactie wordt opgewekt bij een matige huid uiterlijk [19,20,21,22]. Er is gemeld dat de belangrijkste barrière voor percutane absorptie van geneesmiddelen het stratum corneum is [23, 24]. Recente onderzoeken hebben aangetoond dat een van de meest gebruikte klinische ablatieve fractionele lasers, CO2 fractionele laser kan het stratum corneum afbreken en dichte microporeuze kanalen vormen, waardoor de belangrijkste barrière wordt ondermijnd die de percutane absorptie van het geneesmiddel belemmert en goede transdermale geneesmiddelpenetratie bevordert, wat de vooruitzichten bevordert [25,26,27,28].
In deze studie hebben we CO2 . onderzocht fractionele laser-gemedieerde ethosomale gel met anti-littekenmedicijn 5-florouracil (5-FU) in menselijke littekenmonsters en hypertrofisch littekenmodel in konijnenoor. Met behulp van deze nieuwe aanpak hebben we ons gericht op het verbeteren van de efficiëntie van de toediening van geneesmiddelen tegen littekens om het lange littekenbehandelingsproces te verkorten. Voor het eerst is een hypertrofisch littekenmodel van konijnenoor toegepast om CO2 . te bepalen fractionele laser-gemedieerde ethosomen op nanoschaal die 5-FU dragen op hypertrofische littekens en het penetratie-effect van geneesmiddelen. Samen is gesuggereerd dat CO2 fractionele laser gecombineerd met topische medicatie levert een nieuwe therapiemethode voor humaan hypertrofisch litteken.
Methoden
5-FU ingekapselde ethosomen
Touitou's methode [10] werd gebruikt als voorbereiding voor 5-FU ingekapselde ethosomen. Deeltjesgrootteverdeling van 25°C en polydispersiteitsindex (PDI) werden bepaald met behulp van laserdeeltjesgrootte-analysator (λ = 632.8 nm). PDI < 0.1 geeft de gelijkmatige deeltjesgrootteverdeling aan, en PDI> 0.3 suggereert een inhomogene deeltjesgrootteverdeling. Transmissie-elektronenmicroscopie (TEM) werd gebruikt voor de observatie van de morfologie van ethosomen. Ultracentrifugatiemethode [29] werd gebruikt voor het meten van de inkapselingsefficiëntie (EE) van ethosomen in deze studie.
Hoge prestatie vloeistofchromatografie
De concentratie van 5-FU in het receptorcompartiment van de Franz-cellen werd bepaald door een Waters 2695 HPLC-systeem (Meadows Instrumentation, Illinois) en 2487 ultraviolette detector met een omgekeerde-fase Diamonsil TM C18-kolom (250 mm × 4,6 mm, 5 μm ). 5-FU werd gedetecteerd bij 265 nm met een mobiele fase van methanol–H2 O (5:95 v /v ) met een stroomsnelheid van 1 ml/min. De gegevens zijn geanalyseerd per piekgebied en de externe standaardmethode, met behulp van een Waters Empower System.
Confocale laserscanmicroscopie
Menselijk hypertrofisch littekenweefsel werd geanalyseerd met confocale laser scanning microscopie (CLSM) in stappen van 10 μm. Fluorescentie-intensiteit werd geanalyseerd met behulp van een laserscanmicroscoop LSM 510 (Zeiss, Jena, Duitsland) met een Fluar 10 ×, 0, 5 objectief met numerieke apertuur. Optische excitatie werd uitgevoerd met een 543-nm HeNe-laser en fluorescentie-emissie werd gedetecteerd boven 560 nm voor rhodamine 6GO (Rho). Afbeeldingen werden geanalyseerd met Release Version 4.0 SP2 beeldanalysesoftware om de fluorescentiedistributie en fluorescentie-intensiteit van littekenweefsel te berekenen. In 10 × 10 keer het gezichtsveld, moesten de grootte en distributie van de pixelwaarden het penetratiebereik van 5-FU EG (gelabeld met Rho) bepalen en met een semi-kwantitatieve methode.
5-FU ethosomen permeabiliteitstest in menselijk littekenweefsel
Menselijke hypertrofische littekenspecimens van het Shanghai Jiaotong University Affiliated Ninth People's Hospital of Plastic Surgery zijn afkomstig van littekenexcisie bij patiënten met drie gevallen, alle vrouwen, in de leeftijd van 21-35 jaar; het litteken bevindt zich op de schouder en rug; hypertrofisch littekenverloop van 6 maanden tot 1 jaar; integriteit van littekenweefsel; geen ulceratie; geen infectielaesies; en het laagste litteken moet ook hoger zijn dan de huid, en de patiënt heeft sinds de ziekte geen behandeling gekregen. Algemene anesthesie werd gebruikt om het effect van lokale anesthetica op littekenweefsel te elimineren. De verkregen monsters werden onmiddellijk verwijderd uit het onderhuidse weefsel, beschermden de epidermis, maakten een dikte van 4,0 mm, een gebied van 3 cm × 3 cm littekenweefselmonsters, gewassen met zoutoplossing bij kamertemperatuur, gedroogd met gaas droog oppervlaktevocht, verpakt met aluminiumfolie en bewaard in de koelkast bij -20 °C. Menselijk hypertrofisch littekenweefsel werd vóór gebruik verwijderd en bewaard in een vriezer bij -20 ° C. Humaan hypertrofisch littekenweefsel werd gedurende 2 uur ondergedompeld in pH 7,4 PBS bij 25 ° C en het water op het weefseloppervlak werd voorzichtig verwijderd met droog gaas. Alle epidermale weefselgebieden van hypertrofisch littekenweefsel waren CO2 fractionele laser bestraald. Laserparameters worden onmiddellijk gevolgd door DeepFX-modus, 25 mj energiedichtheid, 20% dekking, 300 Hz emissiefrequentie, op de 10e spotgrootte en zonder overlap. Alle bestraalde monsters werden verzameld met behulp van HPLC-detectie om het littekenweefselgehalte van 5-FU te bepalen. Histopathologische secties worden onmiddellijk gebruikt voor CLSM-assay.
Konijnenoor hypertrofisch littekenmodel
De methode van het hypertrofische littekenmodel van konijnenoor werd hieronder kort beschreven:12 witte konijnen uit Nieuw-Zeeland, mannelijk, en met een gewicht van 2 kg (SLAC, Shanghai) werden gedurende 2 weken apart gehuisvest. Voor konijnenanesthesie werd lumianning gemengd met 1,5 mg ketamine per 100 g gewicht via intramusculaire injectie. Alle wonden waren omgeven door het centrale punt van de konijnenoren. Elke ronde wond met een diameter van 1 cm was defect en vervolgens werd het perichondrium verwijderd. Achtentwintig dagen na de operatie krabde het konijnenoor van de wond en genas volledig, met een zichtbare diameter van ongeveer 0,9 cm hypertrofische littekens. Het litteken was felrood, er zaten bulten op de huid rond de duidelijke hyperplasie en het litteken was dik en hard.
Bepaling van openingspercentages voor microkanalen
Verschillende tijdstippen na CO2 fractionele laserbehandeling in konijnenoor hypertrofisch littekenmodel, rode fluorescentie Rodanmin 6GO met ethosomen werd toegepast op littekenweefsel. Drie uur later werd CLSM gebruikt voor het bepalen van de kanaalopeningssnelheid. Kanaalopeningspercentage =open kanaalnummer/(open kanaalnummer + gesloten kanaalnummer) × 100%. Het percentage van de kanaalopeningssnelheid weerspiegelt het effect van CO2 fractionele laserpenetratie effectiviteit.
H&E-kleuring
In het algemeen worden konijnen opgeofferd met 10% pentobarbital i.v. injectie (dosis van 5 maal de normale dosis voor anesthesie, 35 mg/kg). Verwijder de monsters onmiddellijk en ga verder met de H&E-kleuringsstap. De hematoxyline- en eosinekleuringsmethode is volgens het standaard H&E-kleuringsprotocol.
Littekenhoogte-index en relatieve diktebepaling
Achtentwintig dagen na inductie van hypertrofische littekens van konijnenoor, worden vier interventiegroepen uitgevoerd:5EL-groep:enthosomale gels ingekapseld met 5-FU gecombineerd met CO2 fractionele laser; 5E groep:de enthosomale gels ingekapseld met 5-FU; CO2 groep:CO2 fractionele laserbehandeling; en controlegroep. We definieerden A als dikte van het dikste deel van hypertrofisch littekenweefsel van konijnenoor, en B als dikte van 1,0 cm verwijderd van het dikste deel van hypertrofisch littekenweefsel van konijnenoor (dicht bij het middelpunt). De relatieve dikte wordt berekend door A/B. Dermale littekenhypertrofie werd geïllustreerd door de SEI. SEI =het gebied van nieuw gevormde dermis/het gebied van niet-verwonde dermis. SEI> 1.5 toont een hypertrofisch litteken.
Statistieken
Alle experimenten werden drie keer herhaald. Gegevens worden weergegeven als gemiddelde ± standaarddeviatie (SD). Statistische analyse werd uitgevoerd met behulp van SPSS versie 19.0 (SPSS Inc., Chicago, VS). Studenten t test gebruikt om de significantie te berekenen. *p waarde < 0,05 werd als statistisch significant beschouwd; **p waarde < 0,01 werd als statistisch zeer significant beschouwd; ***p waarde < 0,001 werd als statistisch extreem significant beschouwd, en ****p waarde < 0.0001 werd als statistisch zeer extreem significant beschouwd.
Resultaten
Kwaliteitsbeoordeling van ethosomen ingekapseld met 5-florouracil(5E)
Allereerst, om de kwaliteit van ethosomale gel ingekapseld met 5-florouracil (5E) te valideren, werden de morfologie en diameters gedetecteerd door transmissie-elektronenmicroscoop (TEM) observatie. Ethosomen in suspensievorm vormden een complete cirkel of ovaal-bolvormig blaasje van universele grootte, dat onder een microscoop minder dan 100 nm is (figuur 1a-b). Na gelformulering bleven ethosomen intact (Fig. 1c-d). Met behulp van laserdeeltjesgrootte-analysator lijken ethosomen in suspensietoestand een diameter van 87,72 ± 9,27 nm te hebben, en de PDI was 0,10 ± 0,01. Ondertussen was de deeltjesgrootte van de ethosomen 98,78 ± 10,88 nm en PDI was 0,11 ± 0,02. Een statische vergelijking laat zien dat de deeltjesgrootte geen significant verschil heeft (p> 0,05). Bovendien hadden beide PDI's geen significant verschil (p> 0,05). Bovendien toonden de gegevens verkregen uit de laserdeeltjesgrootte-analysator en TEM de vergelijkbare resultaten. Bovendien werd de insluitingswerkzaamheid (EE) ook bepaald met behulp van de ultracentrifugatiemethode (tabel 1). De resultaten toonden aan dat EE van ethosomale suspensie 10,47 ± -1,47% was en EE van ethosomale gel 11,56 ± -1,12% (n = 6), zonder betekenis (p> 0,05). Concluderend werden er geen veranderingen in morfologie en deeltjesgrootte gevonden in suspensietoestand en geltoestand van ethosomen.
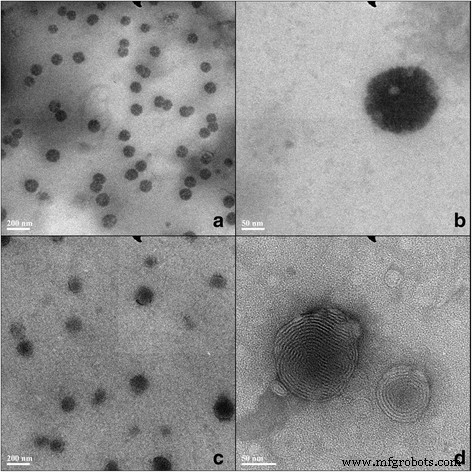
Transmissie-elektronenmicroscoopbeelden van 5-FU-ethosomen. Ethosomen van oplossingen (a en b ) en ethosomen van gel (c en d )
CO2 Fractionele laser bevordert de doorlaatbaarheid van 5E door hypertrofische littekens in vitro
Na evaluatie van de kwaliteit van ethosomen ingekapseld met 5-florouracil (5-FU), onderzochten we de permeabiliteit ervan in menselijke hypertrofische littekens met of zonder CO2 fractionele laser in vitro. Humaan hypertrofisch littekenweefsel werd bestraald met CO2 fractionele laser en vervolgens werd 5E gelijkmatig aangebracht. De cumulatieve concentraties van 5-FU werden bepaald op 1, 3, 6, 10, 16 en 24 uur door HPLC (2). We vergeleken 5-FU cumulatieve concentraties van CO2 fractionele laser gecombineerd met ethosomen ingekapseld met 5-florouracil (5EL) groep en 5E groep op verschillende tijdstippen. Na 1 uur was de 5-FU cumulatieve concentratie van de 5EL-groep 4,15 ± 2,22 μg/ml/cm 2 , die hoger was dan de concentratie van de 5E-groep (0,73 ± 0,33 μg/ml/cm 2 , p < 0,001). Bij de langdurige behandeling (24 uur), 5-FU cumulatieve permeatieconcentratie van de 5EL-groep (107,61 ± 13,27 μg/ml/cm 2 ) was ook hoger dan die van de 5E-groep (20,73 ± 3,77 μg/ml/cm 2 , p < 0,0001). Op de eerdere tijdstippen, 3, 6, 10 en 16 uur, vertoonden de 5EL-groepen altijd een hogere 5-FU cumulatieve permeatieconcentratie dan de 5E-groepen (figuur 2a). Bovendien was de retentiehoeveelheid van 5-FU in de 5EL-groep 24,42 ± 4,37 μg/cm 2 , wat hoger is dan de 5E-groep (12,45 ± 1,64 μg/cm 2 , p < 0.01, n = 6) (Fig. 2b). Dit resultaat suggereerde dat CO2 fractionele laserbestraling kan 5-FU-bevat liposoom aanzienlijk bevorderen via humaan hypertrofisch littekenweefsel en in vitro 5-FU-retentie in hypertrofisch littekenweefsel helpen.
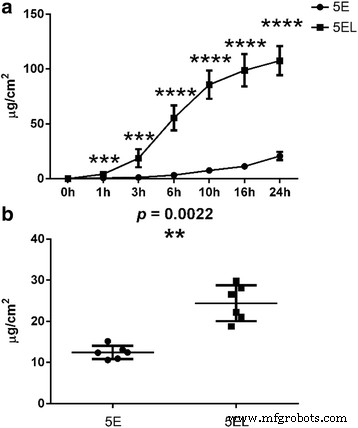
CO2 fractionele laser bevordert de 5E-permeabiliteit door hypertrofische littekens in vitro. een Vergelijking van de permeatie van de 5E- en 5EL-groep in een 24-uurs studie van humaan hypertrofisch litteken in vitro. Waarden werden uitgedrukt als het gemiddelde ± SD. n = 6. b De accumulatieve retentie van 5-FU in hypertrofisch litteken in vitro na 24 uur aanbrengen. n = 6. ***p waarde < 0,001 werd als statistisch extreem significant beschouwd, ****p waarde < 0.0001 werd als statistisch zeer extreem significant beschouwd
De diepte en mate van 5-FU-penetratie werden bepaald met behulp van 5E gelabeld met Rho om het versterkende penetratie-effect van CO2 te evalueren fractionele laser in vitro. Fluorescentietest werd gebruikt om de intensiteit van 5E- en 5EL-groepen aan te geven op 1, 6 en 24 uur na behandeling met 5-FU (figuur 3a). De resultaten toonden aan dat na 1 uur 5EL-behandeling de Rho-fluorescentie werd verdeeld in de ondiepe laag van de epidermis en dermis, vooral rond CO2 fractionele laser-geïnduceerde vergassingszone. In tegenstelling, zonder CO2 fractionele laserbestraling, Rho-fluorescentieverdeling was beperkt tot het epidermisgebied in de 5E-groep. Na een behandeling van 6 uur in de 5EL-groep, breidde de Rho-fluorescentie zich uit naar de diepe dermis en vertoonde meer accumulatie. Hoewel de fluorescentieverdeling van de 5E-groep in de dermis begon te verschijnen, nam de fluorescentie-intensiteit geleidelijk af van de dermis naar de epidermis. Na een behandeling van 24 uur was de fluorescentie van twee groepen wijd verspreid in het hele huidweefsel, maar de intensiteit van de fluorescentie in de 5EL-groep was significant hoger. Verder werd Release Version 4.0 SP2 beeldanalysesoftware gebruikt voor kwantitatieve analyse om de fluorescentie-intensiteit voor beide groepen te berekenen. De kwantitatieve analyseresultaten lieten een significant verhoogde Rho-fluorescentie-intensiteit zien in de 5EL-groep dan in de 5E-groep (1 uur:59.61 ± 6.39 vs.6.39 ± 1.64, p < 0.0001; 6 u:163,32 ± 13,23 vs. 49,89 ± 4,01, p < 0.0001; 24 uur:270,36 ± 8,73vs. 148.25 ± 16.89, p <-0,0001) (Fig. 3b). Samengevat, CO2 fractionele laserbestraling bevordert in vitro aanzienlijk de 5E-penetratie in het menselijke hypertrofische littekenweefsel.
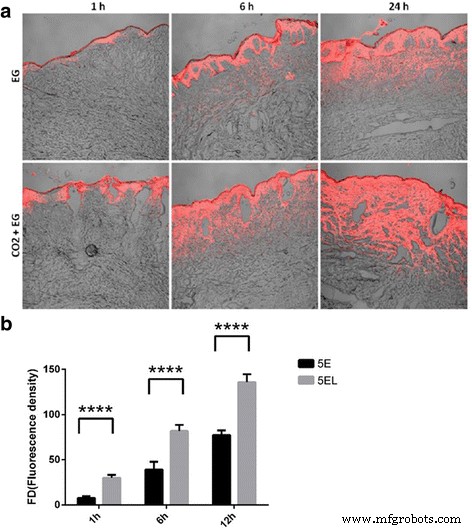
CO2 fractionele laser bevordert de doorlaatbaarheid door hypertrofische littekens in vitro. een De rode fluorescentie wordt gelabeld met ethosomen doordrongen hypertrofische littekenweefsels na 1, 6 en 24 uur in vitro. b De fluorescentie-intensiteit van met Rhodamine 6GO gelabelde ethosomen op hypertrofisch littekenweefsel in vitro na 1, 6 en 24 uur. ****p waarde < 0.0001 werd als statistisch zeer extreem significant beschouwd
Duur van CO2 Fractionele laser verbetert 5-FU-penetratie in vivo
Om meer substantieel bewijs van CO2 . te verkrijgen fractioneel lasereffect, hebben we 5-FU-penetratie in vivo uitgevoerd met behulp van een hypertrofisch littekenmodel van konijnen. Opstelling van het hypertrofische littekenmodel bij konijnen werd beschreven als methode. Verschillende tijdstippen (3 uur, 6 uur, 12 uur, 24 uur, 3 dagen en 7 dagen) na toepassing van CO2 fractionele laser-, 5E- of 5EL-behandeling werd uitgevoerd en de fluorescentieverdeling werd onmiddellijk bepaald door CLSM (Fig. 4). Rho-fluorescentie was uitgebreid zichtbaar en wijdverspreid in de dermislaag van de hypertrofische littekens van het konijnenoor, die dichter bij de ablatieve zone lagen (figuur 4a). Deze resultaten kunnen erop wijzen dat Rho gemengd met 5E voornamelijk infiltreert via het poreuze kanaal na CO2 fractionele laserstraling. Fluorescentie kan worden gedetecteerd in de ablatieve zone rond het dermale weefsel na 6 uur 5EL, zelfs met een klein distributiegebied (figuur 4b). Het distributiegebied van de fluorescentie blijft 12 uur na de medicamenteuze behandeling krimpen, wat aangeeft dat microporeuze kanalen geleidelijk worden gesloten wanneer de wond geneest (figuur 4c). Na 24 uur, 3 dagen en 7 dagen behandeling van CO2 fractionele laserbestraling, fluorescentie kon alleen worden gevonden in de korstporie rond openingen en geen penetratie in de dermis (Fig. 4d-f), wat suggereert dat CO2 het fractionele laserpenetratie-effect is verdwenen met volledige re-epithelialisatie van de epidermis. Onze gegevens suggereerden dat het openen van microkanalen een cruciale rol speelt bij de penetratie van geneesmiddelen met 5EL-behandeling. Daarna berekenden we de openingssnelheid van de microkanalen van respectievelijk 3 uur, 6 uur, 12 uur, 24 uur, 3 dagen en 7 dagen na laserbestraling. Op de tijdstippen van 3 en 6 uur waren alle microporeuze kanalen open, wat aangaf dat de openingspercentages van microkanalen 100% waren. De openingssnelheid van microkanalen begon af te nemen tot 90,59% om 12 uur en 15,58% om 24 uur. In het bijzonder waren alle microporeuze kanalen 3 en 7 dagen na 5EL-behandeling gesloten. Alles bij elkaar genomen suggereren deze resultaten dat CO2 fractionele laser regelt de penetratie van geneesmiddelen in hypertrofisch littekenweefsel van konijnen in vivo.
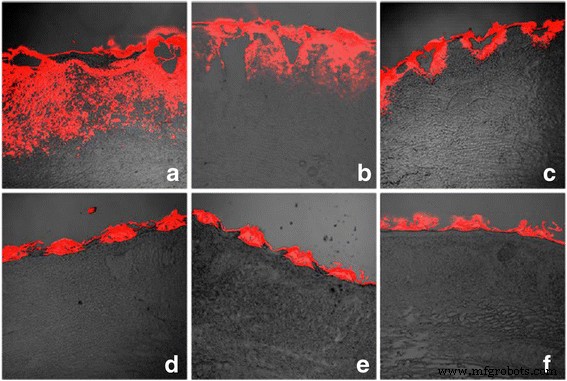
CO2 fractionele laser bevordert de openingssnelheid van microkanalen in vivo. De rode fluorescentie is gelabeld ethosomen doordringen konijnenoor hypertrofische littekenweefsels 0 h (a ), 6 u (b ), 12 u (c ), 24 u (d ), 3 dagen (e ), en 7 dagen (f ) na CO2 fractionele laserbehandeling in vivo
Het therapeutische effect van 5EL op hypertrofisch litteken in vivo
Om de 5EL-behandeling goed te begrijpen, hebben we de relatieve dikte van het hypertrofische litteken van konijnenoren bepaald. Na het opzetten van een hypertrofisch littekenmodel van konijnenoor werden relatieve diktewaarden van voor en na 5EL-behandeling berekend. Er werd geen significant verschil gevonden in groepen vóór de behandeling. De relatieve dikte van de 5EL-groep was echter 1,27 ± 0,15, wat significant lager was dan de 5E-groep (1,52 ± 0,10, p < 0.05) en onbehandeld (1.61 ± 0.15, p < 0.0001) groep (Fig. 5). Interessant genoeg was er geen significante verandering tussen de CO2 alleen laserbehandeling en de 5EL-groep. Deze gegevens suggereren dat CO2 fractionele laser speelt een dominante rol bij het genezen van hypertrofisch litteken van konijnenoor in vivo.
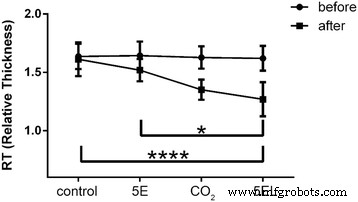
Vergelijking van de relatieve dikte van hypertrofische littekens van konijnen voor en na verschillende behandelingen. 5EL:de enthosomale gels ingekapseld met 5-FU gecombineerd met CO2 fractionele laser, n = 14; CO2 :CO2 alleen fractionele laser, n = 12; 5E groep:de enthosomale gels ingekapseld met 5-FU, n = 14; controle:leeg, n = 16. *p waarde < 0,001 werd als significant beschouwd, ****p waarde < 0.0001 werd als statistisch zeer extreem significant beschouwd
We vergeleken ook de morfologie van hypertrofisch litteken van konijnenoor om het verschil te bepalen bij het gebruik van CO2 fractionele laser. In de 5EL-groep werden hypertrofische littekens afgeplat en werd de kleur significant lichtroze (figuur 6a-b). In CO2 fractionele laserbehandeling, nam de hypertrofische littekendikte tot op zekere hoogte af en de kleur veranderde in bleekrood (Fig. 6c-d). In de 5E-groep nam de hypertrofische littekendikte enigszins af, maar de kleur bleef helderrood (Fig. 6e-f). Ten slotte was er geen significante verandering in de onbehandelde groep in vergelijking met vóór de behandeling (Fig. 6g-h). Vervolgens werd H &E-kleuring gebruikt voor pathologische analyse in 7 dagen na behandeling voor deze vier groepen op hypertrof littekenweefsel van konijnenoren (Fig. 7). De 5EL-groep en CO2 fractionele laserbehandeling alleen groepen vertoonden de verminderde dermale laagdikte van hypertrofische littekens en puntachtige korst met zeldzame oppervlakkige dermis collageenvezels nodulaire of spiraalvormige opstelling (Fig. 7a-b). Een groot aantal dermale collageenvezelpenetratie, ongeordende opstelling van collageenvezels en oppervlakkige dermis-nodulaire of spiraalvormige opstelling werden gevonden in de 5E-groep en de onbehandelde groep (Fig. 7c-d). Een andere belangrijke evaluatiemethode voor hypertrofisch litteken is de litteken-elevatie-index (SEI). Vergelijkbaar met patroon van relatieve dikte, SEI van 5EL-groep (1.16 ± 0.08) en CO2 de groep met alleen fractionele laserbehandeling (1,22 ± 0,10) was significant verlaagd in vergelijking met de 5E-groep (1,32 ± 0,13) en de onbehandelde groep (1,49 ± 0,08) (Fig. 8). Alles bij elkaar tonen morfologie-analyse en SEI-berekeningsgegevens CO2 fractionele laser werkt op genezing van hypertrofisch litteken van konijnenoor in vivo.
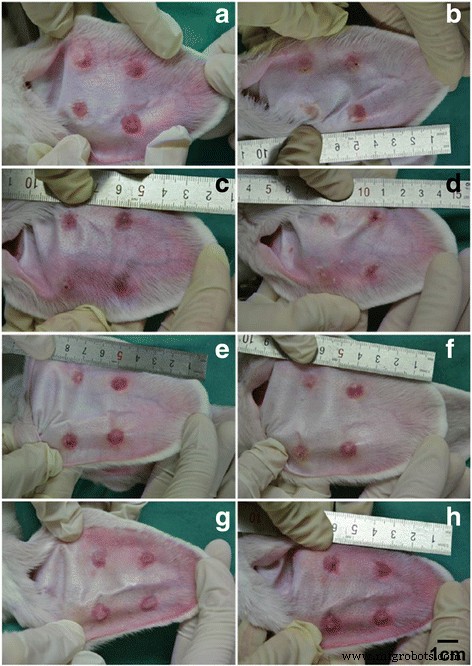
Fotografische beeldvorming van hypertrofische littekens van konijnen voor en na verschillende behandelingen gedurende 7 dagen. De 5EL-groep:de enthosomale gels ingekapseld met 5-FU gecombineerd met CO2 fractionele laser, voor (a ) en na (b ) behandeling gedurende 7 dagen; CO2 groep:CO2 fractionele laser, voor (c ) en na (d )behandeling gedurende 7 dagen; 5E groep B:de enthosomale gels ingekapseld met 5-FU, voor (e ) en na (f ) behandeling gedurende 7 dagen; en blanco groep:blanco, voor (g ) en na (u ) behandeling van 7 dagen
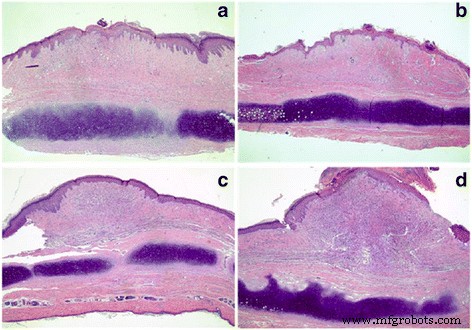
H&E histologische analyse van hypertrofische littekens van konijnen na verschillende behandelingen gedurende 7 dagen. De 5EL-groep:de enthosomale gels ingekapseld met 5-FU gecombineerd met CO2 fractionele laser (a ); CO2 groep:CO2 fractionele laserbehandeling (b ); 5E groep:de enthosomale gels ingekapseld met 5-FU (c ); en blanco groep:blanco (d ). Originele vergrotingen:× 40
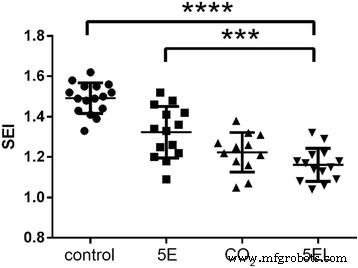
Vergelijking van SEI van hypertrofische littekens van konijnen na verschillende behandelingen gedurende 7 dagen. 5EL:de enthosomale gels ingekapseld met 5-FU gecombineerd met CO2 fractionele laser, n = 14; CO2 :CO2 fractionele laser, n = 12; 5E:de enthosomale gels ingekapseld met 5-FU, n = 14; controle:leeg, n = 16. ***p waarde < 0,001 werd als statistisch extreem significant beschouwd en ****p waarde < 0.0001 werd als statistisch zeer extreem significant beschouwd
Discussie
Medicamenteuze behandeling is de belangrijkste behandelingsbenadering, voornamelijk topisch of als lokale injecties, voor niet-chirurgische behandeling van hypertrofische littekens. Vanwege de bijwerkingen van verschillende geneesmiddelen is lokale injectie vaak beperkt tot kleine doseringen en is er dus slechts een klein aantal behandelingen mogelijk. Vanwege de korte halfwaardetijd van medicijnen, vereisen aanhoudende hoge concentraties in littekens herhaalde injecties [6, 30, 31]. Bovendien, omdat het littekenweefsel erg geconcentreerd is en er vaak hevige pijn bij injecties wordt ervaren, accepteren patiënten vaak geen behandeling. Although external drug usage having advantage of being convenient, painless, with long-term stability, low side effects, avoiding to affection of the gastrointestinal environment [7, 8], there are several limitations. First of all, topical and injected drugs availability is limited by special pathological scar tissue structure, which presents with a thickening of the stratum corneum and hyperplasia of the dermis, which hinders the penetration of the drug and achieving an effective therapeutic concentration. Recent reports have proven this and described how external use of drugs inefficiently penetrates the scar tissue [4, 9]. Ethosomes, proposed by Touitou et al. [10] in 2000 as a transdermal drug carrier, have been widely reported [11, 12, 32]. In this study, we improved the ethosomes preparation process to nano-level (particle size 70~90 nm). This change of a new nanoscale dimensions and the spatial conformation of the ethosomes allow them to penetrate into the scar tissue through a narrowly tightly connected cell gap not only due to the small size, but also by the similarity to the cell membrane of scar tissue cells. Based on such penetration mechanisms, ethosomes become a convenient transdermal drug carrier [14, 33, 34]. However, the anti-scar drug 5-FU encapsulated with ethosomes is mainly concentrated in the epidermis and dermis, which is not conducive to fibroblasts in deeper layers of the dermis. Therefore, our purpose is to explore a method that would allow to increase the penetration of drugs and would promote the uniform dispersion of drugs in scar tissue.
So far, commonly used methods to promote the penetration are divided into two categories:the promotion of chemical substances and physical methods to enhance permeability. The physical enhancement techniques include electroporation, iontophoresis, laser, microdermabrasion, microneedle, pressure, radiofrequency induction, and sonography [35]. There are many different types of lasers that have been shown to promote percutaneous administration, and ablative fractional lasers become the most popular laser in recent years for promoting drug penetration into the skin [20]. Ablative fractional laser can not only extremely reduce drug dosage, but also be conducive to drug penetration into deep skin and achieve high local concentrations to obtain a therapeutic effect. CO2 fractional laser, Erbium-doped Yttrium Aluminum Garnet (Er:YAG) fractional laser, and Erbium-doped Yttrium Scandiu Gallium Garnet (Er:YSGG) fractional laser can produce ablative zone or microporous channels on the surface of the skin. Compared with Er:YAG fractional laser (2940 nm wavelength) and Er:YSGG fractional laser (2790 nm wavelength), CO2 fractional laser (10,600 nm wavelength) has lower water absorption coefficient, larger thermal damage, and greater destruction effect of stratum corneum of the epidermis, which is more conducive to promote penetration effect [36].
In this study, 5-FU retention in the 5EL group (24.42 ± 4.37 μg / cm 2 ) was significantly higher than in the 5E group (12.45 ± 1.64 μg/cm 2 ) in scar tissue of 24 h treatment in vitro. Additionally, in Rho-labeled assay, 5EL group has shown higher fluorescence intensity than 5E group at 1-, 6-, and 24-h treatment time points. Image analysis showed that fluorescence can be found distributed in the gasification zone and surrounding dermal tissue matrix after 1-h CO2 laser treatment in the 5EL group, and the fluorescence in 5E group is only distributed in the epidermis. After 6- and 24-h treatment, diffuse fluorescence range is wider and fluorescence intensity is higher in the 5EL group than in the 5E group. CO2 fractional laser-induced gasification zone provided an effective way for drug penetration through the skin scar tissue, enlarge range of dermis penetration depth, and retention content in scar tissue. There are three different forms of thermal effect damage by CO2 fractional laser acting on the skin or scar tissue, from center to outliner, the gasification zone, thermal coagulation necrosis zone, and thermal denaturation zone [37]. Fluorescence data showed that Rho fluorescence was distributed from more concentrated gasification zone to diffused tissue, suggesting that there is no effect for permeation of drugs in thermal coagulation necrosis zone and thermal denaturation zone, which also confirmed the feasibility of CO2 fractional laser for the promotion of topical anti-scarring drug penetration. Together, CO2 fractional laser is conducive to more anti-scarring drugs 5-FU retention in scar tissue and achieve high drug concentration required to strengthen the anti-scarring effect.
The duration of CO2 fractional laser enhancing 5E was evaluated by CLSM on rabbit ear hypertrophic scar in vivo. The opening rates of microporous channels for drug permeation were 100% (0 h), 100% (6 h), 90.59% (12 h), and decreased to 15.58% (24 h) after CO2 fractional laser treatment of hypertrophic scar. Moreover, microporous channel opening rates dropped to zero on 3 and 7 days, and the drug can no longer penetrate into the skin through these channels. These results were consistent with that of epidermal re-epithelialization after ablative fractional laser irradiation, which is the skin wound around the keratinocytes to the wound defect migration and proliferation, covering the wound to form a complete layer of cells formed by the epidermis. When the dermal layer of skin was wound, the repair process will immediately start and quickly rebuild the skin barrier [38, 39]. The whole skin tissue trauma repair process can be divided into four continuous and overlapping steps:coagulation, inflammation, re-epithelialization, and remodeling [40]. Human skin after ablation of the fractional laser irradiation injury area (including the gasification area and coagulation necrosis area) complete epidermal re-epithelialization in 2 to 3 days and dermal remodeling for at least 4 weeks [41]. Thus, although the lesion in the dermis does not heal within 24 h after the CO2 laser treatment, the epidermis has completed the complex epithelization, including the formation of the stratum corneum, where the topical drug could not penetrate through channels. Taken together, epidermis, especially the stratum corneum, is still the main barrier for drug penetration through the skin.
In addition, our CLSM data showed both in in vitro human hypertrophic scar skin and in vivo rabbit ear hypertrophic scar skin, Rho-labeled 5E can penetrate the necrotic coagulation layer and the formation of crust on the surface after the CO2 fractional laser irradiation. It suggested that the skin under the crust but not the coagulation necrotic layer and crust tissue can impede the penetration of drug. Therefore, 24 h is the critical time-point for the effect of CO2 fractional laser on the penetration effect of hypertrophic scar in rabbits.
It has been reported that the clinical application of exfoliative fractional laser is an effective method to treat various skin diseases (such as solar keratosis, basal cell carcinoma, Bowen’s disease, etc.) [25,26,27,28]. However, the clinical efficacy of CO2 fractional laser in combination with drugs has not been explored in the treatment of hypertrophic scars [42, 43]; in particular, there are no reports of combined CO2 fractional laser (physical technique) with anti-scar drug nano-level ethosomes (chemical substances promoting scar penetration) for the treatment of hypertrophic scars. Using in vivo study, we performed a rabbit hypertrophic scar model for validation of CO2 fractional laser protocol. On the seventh day after intervention, the relative thickness of the four groups of hypertrophic scar was measured:experimental group (CO2 fractional laser combined with 5-FU EG):1.27 ± 0.15
The toxicity of the ethosomes should be a big concern in this study. Nevertheless, after reviewing literature, there are no results exhibiting the toxicity of ethosomes in vitro or in vivo study [44,45,46]. The permeability mechanism of ethosomes is mainly as follows:high concentration of ethosomes, the flexibility, and fluidity of ethanol liposome membrane, makes ethosomes deform in the process of transmission, and enhances the permeability in scar tissue [47].
Although the difference between the experiment group and control group A was not statistically significant, the relative thickness and SEI of the experimental group was smaller than that in the control group A. Both groups were treated with CO2 fractional laser, with or without 5E. This finding suggests that CO2 fractional laser may have the dominant role, which overtakes the minor effect of 5E drug in the final anti-scar effect.
Conclusion
CO2 fractional laser can rapidly and significantly promote 5-fluorouracil encapsulated ethosomes’ permeability through hypertrophic scars in vitro. CO2 fractional laser is a potentially efficient method of promoting drug permeation in hypertrophic scars’ treatment. Our hypertrophic scar model (rabbit) showed that CO2 fractional laser combined with external-loaded 5-fluorouracil encapsulated ethosomes can effectively cure hypertrophic scars. Also, CO2 fractional laser itself can facilitate collagen remodeling in hypertrophic scar of rabbit ears. CO2 fractional laser can significantly promote the permeation of 5-fluorouracil encapsulated ethosomes, but the effect begins to relinquish 24 h after CO2 fractional laser irradiation, which indicates that 24 h is a critical period.
Nanomaterialen
- CO2 versus Nd-lasersnijden:wat is het verschil?
- Wat gaat u maken met een CO2-lasersnijder?
- Lightburn-lasersoftware inbegrepen bij Mantech-lasermachines
- Fibre Laser vs CO2 Laser
- CNC-freesmachines of CO2-lasermachines
- Experimenteel onderzoek naar stabiliteit en natuurlijke convectie van TiO2-water nanovloeistof in behuizingen met verschillende rotatiehoeken
- Experimenteel onderzoek naar de stromings- en warmteoverdrachtskenmerken van TiO2-water-nanovloeistoffen in een spiraalvormig gecanneleerde buis
- Onderzoek naar het effect van het beïnvloeden van richting op het schurende nanometrische snijproces met moleculaire dynamiek
- Tapered Quantum Cascade Laser Arrays geïntegreerd met Talbot Cavities
- Vergelijkende studie van negatieve capaciteitsveldeffecttransistoren met verschillende MOS-capaciteiten
- Waarom is een CO2-lasergraveermachine populair?



