Zink
Achtergrond
Zink is een elementair metaal. Het wordt in het periodiek systeem vermeld als "Zn", met een atoomnummer van 30 en een atoomgewicht van 65,37, en het smelt bij 788 ° F (420 ° C). Zink is meestal een grijze metaalkleur, maar het kan worden gepolijst tot een glanzende zilveren glans. In de natuur wordt het alleen gevonden als een chemische verbinding, niet als puur zink, en kan het worden gebruikt als grondstof voor gietstukken en coatings.
Tijdens het tijdperk van het Romeinse rijk gebruikten mensen zink om koper in messing te legeren voor wapens. Bij dit ruwe proces werd het zink opgevangen door het koper tijdens het verhitten van de ertsen, hoewel men zich toen nog weinig realiseerde over het belang van zink in de metallurgie. De naam zink is mogelijk afgeleid van het Duitse woord "zinn", wat tin betekent. De wetenschappelijke ontdekking van zink wordt toegeschreven aan Nadreas Sigismund Marggraf, een Duitse chemicus die in 1746 puur zink isoleerde. De eerste productiefaciliteit, of smelter, werd kort daarna in Bristol, Engeland opgericht door William Champion.
Slechts ongeveer 5% van 's werelds zinkvoorraad wordt gewonnen in de Verenigde Staten, en de rest komt voornamelijk uit India, Mexico en Canada. Wereldwijd wordt ongeveer 6,7 miljoen ton zinkerts geproduceerd. Ongeveer twee derde van het zink dat in de Verenigde Staten wordt gebruikt, wordt geïmporteerd.
Toepassingen
Zink wordt voornamelijk gebruikt voor het verzinken van staal tegen corrosie, het spuitgieten van ingewikkelde machineonderdelen en in batterijen en andere elektrische toepassingen. Zink wordt ook gelegeerd met koper om messing te vormen.
Het galvaniseren van staal omvat het aanbrengen van een dunne laag zink op alle blootgestelde oppervlakken van het staal om corrosie te voorkomen. Zink biedt een uitstekende corrosieweerstand omdat het gemakkelijker wordt geoxideerd door de atmosfeer. Oxidatie treedt op wanneer metaal wordt blootgesteld aan lucht of water, en elektronen van het metaal worden overgebracht naar de zuurstof. Wanneer zink stevig aan staal is gebonden, maakt het zink zijn elektronen gemakkelijker vrij dan het staal, waardoor het sterkere metaal eronder intact blijft. Het aanbrengen van de zinklaag wordt bereikt door het staal in gesmolten zink te dompelen of door het staal elektrolytisch te bekleden met zink, net zoals bij verchromen.
Spuitgietlegeringen bevatten doorgaans 96% zink en 4% aluminium. Het spuitgietproces maakt gebruik van een tweedelige stalen matrijs en een gietpers om de matrijshelften bij elkaar te houden tijdens de injectie van het gesmolten metaal. In de stalen matrijs bevindt zich een holte die het negatieve beeld heeft van het te gieten onderdeel. Het gesmolten metaal wordt onder druk in de holte geïnjecteerd, waardoor de hele leegte nauwkeurig wordt gevuld. Het metaal koelt af en de pers opent de matrijshelften, waardoor het gevormde deel zichtbaar wordt. De gegoten zinkdelen zijn zeer dicht bij de gewenste vorm en vereisen weinig bewerking voordat ze in een samenstel worden geplaatst. Typische toepassingen zijn onder meer onderdelen van kopieerapparaten, vliegtuigen en medische instrumenten. Autofabrikanten gebruiken gegoten zink voor emblemen, lijstwerk, deurgrepen en beugels. Spuitgietstukken van zink zijn gemakkelijk verchroomd voor duurzaamheid en uiterlijk.
Een unieke toepassing van zink profiteert in het bijzonder van zijn vermogen om zijn corrosieweerstandseigenschappen over te dragen door elektrisch contact. Deze toepassing wordt een "opofferingsanode" genoemd. De anodes, gemaakt van bijna 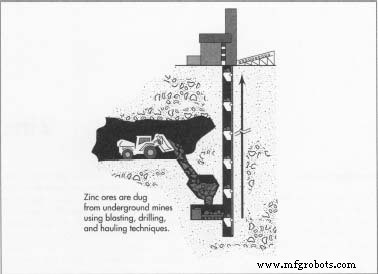 puur zink, zijn vastgeschroefd aan aluminium scheepsmotoren. Tijdens gebruik in water, vooral zout water, vormt de oxidatie een zwakke elektrische stroom, die de romp en motoronderdelen kan aantasten. Aangezien zink gemakkelijk wordt geoxideerd in aanwezigheid van deze elektrische stroom, "offert" het zichzelf op door snel te corroderen, waardoor alle elektrische onbalans in het schip wordt verbruikt. De resterende aluminium romp en motor zijn hierdoor niet gecorrodeerd. Aangezien het wordt verbruikt, moet de anode worden vervangen om voortdurende bescherming te verzekeren.
puur zink, zijn vastgeschroefd aan aluminium scheepsmotoren. Tijdens gebruik in water, vooral zout water, vormt de oxidatie een zwakke elektrische stroom, die de romp en motoronderdelen kan aantasten. Aangezien zink gemakkelijk wordt geoxideerd in aanwezigheid van deze elektrische stroom, "offert" het zichzelf op door snel te corroderen, waardoor alle elektrische onbalans in het schip wordt verbruikt. De resterende aluminium romp en motor zijn hierdoor niet gecorrodeerd. Aangezien het wordt verbruikt, moet de anode worden vervangen om voortdurende bescherming te verzekeren.
In een toepassing die vergelijkbaar is met de opofferingsanode, wordt zink gebruikt als onderdeel bij de productie van batterijen. De droge celbatterij creëert een chemische reactie met zink in een metalen behuizing (of "blik") die resulteert in een spanningspotentiaal tussen twee verbindingen. Een elektrisch apparaat, zoals een zaklamp of draagbare radio, kan worden aangesloten op de batterij en gevoed worden door de geproduceerde elektriciteit. Aldus verbonden, handhaaft de reactie de elektrische stroom voor de duur van de beschikbare chemische reactanten.
Zink als verbinding wordt gebruikt in farmaceutische producten, rubber, cosmetica, verf en keramisch glazuur. Andere verbindingen gebruiken zink in kathodestraalbuizen, soldeervloeistof en houtconserveringsmiddelen.
Het fabricageproces
Mijnbouw
- 1 Zinertsen worden gedolven uit ondergrondse mijnen met behulp van conventionele straal-, boor- en sleeptechnieken. De ertsen komen voor als zinksulfide (ook wel sfaleriet genoemd), zinkcarbonaat (smithsonite), zinksilicaat (calimine) en in verbindingen van mangaan en ijzer (openhartig). Zinkerts wordt soms gedolven in combinatie met zilver of lood ertsen. Naast het erts zelf zijn olie en zwavelzuur nodig voor de afbraak van de ertsen; en elektriciteit, cokes of aardgas zijn nodig om de warmte-energie voor het smelten te leveren.
Schuimflotatie
- 2 Zink kan worden geproduceerd door een proces dat schuimflotatie wordt genoemd en dat ook wordt gebruikt voor de reductie van koper- en looderts. Dit proces omvat het vermalen van het zinkerts tot een fijn poeder, het mengen met water, dennenolie en flotatiechemicaliën, en vervolgens het mengsel roeren om het zink naar het oppervlak te "drijven". Een verscheidenheid aan chemicaliën wordt gebruikt om de belangrijke zinkdeeltjes te coaten en te voorkomen dat ze door het water worden bevochtigd. Vervolgens wordt lucht geïnjecteerd en de gecoate mineralen
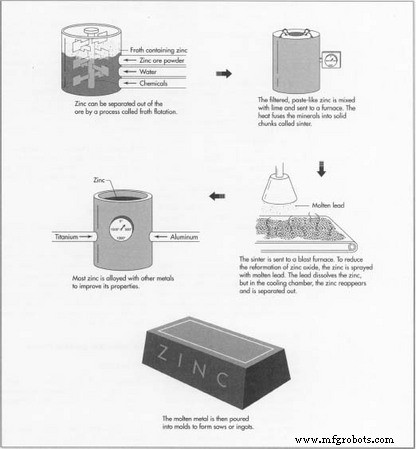 hechten zich aan de bubbels. De bewerking wordt uitgevoerd in een vat en geschud met een waaier. De roterende waaier trekt de lucht langs de standpijp die de waaieras omringt en verspreidt deze door het mengsel of "pulp". Het zink stijgt naar boven en het residu blijft in de bodem van de pulp, omdat het niet aan de bellen kan hechten. Automatische schrapers verwijderen het met mineralen beladen schuim dat het zink bevat.
hechten zich aan de bubbels. De bewerking wordt uitgevoerd in een vat en geschud met een waaier. De roterende waaier trekt de lucht langs de standpijp die de waaieras omringt en verspreidt deze door het mengsel of "pulp". Het zink stijgt naar boven en het residu blijft in de bodem van de pulp, omdat het niet aan de bellen kan hechten. Automatische schrapers verwijderen het met mineralen beladen schuim dat het zink bevat.
Filteren
- 3 Het schuim wordt gefilterd om het water en de vloeibare oliën te verwijderen. De pasta-achtige rest wordt gemengd met kalk en naar een oven gestuurd. De oven roostert het mengsel bij 2500 ° F (1371 ° C), die de mineralen versmelt tot vaste brokken die sinter worden genoemd. Op dit punt is het materiaal volledig omgezet in zinkoxide.
Smelten
- 4 Het volgende reductieproces gebruikt een hoogoven om het bereide erts te smelten tot zijn elementaire componenten. De hoogoven wordt aangedreven door elektriciteit, cokes of aardgas, die temperaturen tot 2200 ° F (1204 ° C) genereren. Dit genereert echter ook koolstofdioxide, dat recombineert met het zink terwijl het afkoelt om zinkoxide opnieuw te vormen. Om deze reformatie te verminderen wordt het zink, terwijl het nog heet is, besproeid met gesmolten lood. Het lood, bij 1022°F (550 °C), lost het zink op en voert het naar een andere kamer, waar het wordt afgekoeld tot 824°F (440 °C). Bij deze temperatuur scheidt het lichtere zink zich uit het lood en wordt van bovenaf afgevoerd. Het lood wordt opnieuw verwarmd en teruggevoerd naar de hoogoven.
Verfijning
- 5 Verdere metaalverbetering kan worden bereikt door het zink enkele uren gesmolten en ongestoord te houden. In deze toestand bezinken ijzer en andere verontreinigingen naar de bodem, waardoor het bijna zuivere zink voorzichtig van de bovenkant kan worden afgezogen en in blokken kan worden gegoten.
Legeren
- 6 Het meeste zink wordt voor gebruik gelegeerd met andere metalen om de eigenschappen te verbeteren. Legeren omvat het opnieuw smelten en mengen van het zink met andere metalen in precieze verhoudingen. Er wordt bijvoorbeeld ongeveer 4% aluminium toegevoegd om de gietkwaliteit en de levensduur van de matrijs in het spuitgietproces te verbeteren. Andere toegevoegde legeringen zijn kleine hoeveelheden titanium, koper en magnesium. Na het legeren wordt het gesmolten metaal in zeugenmallen en ingots gegoten. Zeugen kunnen enkele duizenden ponden wegen, terwijl ingots ongeveer 45 pond (20 kg) wegen.
Kwaliteitscontrole
Metaallegeringen worden geïnspecteerd door een proces dat spectrografische analyse wordt genoemd. Het metaal wordt verbrand onder een beschermkap met behulp van een elektrische boog. Het licht dat door het brandende metaal wordt uitgestraald, wordt door een apparaat geleid dat veel weg heeft van een prisma, dat het licht in al zijn individuele kleuren breekt. Elk element heeft een andere set kleuren, of spectrum, dat lijkt op een vingerafdruk. Elk vreemd materiaal zal het spectrum veranderen en daarbij zijn unieke kleurenspectrum tonen en het identificeren. De computer in de spectrograaf gebruikt sensoren om deze kleuren op te pikken. Het computerprogramma maakt vervolgens een afdruk die elk element in het spectrum en de concentratie in het metaal identificeert. Elementen kunnen worden verminderd of verhoogd om de samenstelling te veranderen.
De Toekomst
Vanwege de sterkte-gewichtsverhouding van zink is het gebruik ervan door de auto-industrie als spuitgietwerk de afgelopen jaren afgenomen. Magnesium, aluminium en kunststoffen hebben veel zinktoepassingen overgenomen. Het gebruik van zink om carrosseriedelen te verzinken neemt echter toe. Veel voertuigen worden tegenwoordig beschermd door verzinking, waardoor de fabrikant uitgebreide garanties kan bieden voor problemen met carrosserieroest bij nieuwe auto's.
Productieproces



